首页 > 医疗资讯/ 正文
前言
胃癌是全球最常见的恶性肿瘤之一,表现出显著的分子和表型异质性。2020年胃癌新增病例1089103例,死亡768793例,是全球第五大常见癌症和第四大癌症死亡原因。胃癌的流行病学分布因性别和地理区域而异,男性的发病率是女性的两倍,东亚和东欧的发病率更高。胃癌通常可以根据两个解剖亚型分类,此外也包括不同的组织学和分子亚型。
胃癌发生遗传畸变的积累,包括生长因子和/或受体的表达、DNA损伤反应的改变和基因组稳定性的丧失,这些表型为靶向治疗提供了各种靶点。目前癌症治疗的有效靶点包括HER2、CLDN18.2、FGFR、VEGFR、TROP2、PD-L1和Dickkopf-related protein 1(DKK1)。靶向治疗采用小分子激酶抑制剂(阿帕替尼、奈拉替尼、吡咯替尼)、单克隆抗体(曲妥珠单抗、帕妥珠单抗)、双特异性抗体(ZW25、JSKN003)、CAR-T疗法和抗体偶联药物(ADC)。
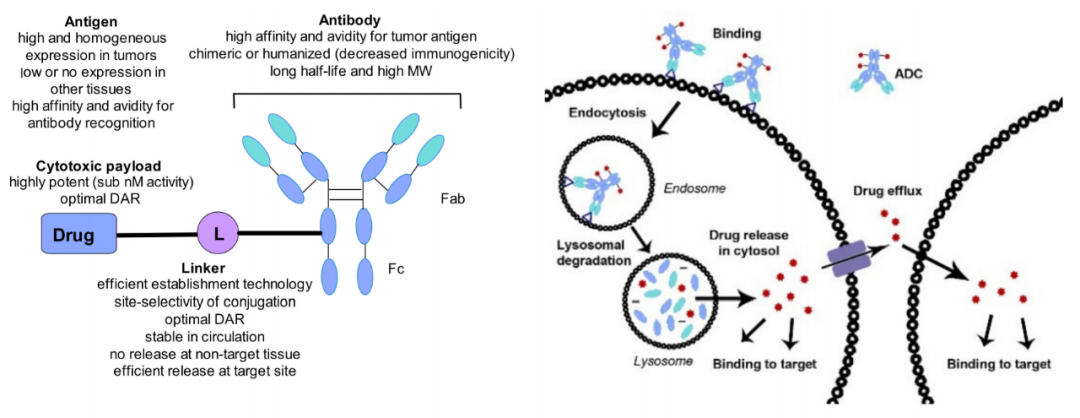
ADC是由靶向特异性抗原的单克隆抗体与小分子细胞毒性药物通过连接子链接而成,兼具传统小分子化疗的强大杀伤效应及抗体药物的肿瘤靶向性。ADC对抗原的识别导致ADC通过内吞途径进入细胞内,通过溶酶体降解后,有效载荷以生物活性形式释放并发挥作用,导致癌细胞死亡。目前,全球已有100多种候选ADC药物进行临床试验,其中15种ADC已获批上市。其中,DS-8201a、RC48和IMMU-132已被批准用于晚期胃癌治疗。因此,开发新的ADC药物和治疗模型很重要,它们可能为选择有限的晚期胃癌患者提供新的可能性。
ADC在胃癌的治疗靶点
目前临床上批准用于胃癌治疗的靶向人表皮生长因子受体2(HER2)的ADC可能无法完全满足患者的治疗需求。因此,越来越多的新靶点正在临床试验中被探索和使用。EGFR, HER3,claudin18.2、GCC、TROP2和SLC44A4均在胃癌患者中过表达,已成为ADC研究的热门靶点。
HER2
HER2作为胃癌最早、最成熟的生物标志物,一直是ADC靶向治疗的重点研究对象。T-DM1于2013年获得美国食品药品监督管理局(FDA)批准,用于治疗HER2-阳性转移性乳腺癌。然而,GATSBY研究表明,与紫杉烷相比,T-DM1对HER2阳性的晚期胃癌患者的OS和无进展生存期(PFS)没有益处,这可能是由于这些癌症中的HER2异质性。因此,鉴定胃癌中的异质性表达可能是下一步的研究方向。
与T-DM1相比,trastuzumab deruxtecan(DS-8201a,T-DXd)由于其较高的膜通透性而表现出强大的旁观者效应,可以靶向低HER2表达和HER2异质性胃癌患者。临床前实验表明,DS-8201a通过抑制ADCC和Akt磷酸化在HER2阳性NCI-N87模型中表现出抗肿瘤作用。此外,DS-8201a与吡咯替尼联合使用可促进泛素化,并增强T-DXd在胃癌细胞中的吸收。RC48(disitamab vedotin),另一种ADC,于2021年获得中国国家医疗产品管理局的批准,在胃癌患者中显示出良好的抗肿瘤活性。目前正在进行进一步测试,以评估其治疗胃癌的疗效(NCT05313906、NCT05241899、NCT05980481)。
此外,一些未上市的ADC也显示出巨大的潜力,如ARX788、PF-06804103、XMT-1522和MEDI4276等,这些ADC也正在进行临床试验,以评估胃癌患者的剂量和组合模式。
EGFR和HER3
MRG003是中国首个测试的EGFR靶向ADC,目前正在参与一项II期临床研究(NCT05188209),评估其治疗晚期胃癌的疗效和安全性。EV20/NMS-P945在涉及猴子的药代动力学和毒理学研究中显示出良好的半衰期和稳定性。此外,它在体外的各种肿瘤细胞系中表现出靶向依赖性细胞毒性活性,包括胰腺癌、前列腺癌和胃癌。AMT-562在源自胃癌患者的低HER3表达细胞系和患者来源的肿瘤异种移植物(PDX)模型中产生强烈而持久的抗肿瘤反应。BL-B01D1,一种靶向EGFR和HER3双特异性抗体偶联形成的新型ADC,正在与SI-B003一起试验,用于治疗胃肠道肿瘤,包括胃癌(NCT06008054)。
CLDN18.2
CLDN18.2是一种参与细胞旁紧密连接结构的重要膜蛋白,在正常生理条件下仅在胃黏膜的分化上皮细胞中表达。该蛋白在近60%的胃癌患者中持续稳定表达。2021年3月,CMG901(AZD0901)被FDA批准用于针对晚期实体瘤(胃癌和胰腺癌)的I期临床研究(NCT04805307),在89名患者中实现了33%的客观缓解率(ORR)和70%的疾病控制率(DCR)。另一个靶向Claudin18.2的ADC EO-3021(SYSA1801)在17名胃癌患者(NCT05009966)中显示出疗效,ORR为47.1%,DCR为64.7%。
此外,其他ADC正处于早期研究阶段,如TORL-2-307和LM-302,它们正在研究CLDN18.2阳性晚期胃肠道癌症患者的临床疗效,无论是作为单一药物(NCT05156866)还是与toripalimab联合使用(NCT05934331)。SOT102(NCT05525286)和CPO102(NCT05043987)已在胃癌和胃食管交界处癌患者中显示出初步疗效。
GCC
GCC属于受体鸟苷酸环化酶家族的成员,在胃肠道的液体和离子稳态中起着关键作用,在原发性和转移性胃肠道癌症中高表达。其表达水平在结直肠癌中达到约95%,在胰腺癌、胃癌和食管癌中达到60-70%。
在评估TAK-264(NCT01577758)的一项人类I期研究中,在胃癌、胃食管癌和胰腺癌中观察到了初步临床疗效。然而,随后的II期研究(NCT02202759)显示,使用TAK-264治疗的一小部分患者的临床益处有限。尽管靶向GCC的ADC尚未达到最佳治疗效果,但由于GCC在胃癌中的高表达,它们继续显示出治疗晚期胃癌的巨大潜力。
TROP2
TROP2在多种肿瘤中高表达,并可促进肿瘤细胞增殖、侵袭、转移和扩散。TROP2的高表达通常与生存期缩短和预后不良有关。
IMMU-132(sacituzumab govitecan)和SKB264都由可切割的连接子和拓扑异构酶I抑制剂组成。IMMU-132在胃癌的活性已在I/II期临床试验(NCT01631552)中报道。一项正在进行的研究(NCT04152499)评估了SKB264作为单一疗法,可能使局部晚期不可切除或转移性实体瘤对标准疗法产生耐药性的患者受益,包括胃腺癌和胃食管交界处腺癌。此外,DS-1062在几种表达TROP2的异种移植物模型中显示出抗肿瘤作用,包括NCI-N87模型。其在晚期/转移性胃癌患者中的试验(NCT05489211)正在进行中。
SLC44A4
SLC44A4通常在分泌上皮细胞的顶面上表达,现已被确定为大多数胰腺癌和胃癌中的新型细胞表面靶标。靶向SLC44A4的ADC药物ASG-5ME的临床研究(NCT01166490)显示,15名胃癌患者接受1.2 mg/kg的最大耐受剂量, DCR为47%。
ADC胃癌的联合治疗
联合治疗现在是肿瘤学临床前和临床研究的核心焦点。将ADC与各种疗法相结合,有利于改善实体瘤患者的预后。
ADC联合单克隆抗体治疗
几项正在进行的临床试验表明,ADC与mAbs联合治疗可提高各种类型胃癌的疗效。一项纳入30名晚期胃癌患者的试验(CTR20639)表明,与曲妥珠单抗单药治疗相比,ARX788联合治疗可显著延长患者的PFS和OS分别达4.1个月和10.7个月。在另一项临床试验(NCT04014075)中,证明DS-8201a可以治疗接受曲妥珠单抗治疗的晚期胃癌患者,从而导致更高的ORR和更长的OS。在联合治疗取得有希望的结果后,DESTINY-Gastric04研究(NCT04704934)目前正在评估在接受曲妥珠单抗治疗后,将T-DXd或ramucirumab和紫杉醇(Ram+PTX)联合治疗HER2阳性的胃癌或胃食管交界腺癌患者的疗效和安全性。
ADC联合免疫疗法
目前,阻断免疫检查点抑制剂已成为增强癌症患者抗肿瘤反应的一种有前景的方法。研究表明,ADC有效载荷直接诱导树突细胞活化和成熟,引发免疫原性细胞死亡。此外,ADC结构内的单克隆抗体可以上调PD-1/PD-L1的表达,增强免疫细胞浸润,促进树突状细胞的抗原呈递,最终提高PD-1/PD-L1抑制剂的疗效。
在一项涉及HER2表达的局部晚期或转移性实体瘤患者的试验中,RC48与JS001(PD-1抗体)联合使用(NCT04280341)。本试验报告胃癌组患者的ORR为43%,DCR为75%,反应持续时间为5.1个月,PFS为6.2个月,mOS为16.8个月。此外,T-DXd已被证明可以增加肿瘤浸润CD8+T细胞的数量,并增强肿瘤细胞中PD-L1和MHC-I的表达。该药物目前正在胃癌患者中单独或与durvalumab(一种PD-L1抗体)联合使用,以评估其安全性、耐受性、药代动力学、免疫原性和初步抗肿瘤疗效(NCT04379596)。
ADC联合其它药物
对于HER2阳性的晚期胃癌,抗HER2靶向治疗和化疗的联合治疗是标准的一线治疗,而基于ADC的联合治疗目前正在积极研究中。在RC48-C008研究(NCT03556345)中,RC48被用于先前接受化疗的局部晚期或转移性胃癌患者,从而形成了联合治疗方法。研究结果表明,ORR为24.8%,PFS为4.1个月,mOS为7.9个月。
药物的选择会影响ADC与靶向表面抗原的结合。例如,pyrotinib显著诱导HER2受体的内化,增强癌症细胞对T-Dxd的摄取。洛伐他汀是一种降胆固醇药物,可暂时增加细胞表面HER2水平,增强HER2-ADC结合和内化。WEE1是一种调节肿瘤细胞分裂的蛋白质,强效WEE1抑制剂adavosterib和T-DXd的组合显著增加了抗肿瘤活性,这是因为Wee1激酶抑制剂在G2期阻滞期间绕过了细胞修复复制应激诱导的损伤的能力,导致DNA损伤积累和随后的有丝分裂破坏。
小结
ADC在胃癌治疗中备受期待,目前上市的DS-8201a、RC48和IMMU-132已成为晚期胃癌患者的二线和后线治疗选择。然而,很少有胃癌患者存活下来接受二线或二线治疗,因此,有必要进一步探索新的ADC药物和联合疗法作为一线和二线治疗。
此外,确定最佳的联合治疗和克服耐药性的方法应在未来的研究中加以解决。偶联技术和新型连接子或有效载荷的增强可以为下一代ADC的胃癌治疗提供思路。鉴于肿瘤环境的复杂性,双特异性ADC可能潜在地促进双重靶点的协同内吞作用,并提高有效载荷进入癌细胞的效率,这也有利于克服耐药性。未来ADC在胃癌和其它实体瘤治疗中应有更广阔的发展前景。
参考文献:
1.Antibody-drug conjugates in gastric cancer: from molecular landscape to clinical strategies. Gastric Cancer.2024 Jul 4.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)