首页 > 医疗资讯/ 正文
静脉血栓栓塞症(VTE)是指深静脉血栓形成的一种常见疾病。VTE的发病率高出4 ~ 12倍,已被广泛认为是所有癌症患者中排名第一的致死性并发症,占癌症总死亡人数的近9%。虽然血栓的分离和移动可能会导致猝死等严重后果,但大多数VTE病例无症状,容易被忽视。

基于此,中科院理化技术研究所王树涛研究员、孟靖昕研究员和首都医科大学张澍田教授合作提出了一种由TiO2纳米花(TiNFs)组成的快速、易操作、高特异性和高灵敏度的促凝血细胞外囊泡条形码(PEVB)检测方法,用于可视化评估癌症患者的VTE风险。通过TiO2-磷脂分子相互作用和TiNFs与EV之间拓扑相互作用的协同作用,TiNFs表现出快速的无标记EV捕获能力。在普通血浆样本中,通过将基于TiNFs的EV捕获和原位EV促凝能力检测与机器学习辅助的临床数据分析相结合,PEVB检测可以评估潜在的VTE风险。通过对167例癌症患者的筛查,我们证明了PEVB检测在VTE风险评估中的可行性,以及高特异性(97.1%)和高敏感性(96.8%),完全超过了非特异性和后循环的传统VTE检测。
总之,我们提出了一个TiNFs平台,可以高度准确和及时地诊断癌症患者的VTE。相关工作以“Machine-Learning-Assisted Procoagulant Extracellular Vesicle Barcode Assay toward High-Performance Evaluation of ThrombosisInduced Death Risk in Cancer Patients”发表在《ACS NANO》。
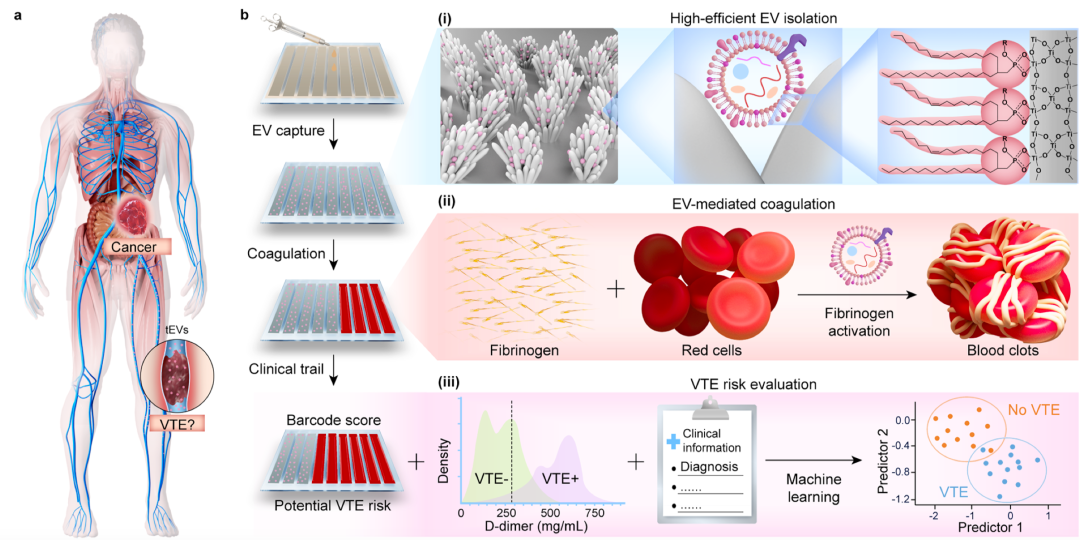
示意图1. 准确评价静脉血栓栓塞(VTE)的PEVB法原理图设计
精确评价VTE的PEVB法设计
为了准确评估促凝血EVs引起的癌症患者VTE风险升高,并防止不明确的诊断,我们开发了一种基于二氧化钛纳米花(TiNFs)的PEVB检测(示意图1)。PEVB检测实现了三个关键过程:
(i)基于TiNFs的EV快速捕获;
(ii)易于操作的通过计数阳性条形码数获得条形码评分的原位EV促凝能力测试;
(iii)机器学习辅助临床数据分析,用于准确的VTE风险评估。
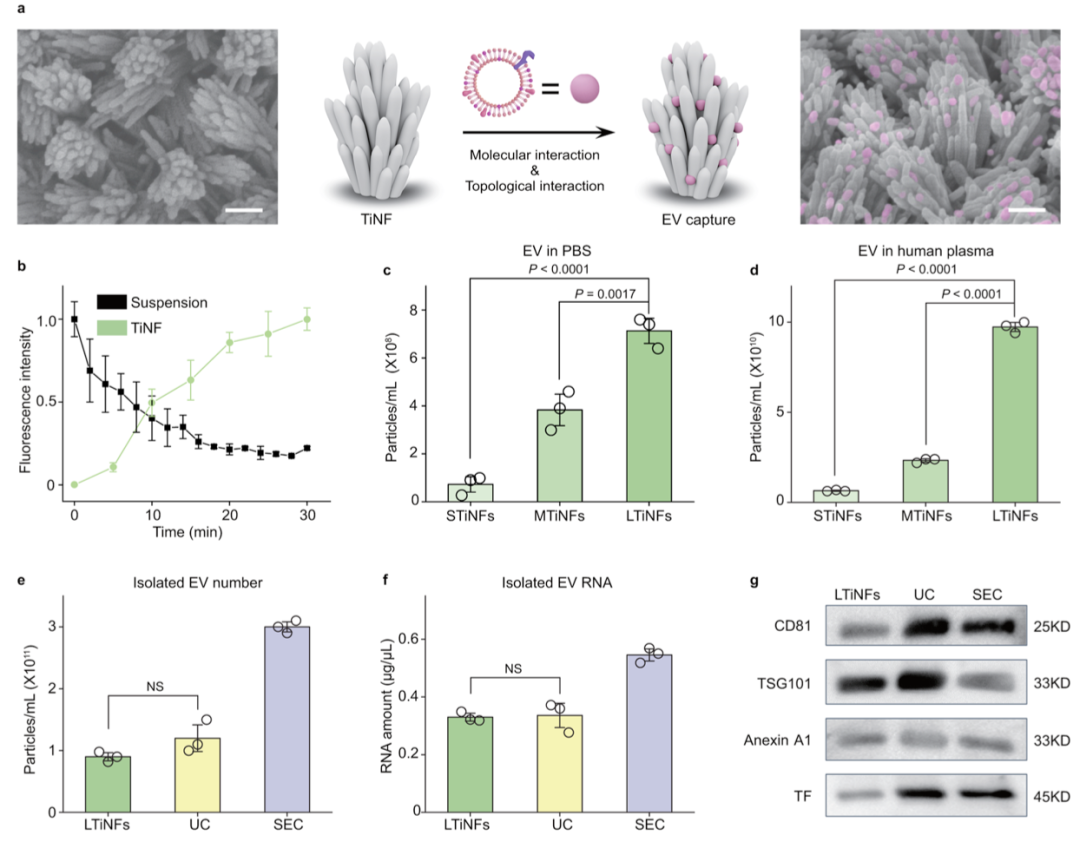
图1. TiNFs上的EV捕获能力
TiNFs上的快速EV捕获
研究者通过将500 μL EV悬浮液滴到铺有TiNFs的55 mm × 25 mm玻璃载玻片上,验证了基于TiNFs的无标记EV捕获的可行性。如图1a所示,通过TiO2 -磷脂相互作用和拓扑相互作用,大量的EVs(用粉红色标出)被捕获到尖端之间的陷阱和相邻的TiNFs纳米金属的间隙上。应用20个FAM标记的人工模型EV 21,优化EV捕获的孵育时间。在TiNFs上捕获的EVs的荧光强度最初随着孵育时间的增加而增加,在约20分钟后达到平台期,进一步确定捕获时间为30分钟(图1b)。

图2. 肿瘤来源的EVs促凝血能力的评估
肿瘤来源的EVs促凝血能力的评估
为了评估TEV促进血凝的效果,我们在铺有LTiNFs的10 mm × 10 mm玻片上测定了EV的促凝能力。简单地说,将50 μL HCT-15细胞衍生的tEV悬液在LTiNFs上孵育30 min,然后用PBS洗涤。随后,将20 μL模拟血和20 μL凝血酶稀释液(人工凝血指示剂)的混合物滴至这些LTiNFs上,触发血凝反应,从而使血细胞缠结凝固。我们绘制了一系列凝血酶浓度(1.8 ~ 6.6 ng/ mL)和tEV浓度(0 ~ 2.1 × 10 7 EVs/mL)的凝血水平,从而生成相图(图2a)。热图由三次独立试验的平均灰度值组成,表明随着tEV浓度的升高,促凝能力升高,从而随着凝血酶阈值的降低,促进血液凝固(图2b)。
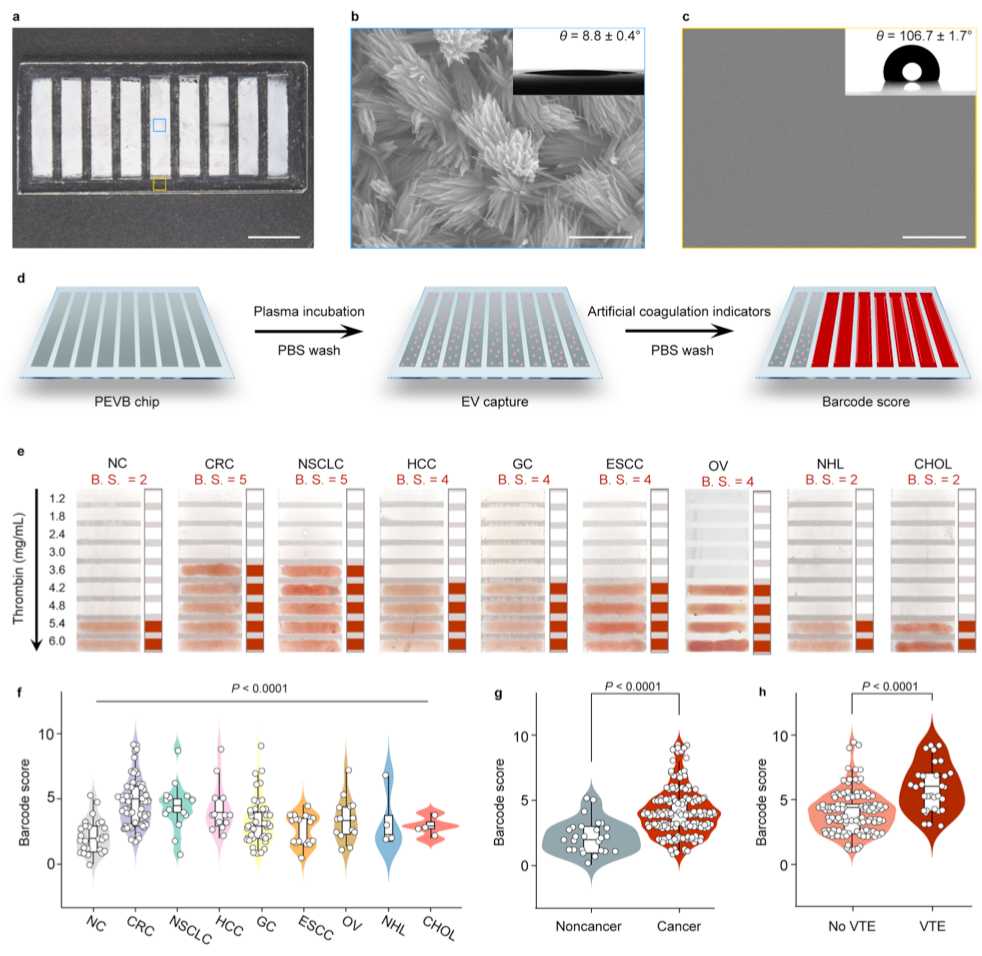
图3. 肿瘤患者样本EV促凝能力的评价
癌症患者EV促凝能力的评估
利用广泛报道的具有直接观察和可视化结果的条形码系统,研究者通过在疏水亲水性图案玻璃衬底上生长LTiNFs来制备PEVB芯片 (图3a)。PEVB芯片由用于EV捕获的亲水性ltinf的条形码区域(白色,20.0 × 4.0 mm)和疏水性区间(1.75 mm)组成,以防止相邻条形码的干扰(图3b, 3c)。多重EV促凝能力试验:将患者血浆20 μL加载到每个条形码区域捕获EV,孵育30 min后加入人工凝血指标(血液悬液、血浆标准品、凝血酶的混合物,9次滴定从6.0 ng/mL降至1.2 ng/mL,间隔0.6 ng/mL)。
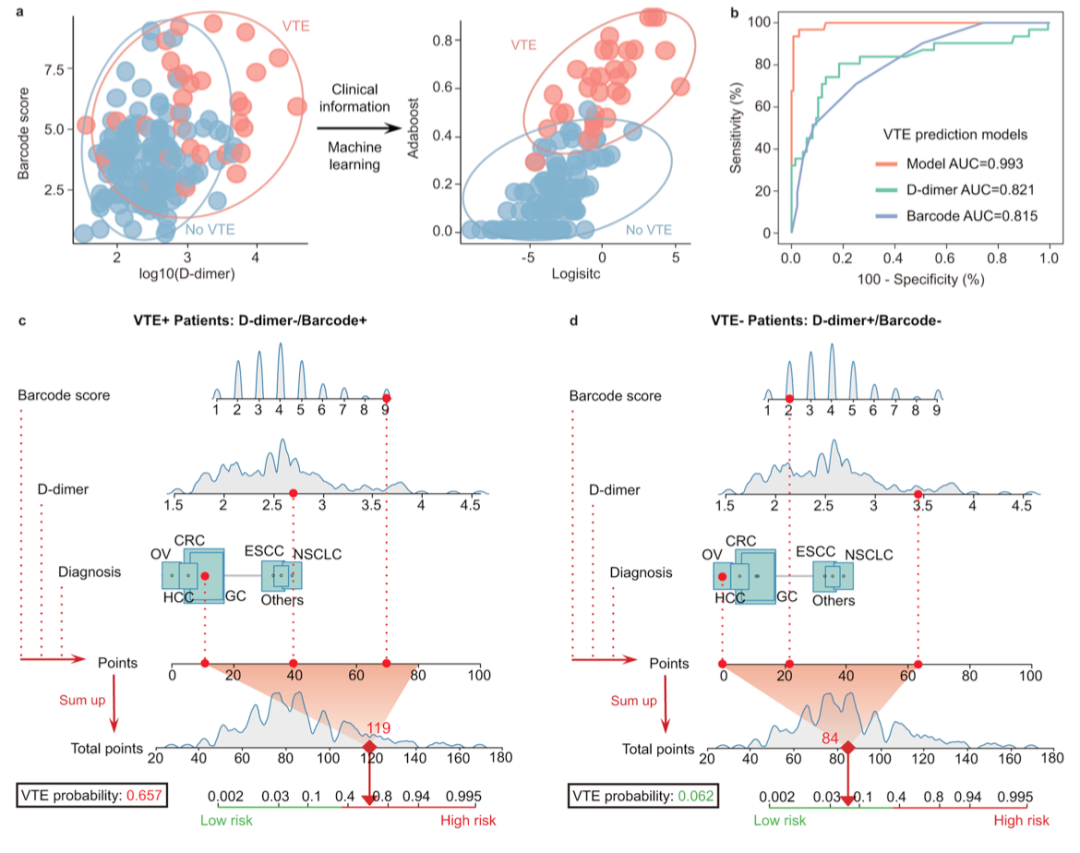
图4. 采用机器学习辅助VTE风险评估
机器学习辅助的VTE风险评估
与条形码评分和d-二聚体水平的简单组合相比,集成了条形码评分、d -二聚体和诊断的机器学习模型(logistic、LASSO、SVM、Adaboost和随机森林)均可明显区分VTE患者和非VTE患者(图4a)。在所有算法中,Adaboost获得了最好的AUC值0.993,同时表现出高特异性(97.1%)、高准确性(97.0%)和高敏感性(96.8%)(图4b)。
相比之下,使用250 ng/mL的临床临界值时,只有d -二聚体表现出低特异性(44.8%)、低准确性(53.2%)和高灵敏度(90.3%),而使用通过最大准确度值确定的临界值5时,PEVB检测法表现出低特异性(75.0%)、低准确性(74.3%)和低灵敏度(70.9%)。这些结果表明,我们可以通过一个简单可行的平台实现高性能的VTE评估。
【小结】
PEVB检测可快速、直观地反映肿瘤患者发生VTE的风险,无需经过特殊培训的普通技术人员即可操作。我们相信,该方法具有良好的性能,可以很容易地应用于临床实践,作为一种评估VTE风险的无创、方便、常规、高度特异和抢先的方法,尤其是对于低收入和中等收入国家。
原文链接:
https://pubs.acs.org/doi/10.1021/acsnano.3c04615.
猜你喜欢
- 健康性生活男女必须遵守的规则
- 法国专家提出母乳喂养新理由:让孩子长得更好看
- 一块榴莲肉的热量有多高 一天吃一块榴莲会生胖吗
- Nature:为什么你能快速上手新事物?原来是纹状体pDMSt帮你搞定了“逐次试验更新”
- JGH: 住院和门诊急性下消化道出血患者的差异
- 常见的10种补肾壮阳中药材盘点
- J Clin Oncol | 未达到主要终点-瑞拉可兰(Relacorilant) + Nab-紫杉醇联合治疗复发性铂类耐药卵巢癌患者:一项三臂、随机、对照、开放标签的 II 期研究
- Nat Commun:中科大瞿昆/郭闯团队对染色体外环状DNA算法性能进行系统评估
- BMC Musculoskelet Disord:应用柔性铰刀克服重度肥胖股骨粗隆间骨折患者股骨近端钉入点误差
- Eur Urol: Pembrolizumab联合阿西替尼与舒尼替尼作为晚期肾细胞癌的一线治疗方案:3期 KEYNOTE-426 研究的43个月随访结果
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)