首页 > 医疗资讯/ 正文
目前,50-60%的癌症患者采用放射治疗(Radiation Therapy,RT),尽管技术和治疗方法不断改进,但很多患者由于耐药或转移而导致治疗失败。放射增敏治疗策略一般集中在抑制DNA修复或增加DNA损伤上,其中免疫环境对治愈性至关重要。临床前数据表明,电离辐射(Ionizing Radiation,IR)单独或联合免疫检查点阻断具有免疫刺激作用。基于此,越来越多的临床试验启动免疫检查点阻断与IR联合疗法。然而,目前治疗效果有限,放疗联合免疫检查点疗法的协同作用机制及两者之间的相互关系仍需进一步探索。
研究表明,髓系抑制细胞(MDSC)已成为抗肿瘤免疫反应的关键负调节因子,且肿瘤浸润的MDSC可能是放疗联合免疫检查点疗法产生抵抗的原因。基于此,目前有一些临床试验旨在通过不同的方式调节MDSC以增强免疫治疗,但仍没有成功案例。
N6-甲基腺苷(m6A)是真核生物中最常见的mRNA的修饰,主要调控mRNA的稳定性和翻译效率。m6A主要由RNA甲基转移酶(writer)—METTL3/METTL14、RNA去甲基化酶(eraser)—FTO和ALKBH5动态调控,随后由“阅读子”(reader)—YTHDF1/2/3和YTHDC1/2识别调节RNA代谢。研究表明,YTHDF2参与调控多种生物学过程,包括细胞周期进程,应激反应等,并与多种肿瘤生长有关。然而,YTHDF2在免疫细胞中的调控作用,尤其是在放疗和免疫治疗中的作用尚未被深入探讨。
2023年5月25日,芝加哥大学 Ralph Weichselbaum 教授、何川教授、Hua Laura Liang 教授与中国科学院上海药物研究所罗成研究员等在 Cancer Cell 期刊发表了题为:YTHDF2 inhibition potentiates radiotherapy anti-tumor efficacy 的研究论文。
该研究发现,YTHDF2可作为放疗和放疗/免疫联合疗法的潜在靶点,提出了通过抑制YTHDF2来增强临床放射治疗效果的新策略。

该研究发现,电离辐射(IR)在小鼠模型和人体内均可诱导免疫抑制性MDSC扩增和YTHDF2表达。IR介导放疗后,表达YTHDF2的MDSC群体增加,这与放疗后的转移进展有关。因此,研究人员猜想YTHDF2的增加是影响放疗效果的原因。
于是,研究人员通过构建Ythdf2敲除小鼠模型,发现IR后,Ythdf2的缺失可改变MDSC分化,抑制MDSC向肿瘤转运,并减弱其抑制功能,增强了抗肿瘤免疫,从而增强了局部肿瘤IR的功效。进一步,研究人员发现,IR诱导的YTHDF2表达上调主要依赖于NF-κB/RELA信号通路。反过来,上调的YTHDF2通过直接结合并降解编码NF-κB信号负调控因子(Adrb2、Metrnl和Smpdl3b)的转录本,导致NF-κB活化,从而形成 IR-YTHDF2-NF-κB回路。这些都表明,可以通过抑制YTHDF2来提高抗肿瘤免疫和放疗效果,其有望成为临床放射治疗的新策略。
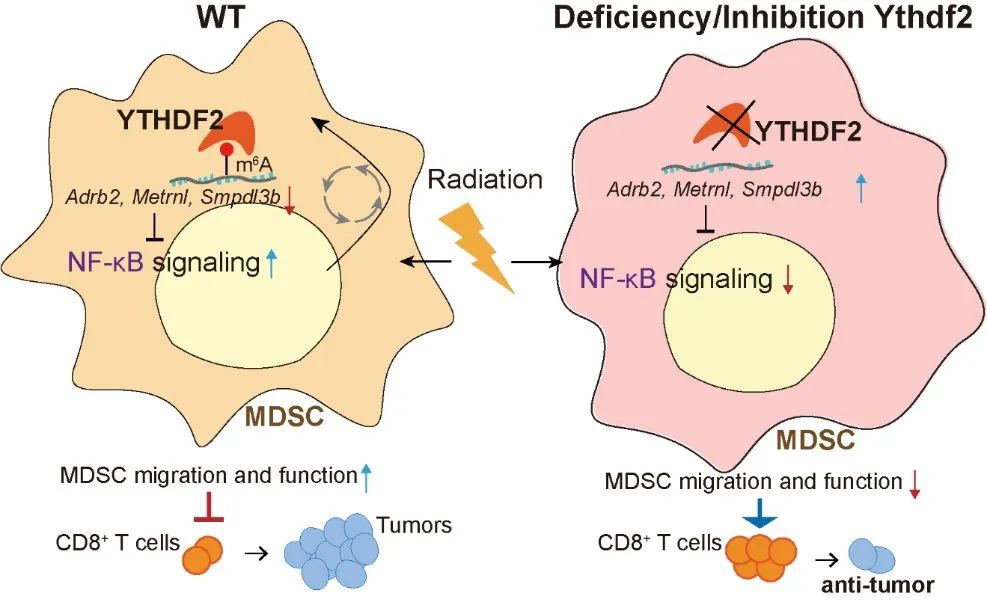
抑制YTHDF2提高放疗抗肿瘤效果的作用机制
为了进一步证明YTHDF2是潜在的改善放疗和RT/免疫联合疗法的靶点,研究人员通过靶向YTHDF2开展化学干预研究。基于建立的化合物高通量筛选方法,开展了小分子抑制剂的筛选并获得了YTHDF2的活性化合物DC-Y13。通过结构改造获得了化合物DC-Y13-27,其可以在体外直接结YTHDF2蛋白并抑制其与m6A-RNA的结合。此外,DC-Y13-27在小鼠上与敲除YTHDF2类似,不仅可有效提高的IR疗效,而且提高了IR与PD-L1抗体联合治疗的抗肿瘤效果。抑制YTHDF2克服了MDSC诱导的免疫抑制,不仅可以改善局部肿瘤治疗效果,还可以抑制肿瘤转移。
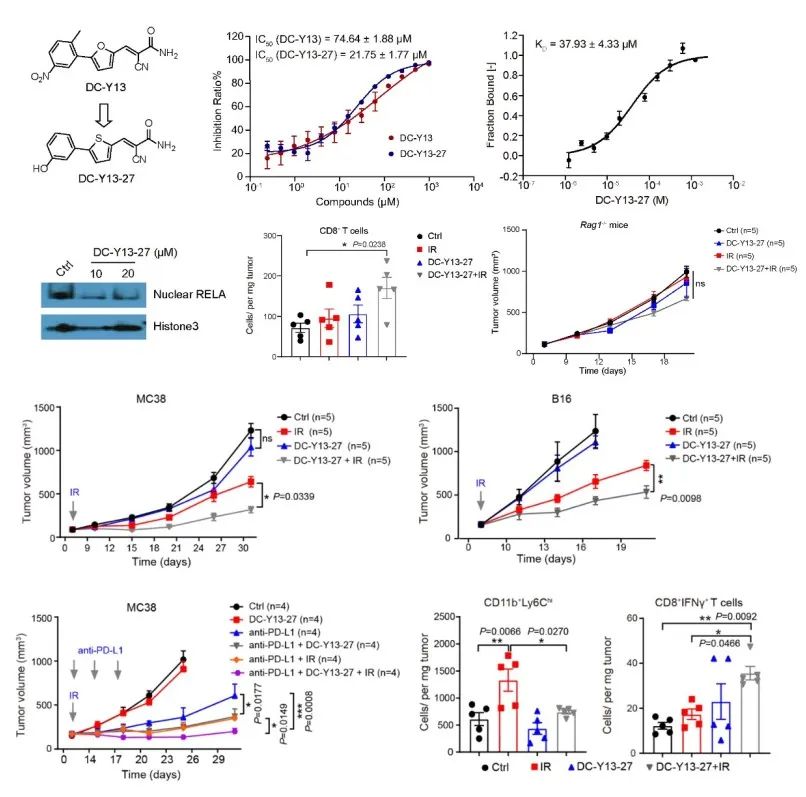
YTHDF2抑制剂DC-Y13-27的发现及其对放疗和免疫治疗疗效的提高作用
综上所述,该研究通过结合基因干预和化学干预手段,揭示了m6A“阅读子”YTHDF2的抑制在改善放疗和放疗免疫检查点联合治疗效果的调控机制,并为相关临床治疗提供了新靶标。该研究获得的YTHDF2小分子抑制剂,不仅为YTHDF2的功能研究提供探针工具,同时也为靶向YTHDF2的药物开发提供先导结构,促进其在临床研究中的应用转化。
论文链接:https://www.cell.com/cancer-cell/fulltext/S1535-6108(23)00163-0
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)