首页 > 医疗资讯/ 正文
过继性T细胞转移(ACT)是肿瘤治疗中最有前途的免疫治疗方法之一。目前有四种成熟的ACT技术,包括自体肿瘤浸润淋巴细胞(TIL)治疗、抗原特异性内源性T细胞治疗(ETC)、T细胞受体工程T细胞治疗(TCR-T)和嵌合抗原受体T细胞治疗(CAR-T)。TIL和ETC疗法分别依赖于从肿瘤或外周血中分离和体外扩增T细胞,而TCR-T和CAR-T疗法利用T淋巴细胞的基因修饰赋予它们肿瘤抗原特异性。
TCR-T细胞疗法最初主要针对共同的肿瘤相关肽靶点,随着最近的技术发展,靶向来自肿瘤体细胞突变的新抗原已成为可能,这代表了一种高度个性化的治疗。TCR-T疗法已在世界各地的许多临床前研究和临床试验中被用于实体瘤的临床疗效测试。然而,TCR-T治疗实体瘤的疗效依然面临许多挑战,包括低TCR亲和力、靶向毒性和导致肿瘤逃逸的靶抗原丢失。
目前,一些新的技术和工具正在应用于TCR-T,有助于提高TCR-T治疗的疗效和安全性,TCR-T细胞治疗正展现出抗肿瘤治疗的巨大潜力。
CAR-T与TCR-T的比较
TCR分子属于免疫球蛋白的一个超家族,由两个共价结合的多态性亚单位组成,每个亚单位都是抗原特异性的,它们至少与四种不同类型的信号转导链有关。为了激活T细胞,TCR和主要组织相容性复合体(MHC)之间必须存在相互作用。
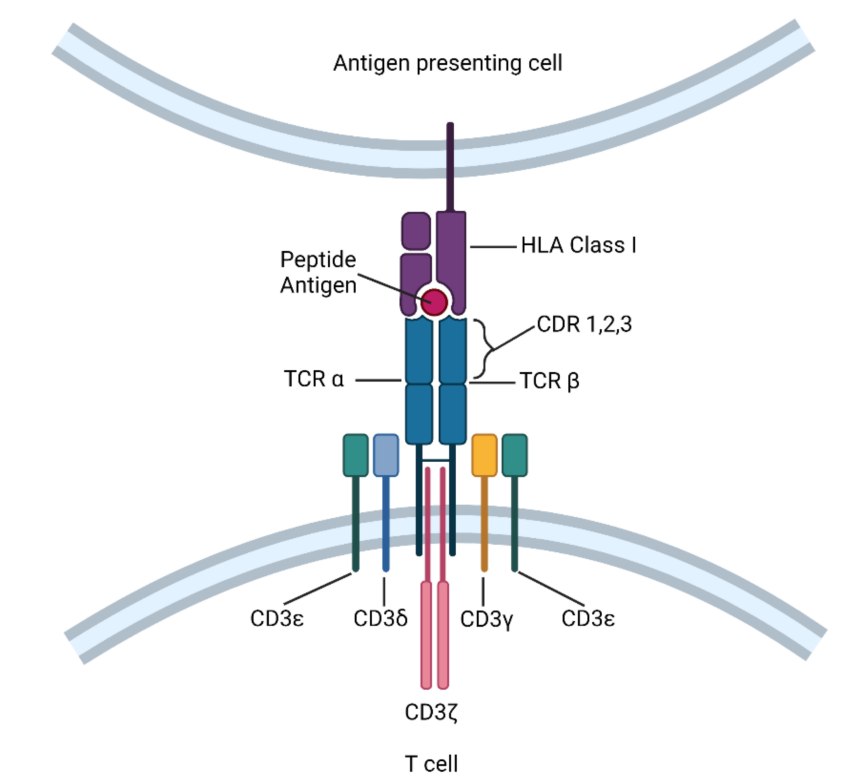
TCRs与pMHC(peptide-MHC)相互作用的强弱决定了未成熟胸腺细胞的命运,对幼稚T细胞的存活至关重要。因此,TCR-T免疫治疗技术通过与MHC特别是Ⅱ类分子的有效相互作用激活宿主的免疫系统。TCR-T细胞可以识别细胞内的肿瘤特异性抗原,而CAR-T细胞主要识别肿瘤表面的特异性抗原。这使得TCR-T细胞在肿瘤治疗中更有效。
CAR包含肿瘤抗原靶向的单链抗体、跨膜结构域和CD3ζ的胞内激活结构域。通过这种方式,工程化的CAR能够识别特定的肿瘤相关抗原,CAR能够在不经过MHC处理的情况下结合未经处理的肿瘤表面抗原。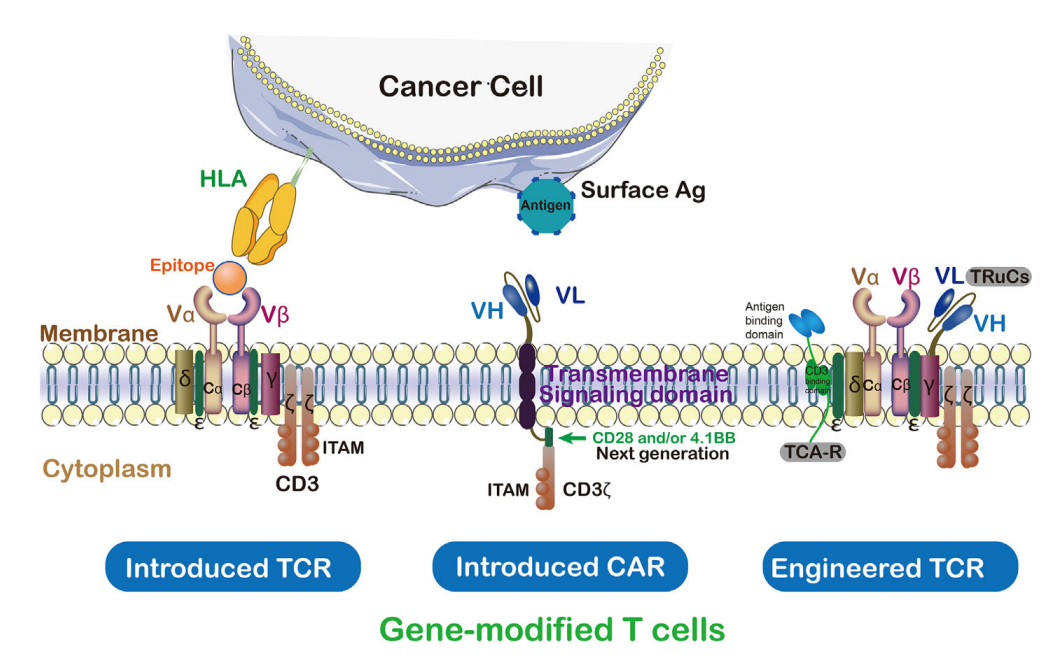
相反,TCR是与MHC抗原复合物结合的α/β异二聚体。与TCR相比,CARs识别肿瘤抗原具有某些缺点,如肿瘤外毒性。与CARs相比,TCRs在基于T细胞的治疗中具有一些结构性优势,例如其受体结构中有更多的亚单位(10:1),免疫受体基于酪氨酸的激活基序(ITAMs)更多(10:3),对抗原的依赖性更小(1:100),以及更多的共刺激受体(CD3,CD4,CD28等等)。具有低MHC亲和力范围(104-106M-1)的TCR就可以有效的激活T细胞,相反,CARs需要更高的亲和力范围(106-109M-1)。
因此,CAR介导的细胞毒性依赖于更高密度的细胞表面抗原。此外,T细胞/抗原相互作用在免疫突触(IS)结构中启动,其中TCR呈现具有外周LFA-1粘附的环状区域,而CAR呈现无环状区域的弥散LFA-1分布。因此,TCR-IS比CAR-IS发出的信令速度慢但持续时间长。同时,CAR-T细胞呈现出更快的杀伤功能,并向下一个肿瘤靶点迁移(连环杀伤),这与TCR-T细胞延长信号传导和延长杀伤时间形成鲜明对比。
TCR-T细胞治疗的临床现状
截止2021年8月9日,在ClinicalTrials上共有175项使用TCR-T疗法的研究正在进行中,其中71项是针对特定TAA或新抗原的特异性TCR,有32项研究已经完成。NY-ESO-1是最常见的靶向抗原,在多种癌症中均有表达,包括骨髓瘤、黑色素瘤等。其他肿瘤睾丸相关抗原,如PRAME和MAGE蛋白,以及黑色素瘤分化抗原MART-1和gp100,以及最近的癌症驱动因子,如WT1、KRAS和TP53,也是流行的TCR-T靶点。
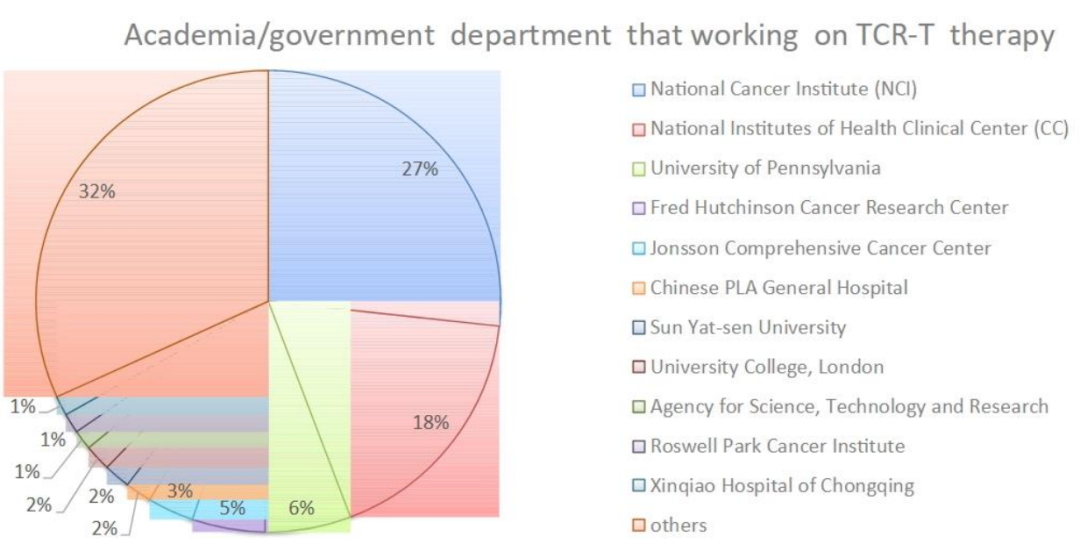
共有83名赞助者/合作者发起或参与TCR-T细胞治疗的研究,包括美国国家卫生研究院(NIH)、政府组织、行业和大学/学术机构。目前,美国国家癌症研究所(NCI)共支持了53个TCR-T项目,占到了所有正在进行项目的20%。
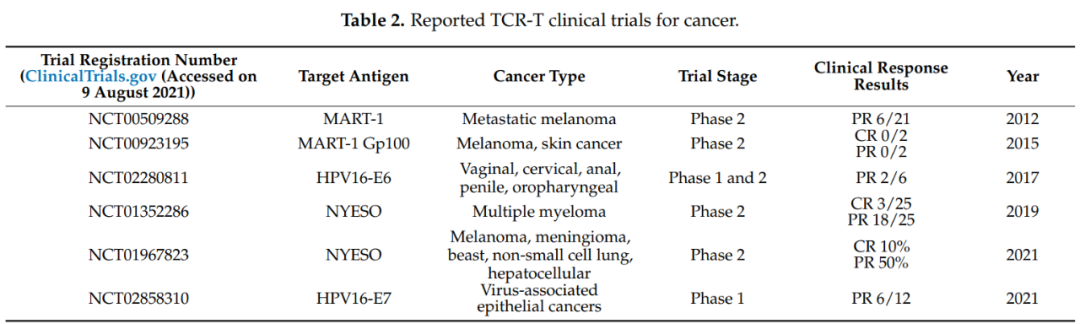
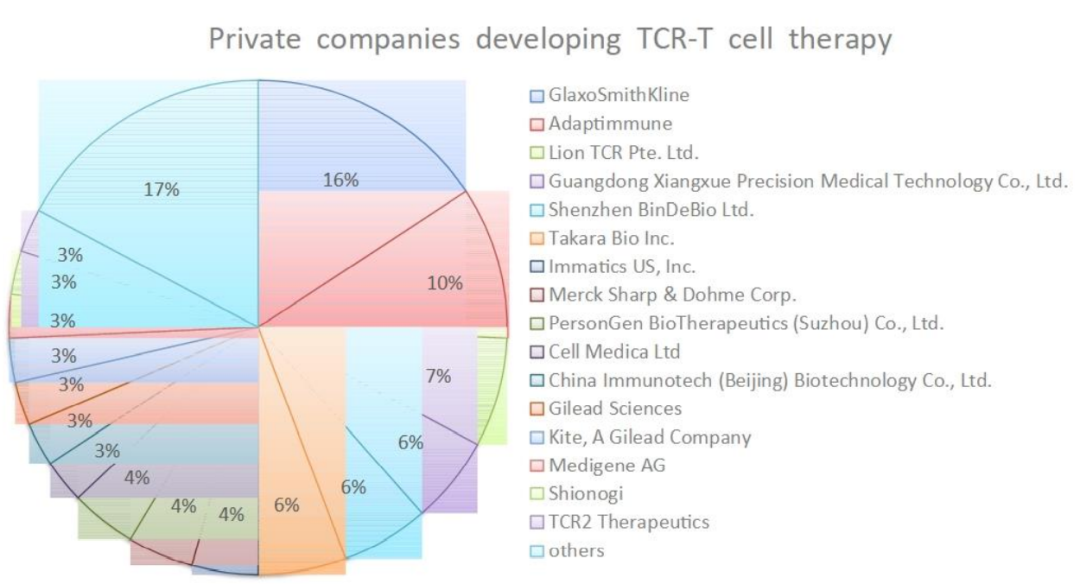
在开发TCR-T疗法的29家制药公司中,葛兰素史克和Adaptimunime发起了最多的临床试验,分别为11项和7项。最近,报道了一项针对人乳头瘤病毒(HPV)-16 E7蛋白的TCR-T细胞治疗转移性人乳头瘤病毒相关上皮癌的1期临床试验(NCT02858310)。在这项研究中,12名接受治疗的患者中有6名出现了客观的临床反应,观察到了稳健的肿瘤消退。这是TCR-T细胞疗法的一个里程碑式的临床试验,证明靶向病毒抗原对病毒相关癌症患者具有良好的临床效果。其他被探索为TCR靶点的病毒抗原包括HPV-E6蛋白、来自EB病毒(EBV)的抗原和人类内源性逆转录病毒(HERV)靶点,如HERV-E。
靶向TAAs 的MART-1和NY-ESO-1 TCR-T疗法在晚期黑色素瘤、骨髓瘤和非小细胞肺癌中也显示出临床疗效。完成的TCR-T临床试验的总有效率(ORR)在0~60%之间。值得注意的是,这些TCR-T临床试验中的大多数都只入组了少量患者(2至25名),因此ORR在统计上可能不太准确。因此,需要更大规模的II期和III期临床试验来确认这些TCR-T疗法的实际临床疗效。
TCR-T细胞治疗的挑战和潜在解决方案
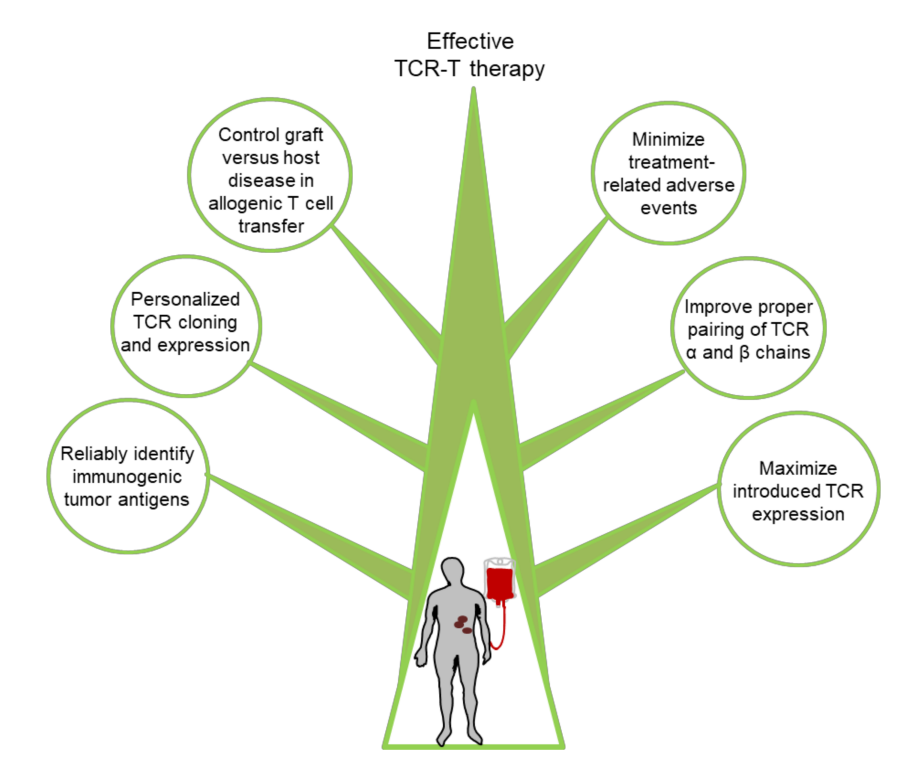
尽管基于TCR-T细胞的免疫疗法已在大部分接受治疗的患者中显示出一定的临床疗效,但在许多领域仍然面临着诸多挑战。这些挑战包括:(1)靶向正常组织引起的免疫毒性;(2)工程化T细胞中TCR表达不足或短暂表达;(3)T细胞耗竭和功能障碍;(4)肿瘤免疫逃逸,以及(5)大多数癌症患者缺乏有效的肿瘤特异性抗原作为靶点。克服这些挑战将是未来取得更大临床成功的关键。
新靶标的发现
目前,用于TCR-T的有效和安全免疫治疗的肽抗原靶点非常有限。目前使用的大多数靶点是TAA,尽管在肿瘤组织中上调,但在正常组织中仍保持低水平的表达,这可能导致自身免疫毒性。因此,新抗原似乎是TCR-T癌症治疗最安全的靶点。然而,在TCR-T临床开发新抗原的主要挑战包括:(1)新抗原形成突变在很大程度上是个体化的,并且在癌症患者之间存在差异,因此难以开发出广泛应用的免疫治疗产品;(2)新抗原在肿瘤组织中的表达常常是异质性的。
尽管如此,近年来的报告强调了肿瘤细胞广泛共享的免疫原性新抗原的出现,包括突变的KRAS和TP53。许多其他研究也证明了可用于产生潜在治疗性肿瘤特异性TCR的共享新抗原的免疫原性。随着下一代测序技术的发展,特别是单细胞DNA测序、转录组测序和成熟的体外验证方法,以个性化新抗原为靶点的TCR-T免疫治疗可能在未来几年成为一种流行的癌症治疗方法。此外,新出现的TAA类别,如癌胚抗原,也可能构成未来TCR-T发展的可行靶标。
最大化治疗性TCR表达
转基因α和β链的正确配对是阻碍TCR-T细胞发展的主要挑战之一。由于每个转导的T细胞包括两条内源性TCR链和两条转化的TCR链,因此具有未知特异性的异二聚体可导致潜在的自身免疫后果。另一个相关问题是,不恰当的α/β链TCR配对将竞争CD3复合物,从而降低治疗性TCR的表面表达和信号转导。
有几种方法可对转导的TCR链进行适当配对,包括:(1)部分鼠源化TCR的恒定区;(2)添加半胱氨酸残基以促进引入TCR链的二硫键;(3)改变内源性TCR恒定区的二级结构;(4)向转导TCR的细胞内部分添加信号域;(5)将TCR-α/β链引入替代效应细胞或构建单链TCR。
增强治疗性TCR表达的方法包括:(1)TCR-α和TCR-β链转基因的密码子优化,以及(2)改变TCR-α/TCR-β载体配置以优化表达。
减少不良事件
通常,靶向非肿瘤毒性是TAA的主要关键障碍,这种风险促使研究人员更仔细地研究共同的新抗原。目前,多个癌基因热点突变正在被研究作为潜在的TCR靶点,如磷酸肌醇-3-激酶(PI3K)、KRAS和TP53。此外,通过带有自杀基因的基因工程化的TCR-T细胞是采用的一项重要安全措施。显然,发展可靠识别的个性化、高度特异性和免疫原性的肿瘤抗原靶点对于减少与TCR-T细胞治疗相关的不良事件至关重要。
异体T细胞的移植物抗宿主病
使用同种异体T细胞是一个非常有希望的方案,可以克服制造问题、患者相关免疫细胞缺陷和治疗延迟。为了使用同种异体T细胞,有必要控制由转导的同种反应性淋巴细胞引起的移植物抗宿主病以及宿主免疫系统对工程化淋巴细胞的排斥。
内源性TCR基因、HLA-I位点或CD52分子的缺失是避免TCR-T移植失败的策略之一,可通过多种方法实现,如基因编辑或使用siRNA。此外,多能干细胞技术也被认为是一种潜在的解决方案。
小结
TCR-T疗法是一种非常有前途的癌症免疫治疗方法,具有其它T细胞过继性疗法不可比拟的优势。然而,提高TCR-T免疫治疗的抗肿瘤疗效仍然有几个关键挑战,包括如何安全地增加治疗性TCR的亲和力,如何在患者群体中鉴定共有的肿瘤特异性抗原和TCR,以及如何调节TCR的表达并实现最佳功能。这些问题的解决将有助于充分发挥TCR-T细胞治疗的潜力,给肿瘤患者解除病痛带来希望。
参考文献:
1.Evolution of CD8+ T Cell Receptor(TCR) Engineered Therapies for the Treatment of Cancer. Cells. 2021 Sep;10(9): 2379.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)