首页 > 医疗资讯/ 正文
流感病毒是全球性的公共卫生问题,它不仅会导致季节性流感,还会引发偶发的大流行,给人类健康带来严重威胁。历史上多次流感大流行造成了数以百万计的死亡,例如1918年大流行就导致了约5000万人死亡。此外,季节性流感每年也会导致29万至65万人死亡。由于流感病毒的包膜蛋白具有高突变率,现有的疫苗无法有效预防新出现的病毒株。目前主流的抗流感药物主要针对病毒的包膜蛋白,但抗药性问题日益严重。近年来,虽然有新的抗病毒药物如玛巴洛沙韦获批,但耐药病毒株也迅速出现。因此,开发新的广谱流感疫苗和抗病毒药物迫在眉睫。
流感病毒属于正黏病毒科,是一种分节段的负义单链RNA病毒。其基因组包含7或8个RNA片段,每个片段编码至少一种病毒蛋白。病毒的核糖核蛋白复合物(RNP)由病毒基因组RNA片段、多个核蛋白(NP)亚基和聚合酶复合物组成,负责在宿主细胞中执行病毒基因组的转录和复制。与包膜蛋白相比,NP和聚合酶复合物在进化上更为保守,因此被认为是开发抗病毒药物的理想靶点。然而,由于RNP的结构复杂且具有高度柔性,其高分辨率结构分析一直是一个挑战。
美国宾夕法尼亚州立大学Yi-Wei Chang通过结合冷冻电镜单颗粒分析(SPA)和冷冻电子断层扫描(cryo-ET)技术,揭示了流感RNP的高分辨率结构,并提出了流感病毒复制过程中RNP如何维持其双螺旋结构的同时进行RNA合成的机制。此外,研究还通过虚拟筛选发现了针对RNP的潜在抗流感药物先导化合物。相关内容以“Molecular basis of influenza ribonucleoprotein complex assembly and processive RNA synthesis”为题发表在《Science》上。

【核心结果】
RNP结构解析:通过SPA技术,研究者们发现流感D病毒的RNP呈现出右手、反平行的双螺旋结构,NP亚基通过尾环连接,RNA被封装在双螺旋的小沟中。通过STA技术,研究者们进一步确认了这一结构,并观察到RNP在不同功能状态下呈现出多种不同的构象,表明双螺旋内部存在动态的链间运动。
聚合酶复合物的可视化:研究者们在RNP的预启动和延伸状态下可视化了聚合酶复合物,发现聚合酶始终与RNP的外表面相关联,支持了一种螺旋链滑动模型,即聚合酶沿着RNA模板进行RNA合成,同时保持RNP的整体双螺旋结构。
抗流感药物先导化合物的发现:通过虚拟筛选,研究者们针对NP的尾环结合界面识别出了一些先导化合物,这些化合物在细胞实验中有效抑制了流感病毒的复制。
【主要内容】
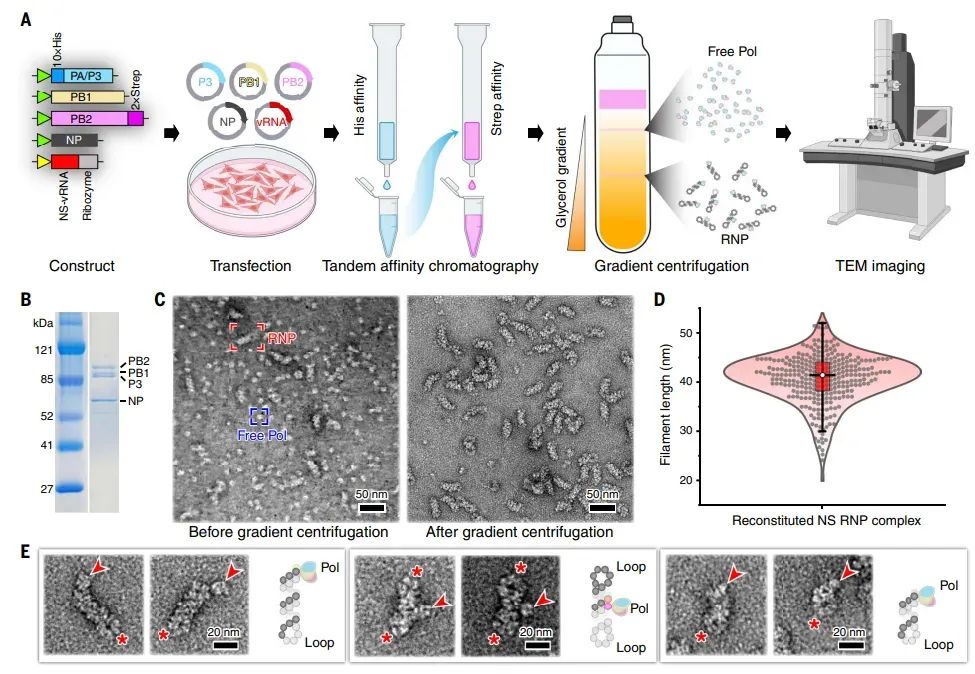
图1流感D病毒NS段RNP的体外重组与纯化
图中展示了流感D病毒NS段RNP的重组过程。通过共转染NP、聚合酶亚基和NS RNA片段到HEK293T细胞中,利用串联亲和纯化技术分离出完整的RNP复合物。重组的RNP呈现杆状结构,长度主要集中在35-45 nm,比长RNP更刚性。实验还证实了重组RNP的活性,检测到病毒RNA(vRNA)和互补RNA(cRNA),其中vRNA含量远高于cRNA,与病毒感染细胞中的情况类似。此外,观察到聚合酶在RNP复合物中的不同位置,表明其可能处于启动、终止或延伸状态。
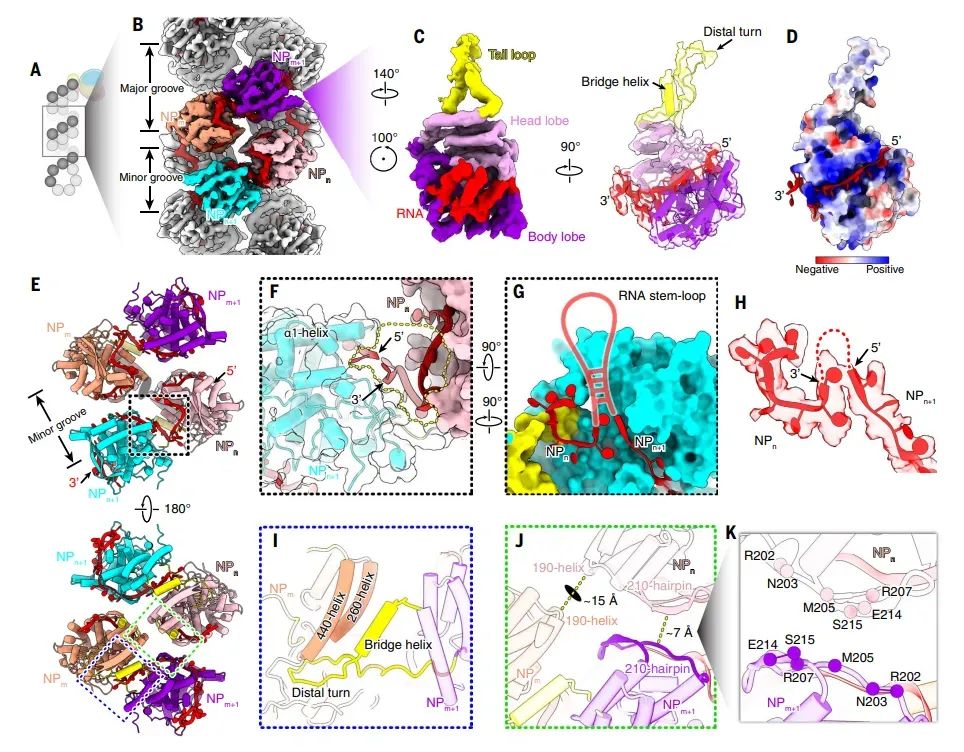
图2流感D病毒NS段RNP的双螺旋结构
通过冷冻电镜单颗粒分析(SPA)解析了流感D病毒NS段RNP的高分辨率结构。结果显示RNP为右手、反平行的双螺旋结构,NP亚基通过尾环连接,病毒RNA被封装在双螺旋的小沟中。每个NP亚基可容纳约20个核苷酸,RNA结合槽高度带正电荷,有利于RNA的结合。此外,还观察到NP亚基之间的开放口袋,可能允许RNA的二级结构伸出RNP。
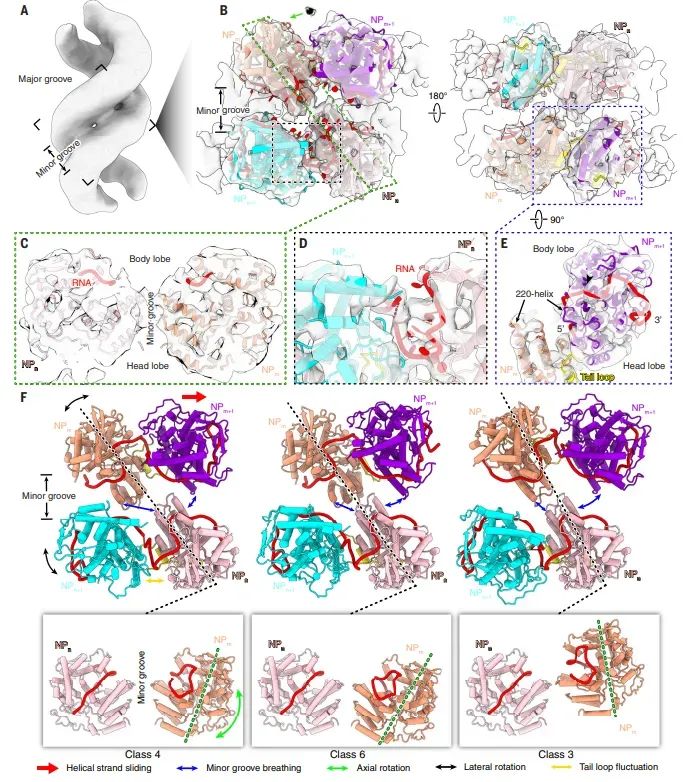
图3流感A病毒天然RNP的构象景观
利用冷冻电子断层扫描(cryo-ET)和子断层平均法(STA)分析了流感A病毒天然RNP的结构。结果显示RNP为右手双螺旋结构,与重组RNP类似,但天然RNP更伸展,展现出更高的动态性。NP亚基在双螺旋中可以沿轴向和垂直于轴向自由旋转,导致相邻NP亚基之间的距离和小沟的宽度沿螺旋路径变化,这种动态性可能有助于RNP在RNA合成过程中的链间滑动。
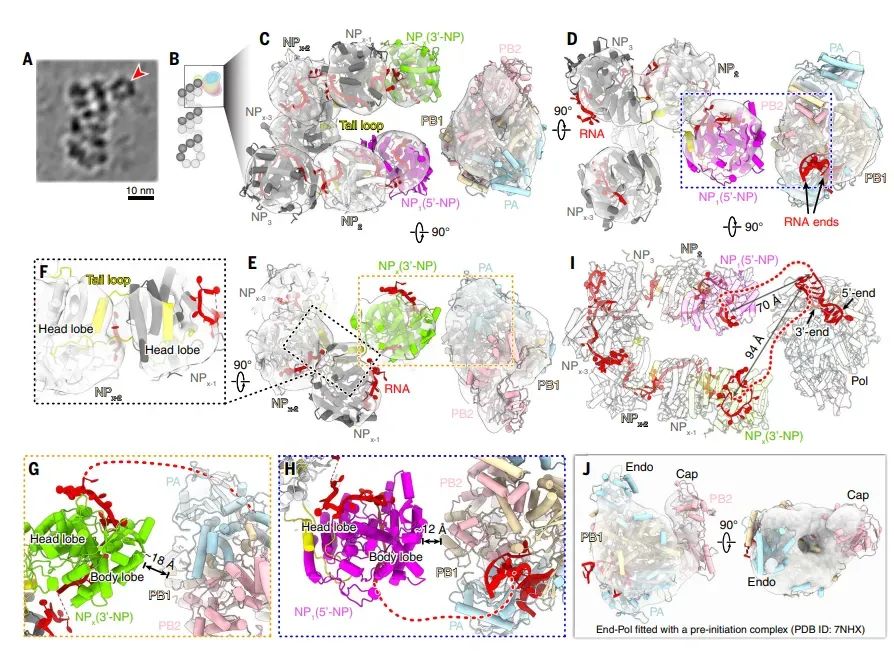
图4流感D病毒NS段RNP聚合酶端的结构
通过冷冻电子断层扫描(cryo-ET)和子断层平均法(STA)解析了流感D病毒NS段RNP聚合酶端的结构。结果显示聚合酶位于RNP末端,与末端NP亚基之间存在约12-18 Å的间隙,表明聚合酶与NP之间的相互作用可能是灵活的或瞬时的。聚合酶的结合需要至少15-20个核苷酸的RNA片段来连接末端NP亚基和聚合酶中的RNA末端。
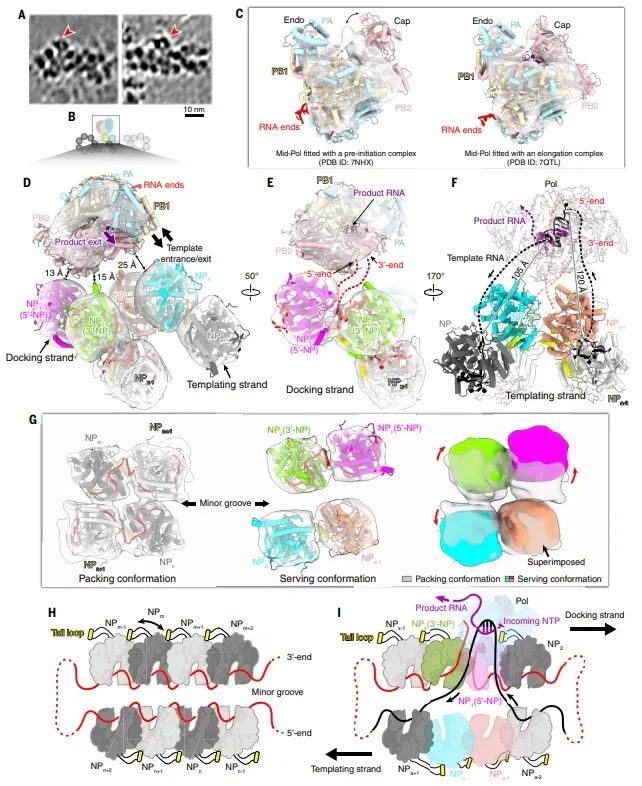
图5流感D病毒NS段RNP在RNA延伸过程中的结构
通过冷冻电子断层扫描(cryo-ET)和子断层平均法(STA)解析了流感D病毒NS段RNP在RNA延伸过程中的结构。结果显示聚合酶位于RNP中间,与两个末端NP亚基相互作用。聚合酶从双螺旋的一侧读取RNA模板,而另一侧的NP亚基则通过局部构象变化(“服务构象”)释放RNA,使其可供聚合酶使用。这种机制允许聚合酶在RNP的一条链上保持静止,而在另一条链上移动,从而实现双螺旋链之间的滑动。
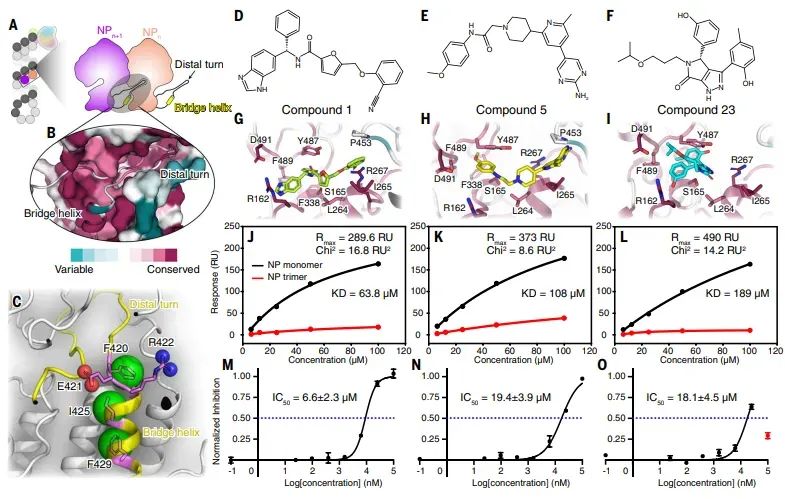
图6针对NP尾环结合界面的抑制剂设计
基于NP尾环结合界面的结构特征,设计并筛选了针对该界面的抑制剂。通过虚拟筛选和表面等离子共振(SPR)实验,识别出三种候选化合物(化合物1、5和23),它们对单体NP具有良好的结合亲和力,而对三聚体NP的结合较弱。这些化合物在细胞实验中显示出对流感A病毒复制的抑制作用,其中化合物1和5的抑制效果较好,且在低浓度下无明显细胞毒性。
【全文总结】
本文通过结合冷冻电镜单颗粒分析(SPA)和冷冻电子断层扫描(cryo-ET)技术,揭示了流感病毒核糖核蛋白复合物(RNP)的高分辨率结构及其在RNA合成过程中的动态机制。研究发现,流感RNP呈现为右手、反平行的双螺旋结构,病毒RNA被封装在双螺旋的小沟中,相邻的核蛋白(NP)亚基通过尾环相互连接。聚合酶复合物在RNP的外表面与双螺旋结构相互作用,通过链间滑动模型沿着RNA模板进行RNA合成,同时保持RNP的整体双螺旋架构。此外,研究还通过虚拟筛选发现了针对NP尾环结合界面的潜在抗流感药物先导化合物,这些化合物在细胞实验中有效抑制了流感病毒的复制。这些发现不仅增进了我们对流感病毒复制机制的理解,还为开发下一代广谱抗流感治疗药物提供了重要的结构基础和潜在的药物靶点。
原文链接:
https://www.science.org/doi/10.1126/science.adq7597
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)