首页 > 医疗资讯/ 正文

阻塞性睡眠呼吸暂停(Obstructive Sleep Apnea, OSA)是一种常见的睡眠障碍,其与高血压、心血管疾病的发病密切相关。尽管其致病机制复杂,近年研究逐渐聚焦于肠道菌群与高血压之间的潜在联系。最新一项来自科研团队的动物研究首次明确了肠道菌群在OSA诱发高血压过程中的关键作用,揭示了通过“肠-心轴”介导的分子机制,为精准治疗带来新思路。
研究背景:OSA与高血压之间的“隐形桥梁”
OSA是一种由于睡眠过程中上气道反复塌陷导致间歇性低氧的疾病,已被广泛证实是继发性高血压的重要危险因素。然而,OSA患者中并非人人都患高血压,这提示其他调节因子可能参与其中。
近年来,肠道菌群被称为“第二基因组”,其在代谢调控、免疫调节、血管功能等多方面扮演关键角色。有研究提示,OSA可引发肠道菌群失调(gut dysbiosis),但其是否为高血压发生的“导火索”,尚缺乏直接实验证据。
实验设计:粪菌移植+分子机制揭示
本项研究采用C57BL6J小鼠模型,创新性地将人类粪菌移植(Fecal Microbiota Transplantation, FMT)与分子机制研究相结合,从而系统评估肠道菌群在OSA相关高血压中的致病作用。
实验共设4组,每组小鼠分别接受来自以下人群的粪菌移植:
-
健康对照者(Control组);
-
纯OSA患者(OSA组);
-
OSA合并前期高血压患者(OSA-pHTN组);
-
OSA合并高血压患者(OSA-HTN组)。
研究者通过测量收缩压、观察主动脉组织变化、菌群16S rDNA测序、以及关键炎症通路蛋白表达,全面剖析“肠-心”信号通路。
研究结果:OSA来源菌群可诱发高血压及血管损伤
实验发现,接受来自OSA、OSA-pHTN和OSA-HTN患者粪菌的小鼠均出现明显的收缩压升高及主动脉损伤,表现出与OSA患者相似的高血压表型。对照组小鼠无类似变化,提示肠道菌群具有决定性的致病潜力。
微生物分析显示,三组患病来源菌群移植组小鼠均存在明显的肠道菌群失调,典型特征为有益菌Akkermansia属显著减少,肠道屏障蛋白如Zonula Occludens-1(ZO-1)和Occludin表达降低,说明肠屏障功能受损。
进一步分子层面分析显示,患病来源组小鼠的主动脉组织中LPS、TLR4和磷酸化NF-κB显著升高,且免疫荧光结果提示TLR4在血管内皮细胞中高度表达,揭示了LPS/TLR4/NF-κB通路在高血压形成中的核心作用。
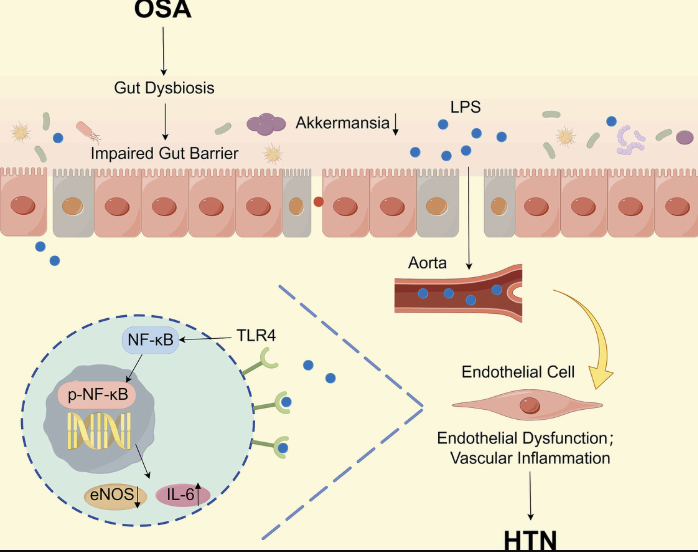
研究结论:肠道菌群是OSA致高血压的“操控者”
这项研究首次在动物模型中证实,来自OSA患者的肠道菌群可通过肠源性LPS激活TLR4/NF-κB炎症通路,诱导血管损伤及血压升高,构成了OSA与高血压之间的关键分子桥梁。
此外,实验还表明,随着患者高血压程度的加深,其肠道菌群致病性呈递增趋势,进一步验证了菌群在疾病进展中的“推进器”作用。
临床启示:微生态干预或成治疗新方向
本研究为OSA相关高血压的防治提供了新的策略思路。未来若能通过干预肠道微生态(如益生菌补充、菌群移植、特定菌种替代等)改善菌群结构,有望打破OSA-高血压的致病链条。
特别值得关注的是,Akkermansia属被认为在维持肠道屏障完整性中具有关键作用,该菌的减少或可作为OSA患者高血压风险的生物标志物。
结语
阻塞性睡眠呼吸暂停与高血压的关系不再仅仅是“氧气与血压”的逻辑链条,本项研究为这一联系增添了“肠道-血管”新通道的证据。通过探索肠-心轴,科学家正揭开慢性疾病背后的“隐秘操控者”。
参考文献
Zhang X, Yin Y, Chen Y, Lin L, Shen S, Fang F, Wang Q. Gut microbiota contributes to obstructive sleep apnea-induced hypertension by gut-heart axis in mice. Int Immunopharmacol. 2025 Apr 16;155:114667. doi: 10.1016/j.intimp.2025.114667. Epub ahead of print. PMID: 40245774.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)