首页 > 医疗资讯/ 正文
前言
急进性肾小球肾炎(RPGN)是一种临床危重症,主要病理表现为大量新月体形成,Ⅰ型RPGN病理表现为肾组织上有抗GBM沉积,又称抗GBM病,也可以肺和肾同时受累,表现为Goodpasture综合征。
该病病程进展迅速,预后差,抗GBM病发病率较低,临床表现不典型,其诊断主要依赖血清或组织中检测出抗GBM抗体。其检测对疾病的诊断具有重要意义。现对一例抗GBM抗体介导的肾小球肾炎患者进行总结,旨在从实验室角度对临床病例进行分析,认识实验室检测方法对临床诊断和治疗的影响。
案例经过
患者男性,69岁,2022年7月17日以“发现蛋白尿5年,尿色加深4天”入院,患者5年前因浮肿于我院就诊发现尿蛋白3+,24小时蛋白尿8g左右,肾功血肌酐正常。当时明确诊断“肾病综合征”,给予“中药汤剂(具体药名及计量不详)”、雷公藤及黄葵治疗。其后未复查。
近1个月患者逐渐出现浮肿,以双下肢为着,4天前发现尿色加深,为洗肉水样,无尿痛,尿急,尿频,16日门诊检查:尿素6.44mmol/L,肌酐130umol/L,总蛋白49g/L,白蛋白28g/L,尿常规:尿潜血3+,尿蛋白3+,红细胞计数969/ul,白细胞计数37/ul,门诊以“血尿”收入院。
查体:慢性病容,轻度贫血外观,浅表淋巴结未触及肿大,双眼睑轻度水肿,心肺听诊正常,全腹无压痛反跳痛及肌紧张,双下肢中-重度浮肿。余体征正常。
入院后胸部CT影像分析:双肺野透过度正常,可见斑片样及条索样密度增高影,边缘清楚,气管、支气管通常,考虑双肺慢性炎症。实验室报告:抗ANA,dsDNA,ANCA谱均阴性,甲状腺功能,凝血功能,心肌酶传染病检查未见异常。
血糖、肾功、离子检测报告:
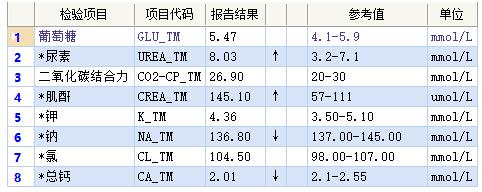
24小时尿蛋白定量检测报告:
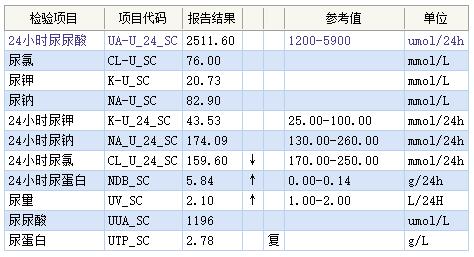
血清蛋白电泳检测报告:
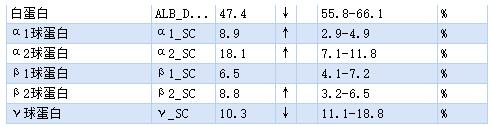
ANCA抗体+抗GBM抗体检测报告:

该患者抗肾小球基底膜抗体阳性,>200RU/mL,血肌酐升高,血尿、蛋白尿,考虑抗肾小球基底膜抗体病诊断明确。本病预后凶险,如不及时治疗,患者多进展为终末期肾脏病,很少有自发缓解的可能。标准治疗是强化血浆置换,联合糖皮质激素和环磷酰胺。
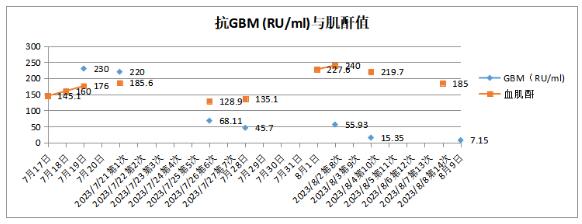
图1 血浆置换治疗中抗GBM浓度与肌酐值变化趋势
表1 不同试剂抗GBM抗体检测结果

A试剂参考区间:<20IU/mL;B试剂参考区间:<1 S/CO ;C试剂参考区间:<20CU
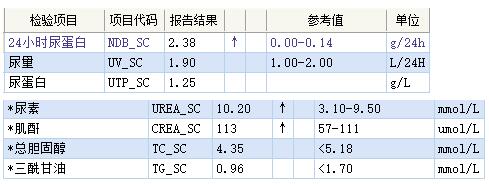
9月30日复查结果:
案例分析
老年男性患者,以蛋白尿、血尿入院,5年前曾于我院诊断“肾病综合征”,查体双下肢中-重度浮肿。根据CKD-EPI公式计算患者肾小球滤过率为47.96mL/min,符合慢性肾脏病3期,给予改善肾功、利尿消肿、降低肾小球囊内压、降低尿蛋白等对症治疗。
患者本人拒绝肾活检,20日实验室回报抗肾小球基底膜抗体阳性,检测值为230RU/mL(酶联免疫吸附法),结合目前肾功、血肌酐升高,血尿、蛋白尿,考虑抗GBM病诊断明确,给予激素冲击治疗3天,次日开始血浆置换治疗,22日冲击治疗后停激素静点,给予美卓乐口服,同时给予应用环磷酰胺口服,连续血浆置换至7次,抗GBM为45.7RU/mL,28日出现感染性发热,不能除外肺炎,给予对症治疗并监测感染相关指标,8月2日继续血浆置换连续7次,7次后检测抗GBM抗体7.15RU/mL,停止血浆置换,继续应用糖皮质激素及环磷酰胺治疗。
在患者血浆置换期间,使用A与B试剂持续监测抗GBM抗体的滴度变化,并在患者进行了数次血浆置换后,使用化学发光的方法(C试剂)复测患者抗GBM抗体。A、B、C试剂的结果出现了不符,患者8月4与9日A试剂结果抗体阴性,C试剂阳性,且滴度呈现下降趋势。
出现不符可能的原因是ELISA与CLIA方法学的差异。文献表明:化学发光法抗GBM抗体检测试剂的灵敏度和特异度分别为97.4%和100%,AUC 0.987, 酶联免疫法为94.9%和97.9%, AUC 0.966。
抗GBM抗体在GBM病的诊疗中至关重要,2020年KDIGO指南推荐对于临床疑似RPGN的患者,无论是否合并肺出血都要进行实验室抗体的检测,其中对于临床高度怀疑抗GBM病的患者,若抗GBM抗体检测结果24小时内未出,在报告出来前要及时开始糖皮质激素与血浆置换的治疗。
实验室检测的及时性可以更好的辅助临床诊疗。在本案例中,患者治疗1个多月后,因呼吸道疾病住院治疗科,检测血肌酐值为113umol/L,略高于正常参考范围,较之前好转。
知识拓展
抗GBM病是以循环中出现抗GBM抗体及其在脏器中沉积为特征的自身免疫病,发病率0.5/百万~1/百万,1919年美国病理学家Goodpasture首先报道1例18岁男性患者,咯血,急性肾双节,病理显示主要累及肺和肾脏。80%就诊时已进入尿毒症期(ESRD),后继发现抗GBM抗体,1988年Saus等发现a3(Ⅳ)NC1区为主要靶抗原。
该病变主要累及基底膜:包括肾小球基底膜(GBM)、肾小管基膜(TBM)、肺泡毛细血管基膜(ABM)及其他组织基膜(如脉络膜、角膜、视网膜血管基底膜等处)。抗GBM病的发病机制被认为是在外界因素诱发下,IV型胶原a345链NC1区四级结构发生改变导致自身抗原暴露,与抗体结合,诱发自身免疫反应。
该疾病的临床表现方面一般急骤起病,多表现为急进性肾炎综合征,明显的血尿和蛋白尿,少数患者起病隐袭,发现时已进展至尿毒症期,发病前驱症状缺乏特异性。部分患者可以出现肺出血而诊断为Goodpasture病,多数患者有小细胞低色素性贫血,贫血程度往往与肾功能损害不平行。通过血浆置换清除循环中的抗体,对于肺出血和肾功能的恢复具有良好的效果。
抗GBM病患者有两个发病高峰,分别在20-40岁和60-80岁,可能与感染、环境因素和遗传背景相关,约半数以上患者有上呼吸道感染的前驱病史,其中多为病毒性感染。抗GBM抗体可以直接参与致病,抗体的免疫学特性对其致病性起了决定性作用,抗GBM抗体滴度的升高、抗体识别的抗原表位的不断扩展、IgG亚型增多、亲和力的不断成熟,在病情的发生进展中起到一定致病作用。
抗GBM抗体可以分为IgG1-IgG4亚型,亲和力高,主要靶抗原位于Ⅳ型胶原a3链的NC1区,有两个主要的抗原构象表位EA和EB,存在于a3链的氨基端,正常情况下隐匿,环境或其它因素可诱使其暴露。在正常人血清中也存天然抗体,但滴度和亲和力都极低。
在累及肺脏的病例中,该抗体的阳性率为80-90%,抗GBM抗体水平与肾脏损伤程度相关,与肌酐和少尿程度具有相关性,同时抗体水平与CD4+T细胞数值呈现相关性。循环中检测到抗GBM抗体是诊断抗GBM病的重要依据,也是治疗监测指标,同时预后不良的提示作用同时对于预后不良具有提示作用。
抗GBM抗体会出现假阳性情况,在SLE患者、一些淋巴增殖性疾病如Castleman可能出现抗GBM抗体阳。会出现,Alport综合征是一种遗传性肾小球基底膜疾病,主要为Ⅳ型胶原的遗传突变,进行肾移植后会出现抗GBM抗体,但不一定有GBM病。HIV病毒感染后也会出现抗GBM抗体阳性情况。临床会有10%左右血清学抗GBM抗体阴性患者。
案例总结
老年男性患者,蛋白尿、血尿入院,血清学检查抗GBM抗体阳性,临床诊断急进性肾小球肾炎,进行标准的血浆置换联合环磷酰胺与激素治疗,本案例患者治疗过程中恢复良好。抗GBM病进展迅速,若血浆置换不充分,抗GBM抗体尚未转阴,患者有很快进展成晚期肾小球肾炎的风险。及时准确的诊断是提高救治的关键。推荐使用多种方法学进行复测,治疗时持续监测抗体滴度直至抗GBM抗体转阴。
参考文献:
[1]Rovin B H,Adler S G,Barratt J,et al.Executive summary of the KDIGO 2021 Guideline for the Management of Glomerular Diseases[J].Kidney lnt,2021,100(4):753-779.
[2]赵明辉.急进性肾小球肾炎,余学清,赵明辉。肾内科学.第3版.人民卫生出版社,2021:27-32.
[3]2019年美国血浆置换学会血浆置换学会血浆置换和免疫吸附临床实践指南(第8版)解读.中华肾病研究电子杂志,2021,10(1):8-13.
[4]AsimM,Akhtar M,Epidemiology,impact,and management Strategies of Anti-GlomerularBasement Membrane Disease.Int J Nephrol Renovasc Dis.2022 Apr7;15:129-138.
[5]系统性血管炎相关自身抗体谱实验室检查及临床应用进展.吴子燕,李永哲.临床实验室,2022年12月刊
[6]Ying Tan, Wei Pang, Xiaoyu Jia & Ming-hui Zhao (2020) Comparison of the performance of a chemiluminescence assay and an ELISA for detection of anti-GBM antibodies,Renal Failure, 42:1, 48-53.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)