首页 > 医疗资讯/ 正文
KMT2A(MLL)基因变异是急性髓系白血病(AML)中一类重要且异质性强的分子异常,包括KMT2A重排(KMT2A-r)、KMT2A部分串联重复(KMT2A-PTD)和双重变异(KMT2A-r/PTD)。
瑞金医院血研所学者开展研究,分析了不同KMT2A变异类型的分子特征与临床表型,探讨了融合伴侣基因对预后的影响,构建了新的风险分层模型,评估了异基因造血干细胞移植(allo-HCT)的疗效。近日发表于《Experimental Hematology & Oncology》。

研究结果
患者
该研究纳入2019年2月至2023年5月收治的125例KMT2A变异AML患者,包括KMT2A-r 36%、KMT2A-PTD、 53%和KMT2A-r/PTD 11%。
分子特征
KMT2A-r:更年轻,继发性AML比例高;突变少,但RAS通路突变富集(KRAS/NRAS/PTPN11,47.6%)。
KMT2A-PTD:突变负荷高,表观遗传调控基因突变常见(如DNMT3A 40%,FLT3-ITD 32.3%,RUNX1 26.2%)。
KMT2A-r/PTD:兼具KMT2A-r和KMT2A-PTD特征,提示KMT2A-r为起始事件,PTD为进展事件;支持“KMT2A-r启动白血病,PTD促进进展”的层级模型。
融合伴侣与预后(KMT2A-r组)
KMT2A-r 的预后与融合伴侣密切相关:MLLT3/ELL 融合预后较好,中位EFS未达到;AFDN等其他融合预后差,中位EFS 3.9–7.3个月;若同时存在KMT2A-PTD,则MLLT3/ELL的生存优势消失,中位EFS 17.6个月。
新的三层次风险模型(基于融合伴侣与PTD状态)
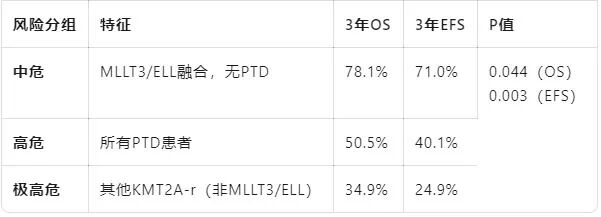
新模型在预测OS和EFS方面优于ELN 2022标准(AUC更高)。
allo-HCT显著改善生存
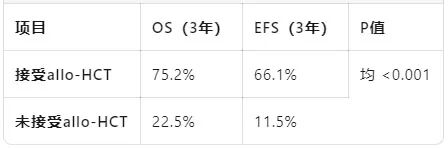
CR1期移植者预后最佳:32个月OS为90.2%,显著优于非CR1移植者(36.4%,P <0.001)。allo-HCT获益主要集中于高危和极高危组,中危组未显示显著获益(P = 0.461)。
多因素分析独立预后因素
有利因素:两个疗程内达到完全缓解(CR);接受allo-HCT。
不利因素:KRAS突变(KMT2A-r组);FLT3-TKD突变(KMT2A-PTD组)。
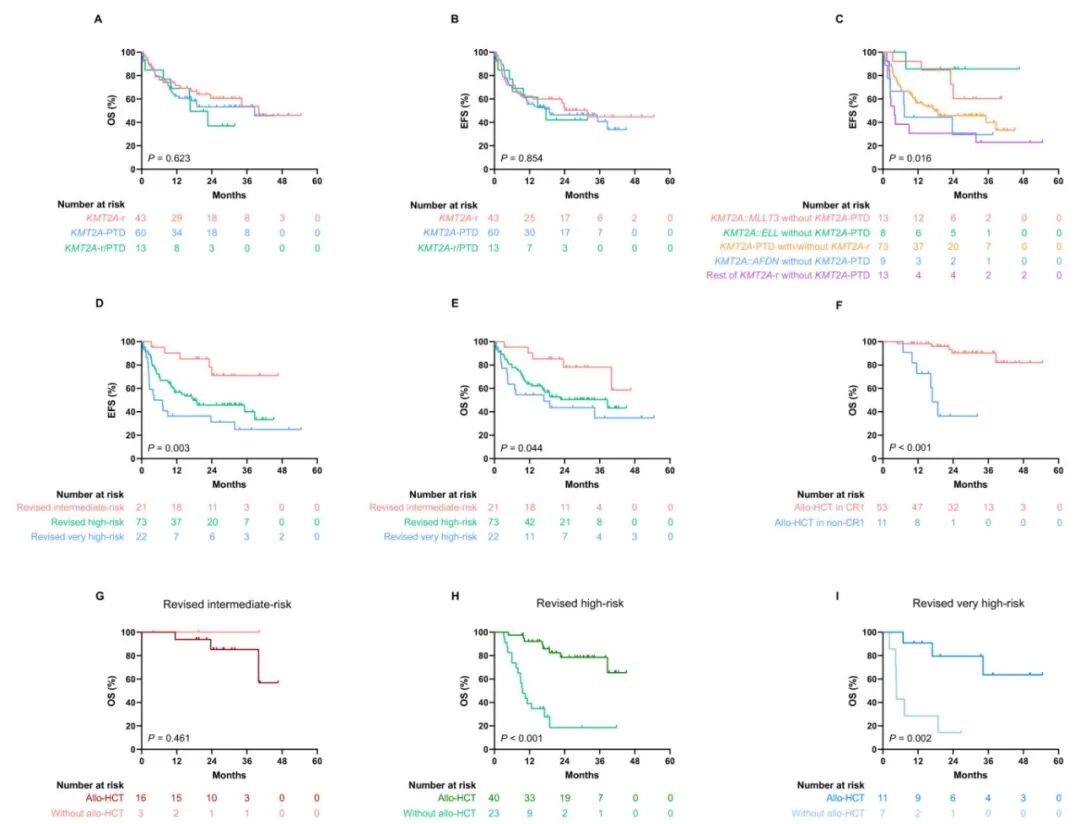
KMT2A突变型急性髓系白血病(AML)的生存与移植结局
A–C 不同分子亚型生存的Kaplan–Meier曲线
D、E 基于新修订的三层风险模型的生存分析
F allo-HCT对CR1与非CR1患者总生存的影响
G–I 各修订风险亚组内allo-HCT的结局
总结
KMT2A变异AML具有显著的分子和预后异质性。
KMT2A改变类型与融合伴侣基因显著影响AML患者预后。MLLT3/ELL融合者预后最佳,但合并PTD会削弱其优势。
提出的三层次风险模型能有效分层患者预后。
allo-HCT可显著改善生存,尤其适用于高危/极高危患者,推荐在CR1期进行。
推荐对高危/极高危患者尽早行allo-HCT,并探索menin抑制剂等新型靶向药物。
该研究支持基于分子特征的风险分层治疗策略,推动精准治疗。
参考文献
Chen, L., Li, J., Zhu, Y. et al. KMT2A alterations in acute myeloid leukemia: a proposed genetic risk model and transplantation outcomes. Exp Hematol Oncol 14, 123 (2025). https://doi.org/10.1186/s40164-025-00714-8
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)