首页 > 医疗资讯/ 正文
在全球范围内,听力损失是导致残疾的主要原因之一,约有4.3亿人患有不同程度的听力障碍,其中遗传性耳聋占据了先天性听力损失的约60%。常染色体隐性遗传性耳聋9(DFNB9)是由OTOF基因突变引起的一种常见听觉神经病变,该基因编码耳铁蛋白(otoferlin),该蛋白在内毛细胞带状突触中负责囊泡释放和神经递质Ca²⁺依赖性外排。患者通常表现为先天性或语前性重度至极重度双侧听力损失,听性脑干反应(ABR)缺失,而耳声发射(OAE)往往可正常引出,反映出内毛细胞功能受损而外毛细胞功能保留的典型特征。近年来,基因治疗在遗传性耳聋领域取得了显著进展,尤其是基于腺相关病毒(AAV)的基因替代策略,已在多项临床试验中显示出恢复听力的潜力。然而,基因治疗后听觉通路的功能恢复过程及其评估方法仍不明确,尤其是在儿童患者中,行为测听难以实施,客观听力学评估的价值亟待系统研究。

本研究共纳入10例接受基因治疗的DFNB9患者,其中5例接受单侧治疗并随访52周,另5例接受双侧治疗并随访26周。所有患者在治疗前均未检测到ABR波形,即使在95 dB nHL的刺激强度下亦无反应。治疗后,通过多项听力学检测方法系统收集数据,包括听性脑干反应(ABR)、听觉稳态反应(ASSR)、畸变产物耳声发射(DPOAE)和纯音测听(PTA)。ABR测试采用短纯音刺激,在麻醉状态下进行,记录电极放置于皮肤表面,测定0.25、0.5、1、2和4 kHz频率下的反应阈值及波V潜伏期和振幅。ASSR在隔声室中完成,通过气导耳机施加频率特异性刺激,记录Fz、乳突和Fpz位置的电极响应,以评估各频率听觉阈值。PTA仅在4名能配合的患儿中进行,采用递减法确定气导和骨导听阈。DPOAE测试使用两个纯音(f₁和f₂,f₂/f₁=1.22)同时刺激,记录2f₁–f₂畸变产物的信噪比(SNR),以评估外毛细胞功能。
结果显示,基因治疗后患者听觉功能逐步恢复。至13周时,所有10名患者均可在ABR中识别出波V,且随着时间推移,波V潜伏期显著缩短,振幅呈上升趋势。以1 kHz频率为例,在85 dB nHL刺激下,波V潜伏期从治疗4周时的9.220 ms(范围9.015–9.810 ms)缩短至52周时的8.190 ms(范围7.780–8.530 ms),差异具有统计学意义(p=0.004)。波V振幅虽未达到显著差异(4周为0.200 μV,52周为0.310 μV,p=0.055),但整体呈上升趋势。在部分患者中,治疗后还可观察到波I和波III的出现,波I在13周时检出率为6.7%,最终随访时增至13.3%;波III在6周时检出率为6.7%,26周时达到60.0%,提示听觉通路逐渐恢复同步化活动。除1 kHz外,0.5、2和4 kHz频率也表现出类似的潜伏期缩短和振幅增加趋势。
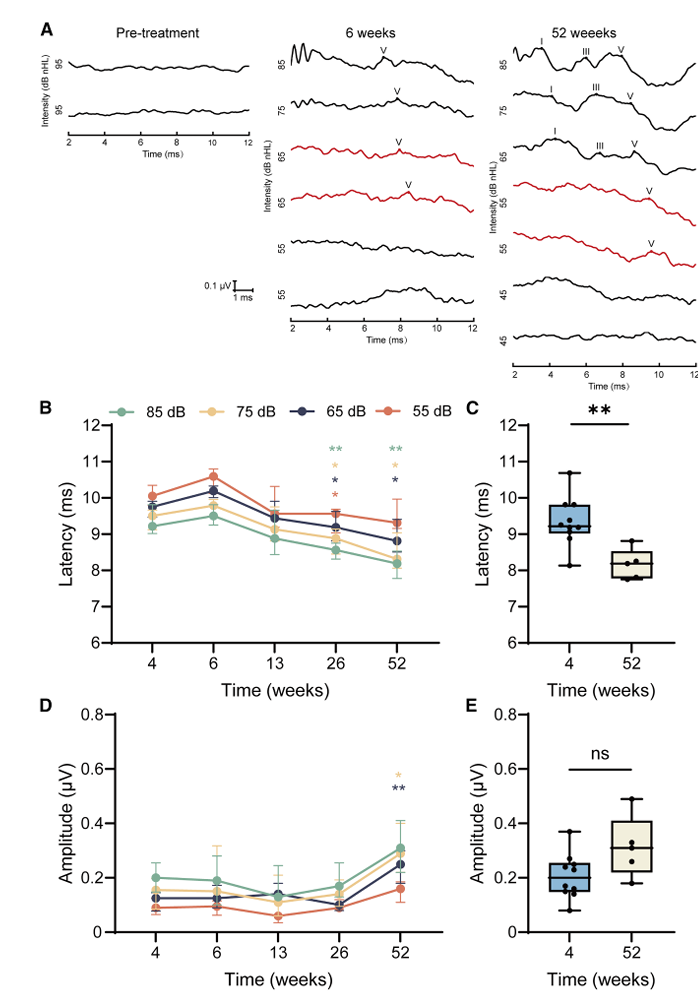
图1. 患者基因治疗后1 kHz ABR波V振幅和潜伏期随时间的变化
为进一步探究治疗前因素对疗效的影响,研究对26周时75 dB nHL刺激下1 kHz ABR波V的潜伏期和振幅进行了分组分析。根据中位数将患者分为长潜伏期/短潜伏期组和高振幅/低振幅组,并分析年龄、性别、人工耳蜗植入史、助听器使用史、听觉行为分类(CAP)和言语可懂度分级(SIR)等因素的分布差异。结果显示,潜伏期长短与年龄、性别或助听器使用无显著关联,但有人工耳蜗植入史、CAP>0或SIR>1的患者更倾向于表现出较短潜伏期。在振幅方面,人工耳蜗植入、CAP>0和SIR>1与较高的波V振幅显著相关(p值分别为0.027、0.005和0.027),提示早期干预和较好的听觉言语基础可能有助于基因治疗后听觉通路的神经反应增强。
PTA、ABR和ASSR阈值之间显示出显著的正相关关系。由于患儿年龄小、配合差,仅4名患者(5耳)能完成PTA测试。Spearman相关分析表明,在0.5、1、2和4 kHz频率下,PTA与ABR阈值的相关系数分别为0.630、0.428、0.683和0.702(p值均<0.05),PTA与ASSR阈值的相关系数分别为0.760、0.466、0.810和0.754(p值均<0.05)。ABR与ASSR阈值之间也存在显著正相关,相关系数在0.5–4 kHz范围内介于0.509–0.702之间(p<0.001)。这一结果证实了ABR和ASSR可作为评估基因治疗后听力恢复的可靠客观工具,尤其适用于无法配合行为测听的儿童患者。
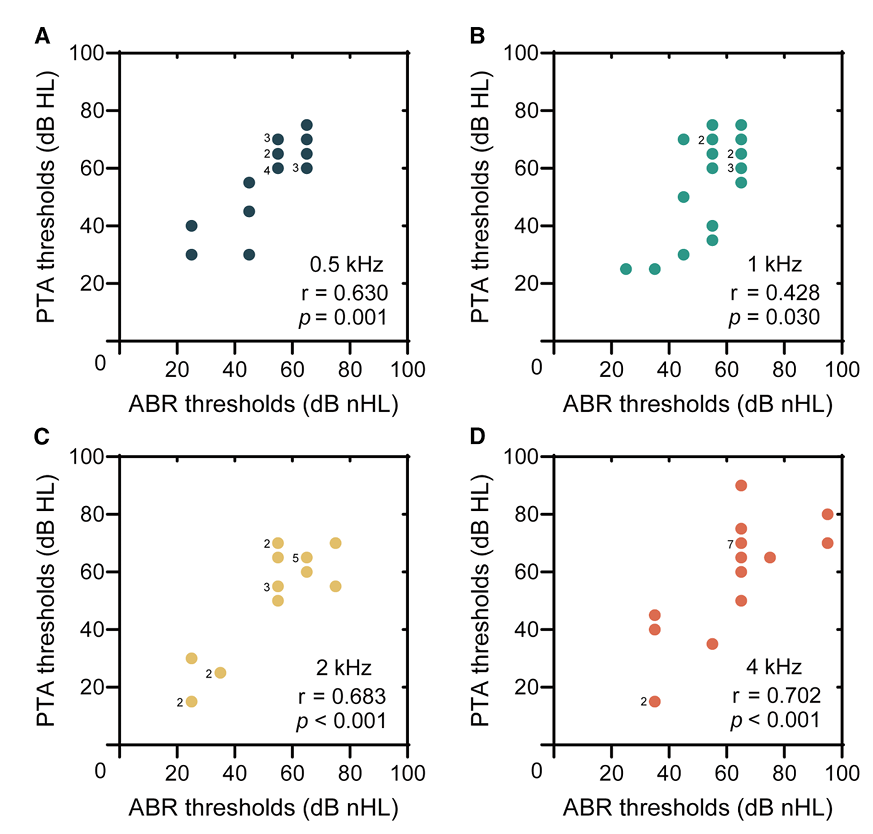
图2. 基因治疗后患者纯音听阈与ABR阈值之间的相关性
DPOAE测试结果显示,基因治疗对外毛细胞功能未产生显著影响。治疗前与治疗后26周的各频率DPOAE信噪比(SNR)无统计学差异,且治疗前SNR值与治疗后ABR阈值之间无显著相关性。虽然在52周时0.5 kHz处SNR出现显著变化(p=0.026),但因样本量减少(仅5耳),该结果需谨慎解读。此外,根据OTOF基因突变类型将患者分为截短突变+非截短突变(T+N)、双截短突变(T+T)和双非截短突变(N+N)三组,分析其与26周时ABR阈值的关系,结果显示各频率阈值在不同基因型组间无显著差异(p值均>0.05),表明基因治疗效果可能不受突变类型的显著影响。
本研究通过系统分析DFNB9患者基因治疗后听觉通路的变化,证实ABR和ASSR是评估听力恢复的可靠客观手段。波V潜伏期的缩短和振幅的增加反映了听觉通路的神经可塑性变化,包括内毛细胞-听神经突触功能的修复和中枢听觉通路的重组。基因治疗未对外毛细胞功能产生负面影响,且治疗前DPOAE水平与治疗后听力恢复无显著关联。多项客观听阈评估方法之间存在高度一致性,为临床监测听力恢复提供了重要依据。尽管样本量较小且缺乏言语感知结果评估,本研究为DFNB9基因治疗的疗效和安全性提供了深入见解,并为未来优化治疗策略和评估方案奠定了基础。
原始出处:
Zhang, L., Dong, D., Yin, Y., Tang, H., Lv, J., Cao, Q., Wang, W., Chen, B., Wang, Y., Li, H., Wang, D., & Shu, Y. (2025). Audiological characteristics following gene therapy in patients with autosomal recessive deafness 9. Med, 6, 100696. https://doi.org/10.1016/j.medj.2025.100696
本文相关学术信息由梅斯医学提供,基于自主研发的人工智能学术机器人完成翻译后邀请临床医师进行再次校对。如有内容上的不准确请留言给我们。
猜你喜欢
- 危重症患者白蛋白的使用或误用
- 下巴长痘痘的原因中医
- Eur Heart J:伴有或不伴有心力衰竭个体利尿剂应用情况比较
- 北京有序开放医院陪护探视
- Hematology:原发性免疫性血小板减少症患者血小板糖蛋白特异性抗体与短期大剂量地塞米松疗效及出血评分的关系
- 如何护理唇部脱皮会出血症状
- 春护健康 片仔癀与您同行——湘西片仔癀国药堂德夯大峡谷店-“养肝爱肝,爱护健康”
- Orthop J Sports Med:髌股内侧韧带重建的全缝线锚定内固定研究
- 肿瘤缓解率91%!百时美施贵宝自体CAR-T疗法BMS-986393治疗多发性骨髓瘤新疗效数据公布!
- 问诊分析:肺混合磨玻璃结节,随访2年报告说相仿就真的相仿吗?
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)