首页 > 医疗资讯/ 正文
导读
2025年2月19日加州大学Hideho Okada、Joseph Costello团队与纪念斯隆凯特林癌症研究所Christopher A. Klebanoff合作,在《Nature》发表题为《Tumour-wide RNA Splicing Aberrations Generate Actionable Public Neoantigens》的研究论文,为低肿瘤突变负荷(TMB)及高异质性癌症患者提出突破性解决方案:通过靶向RNA剪接异常产生的广谱公共新抗原,破解免疫治疗耐药困局。
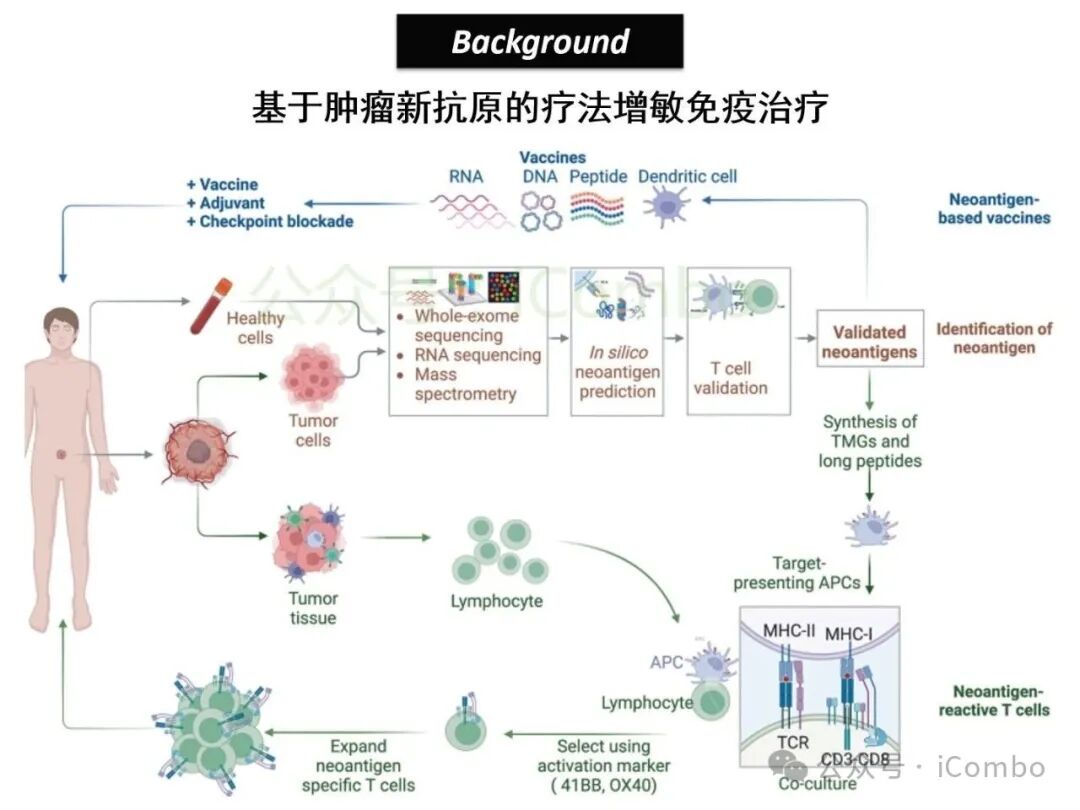
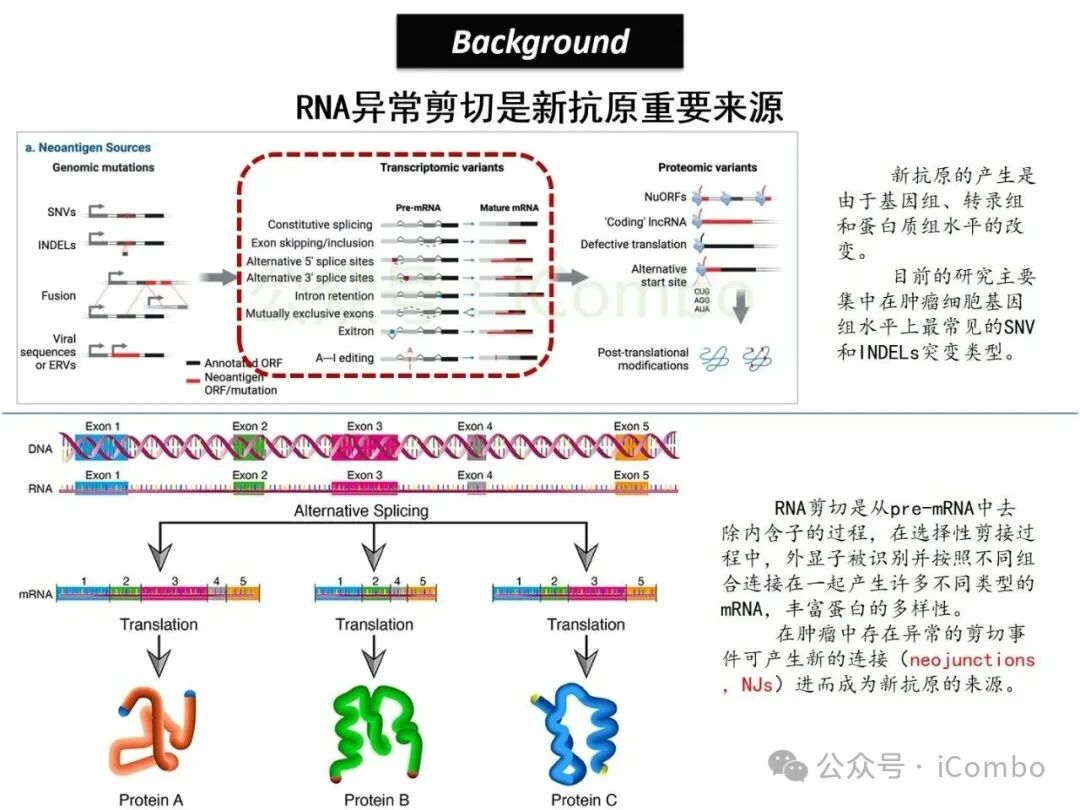
肿瘤异质性导致的免疫逃逸是T细胞疗法在低突变癌症中失效的核心难题。传统新抗原研究聚焦于基因突变,而剪接异常产生的“基因碎片”长期被忽视。该研究首次揭示,这些“碎片”可编码跨患者共享的公共新抗原,为攻克异质性提供新范式。
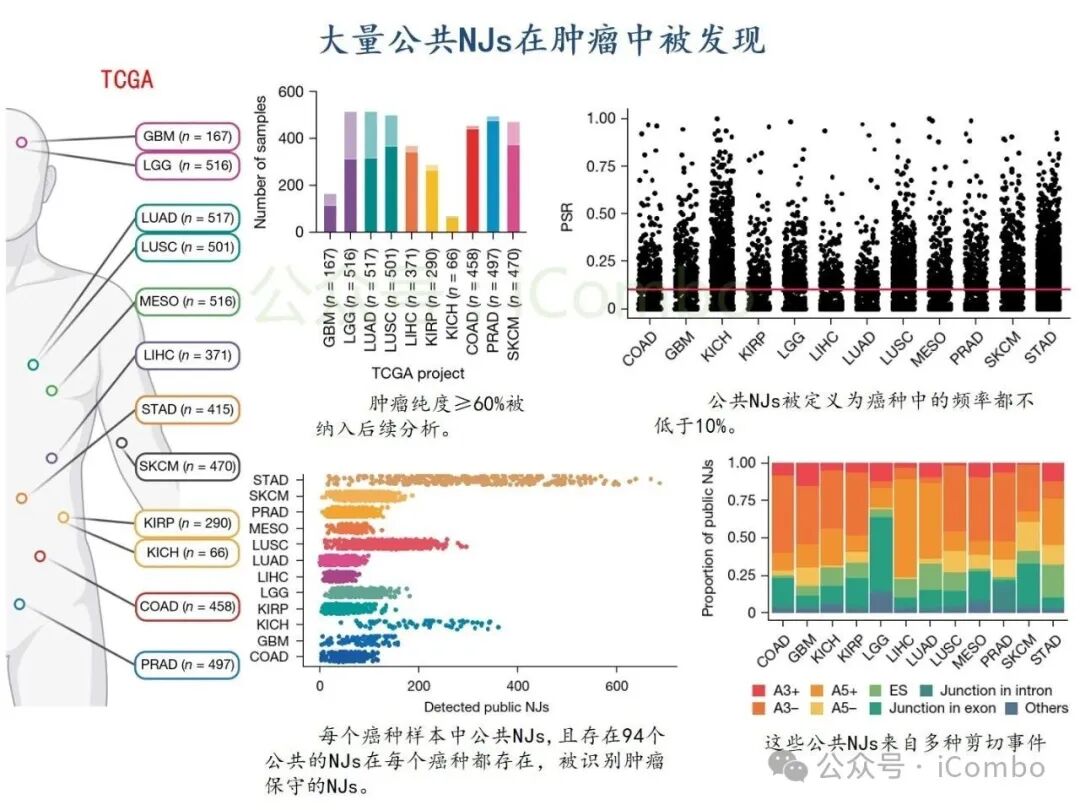
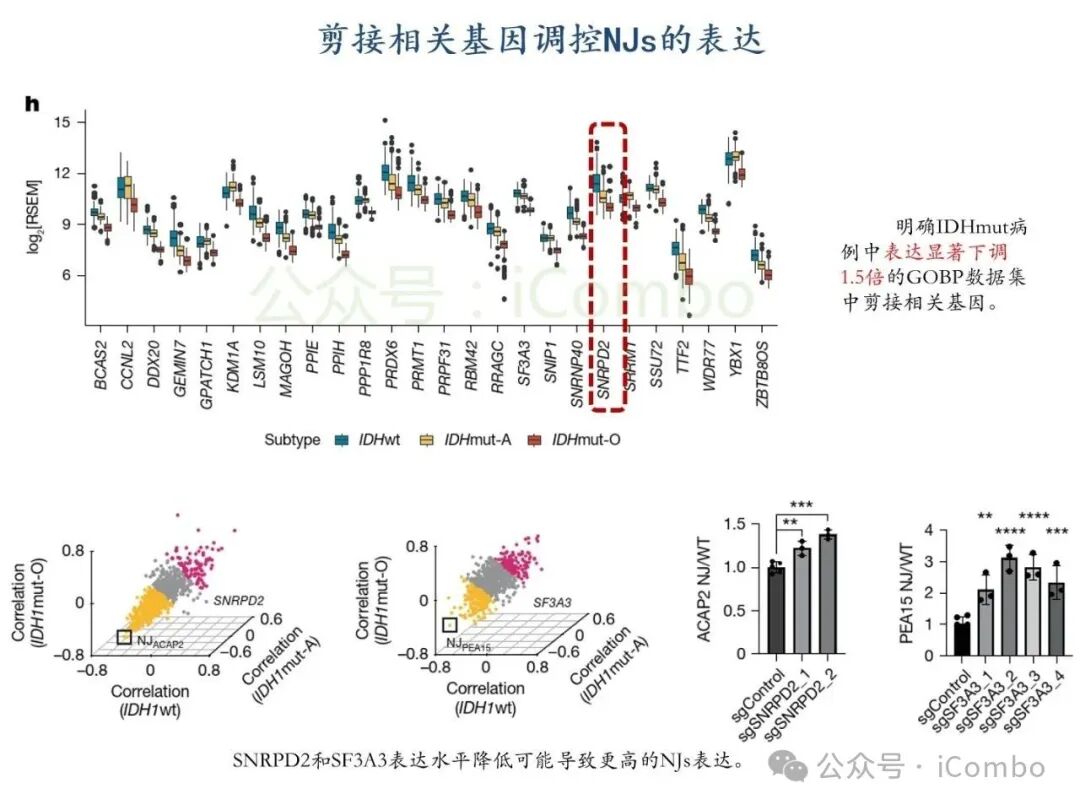
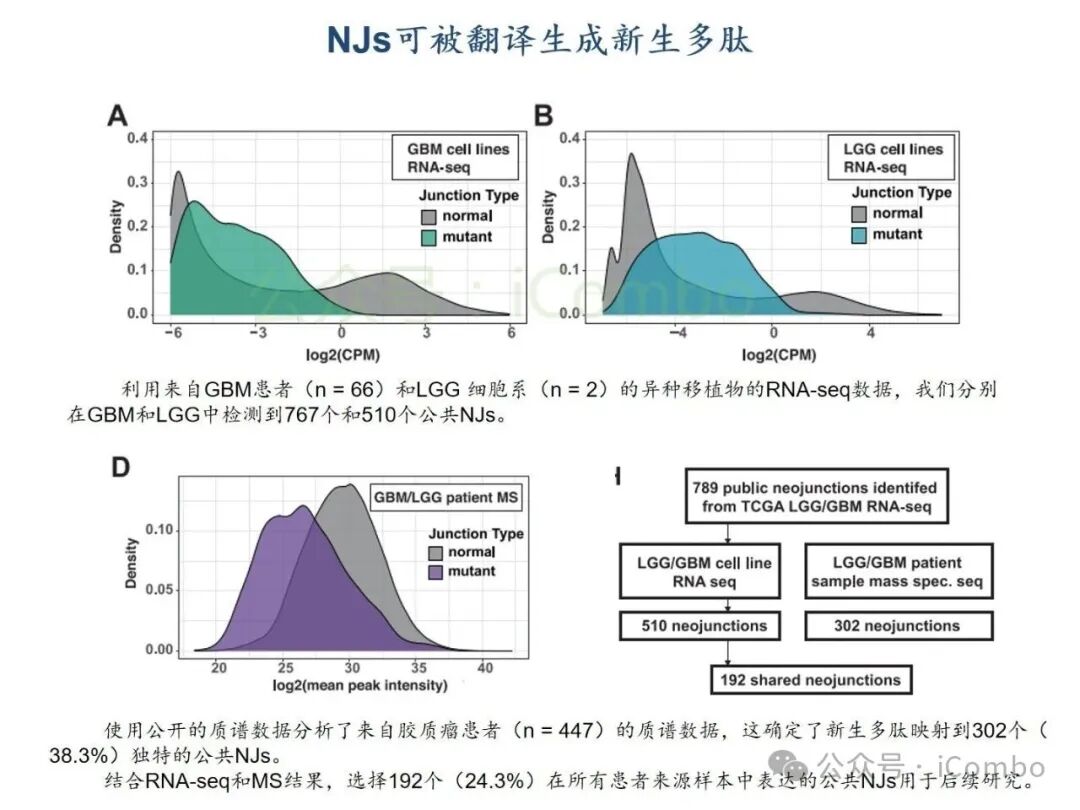
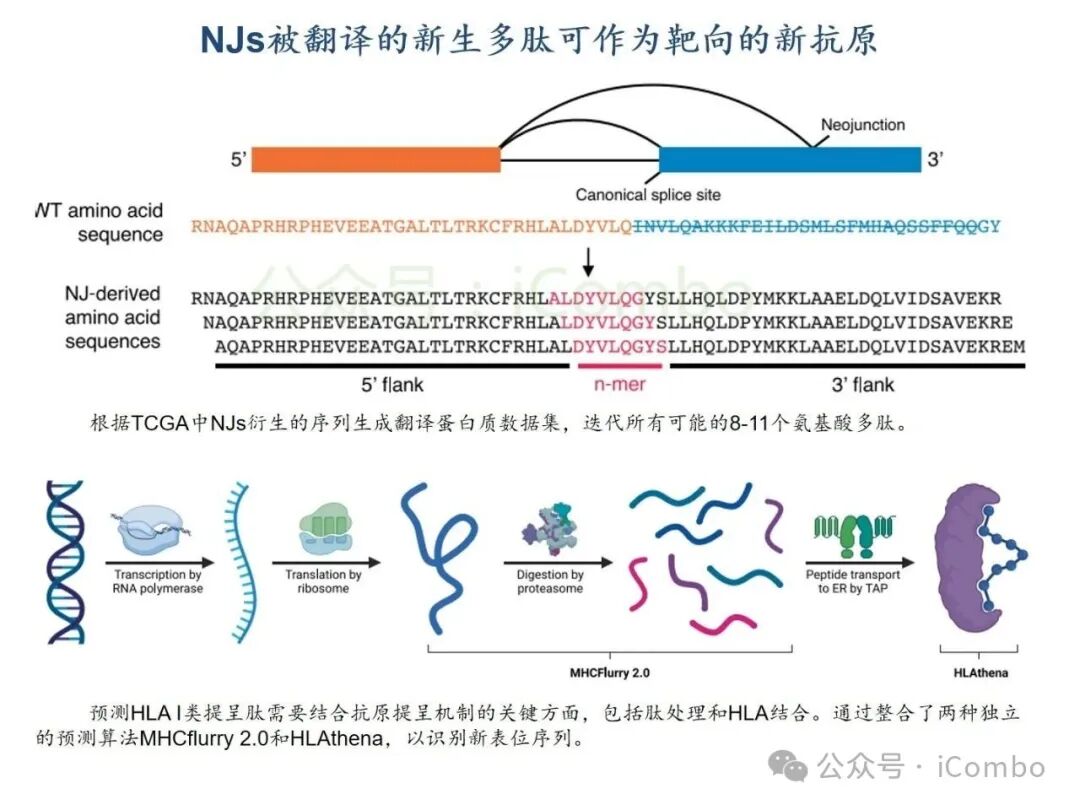
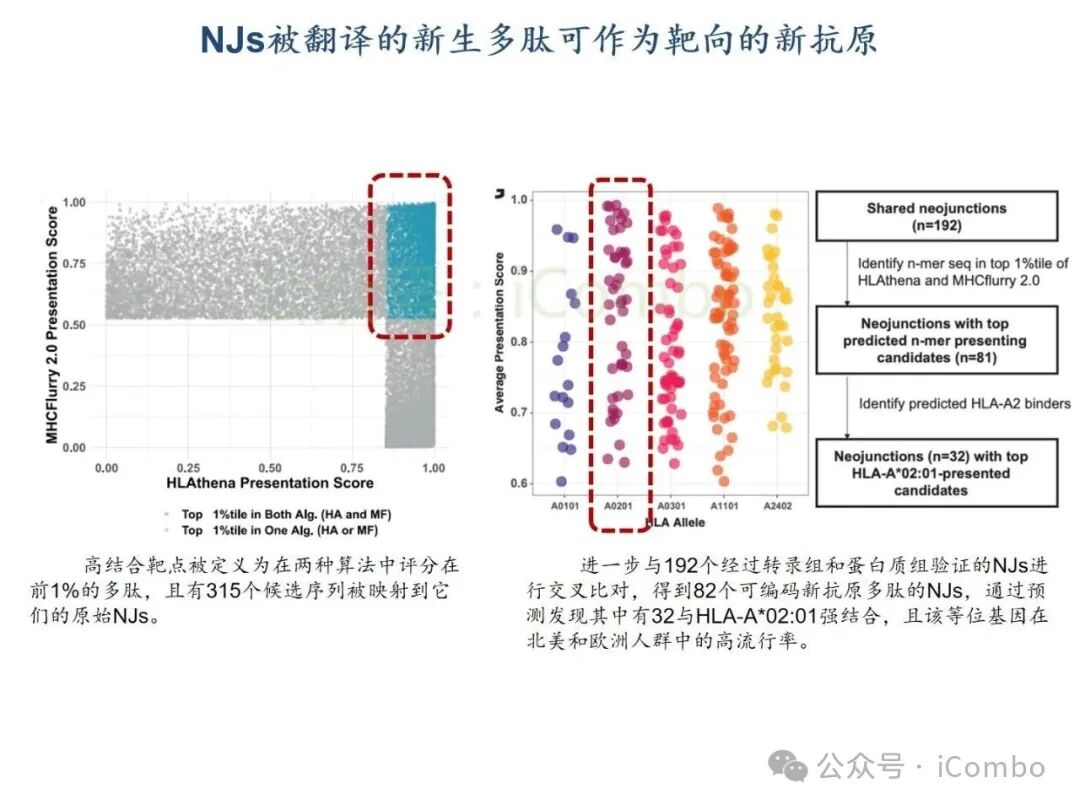
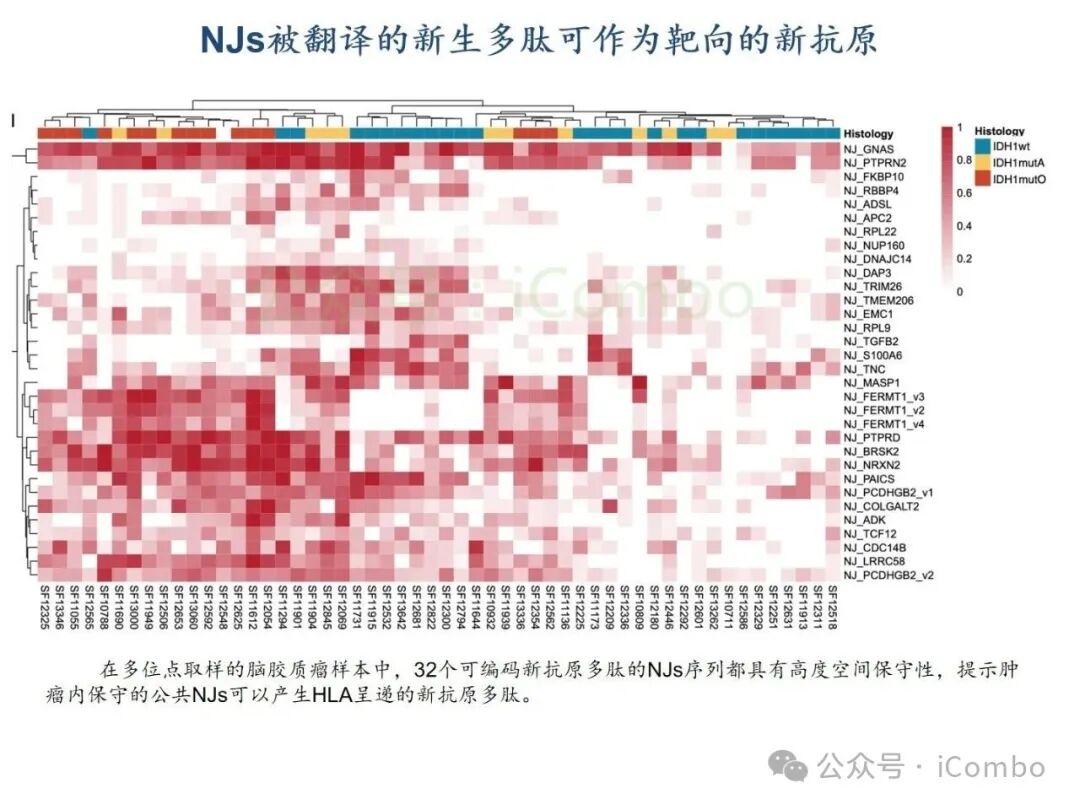
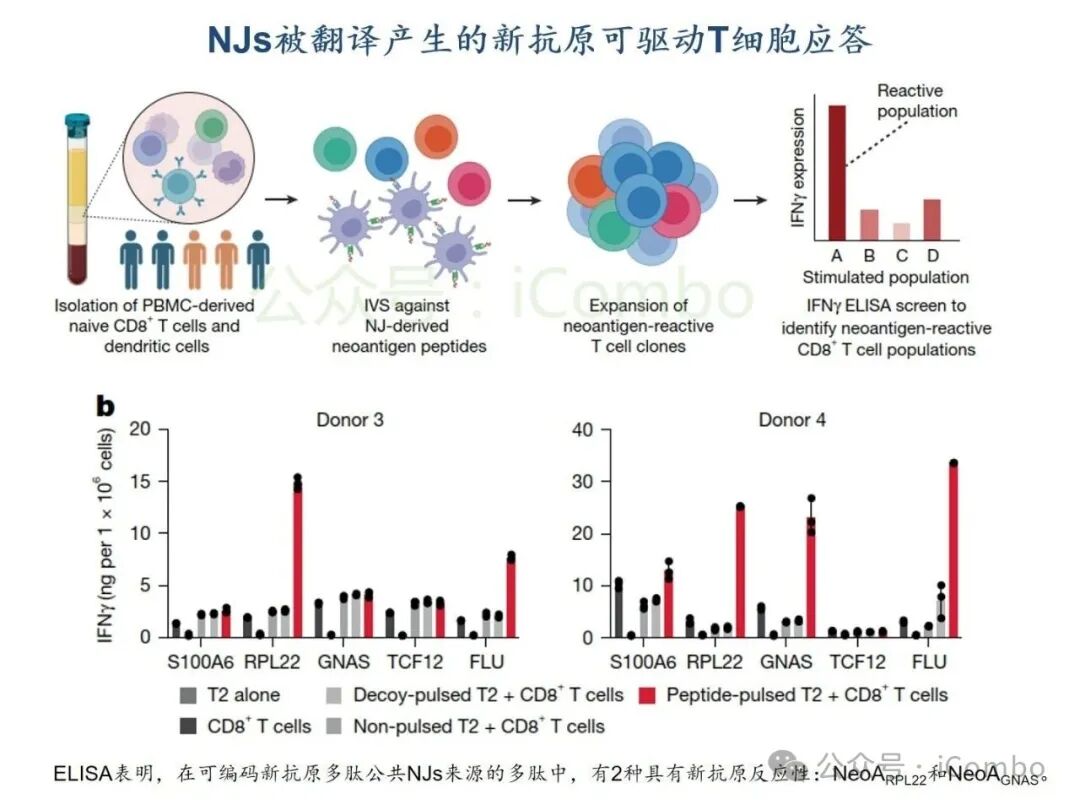
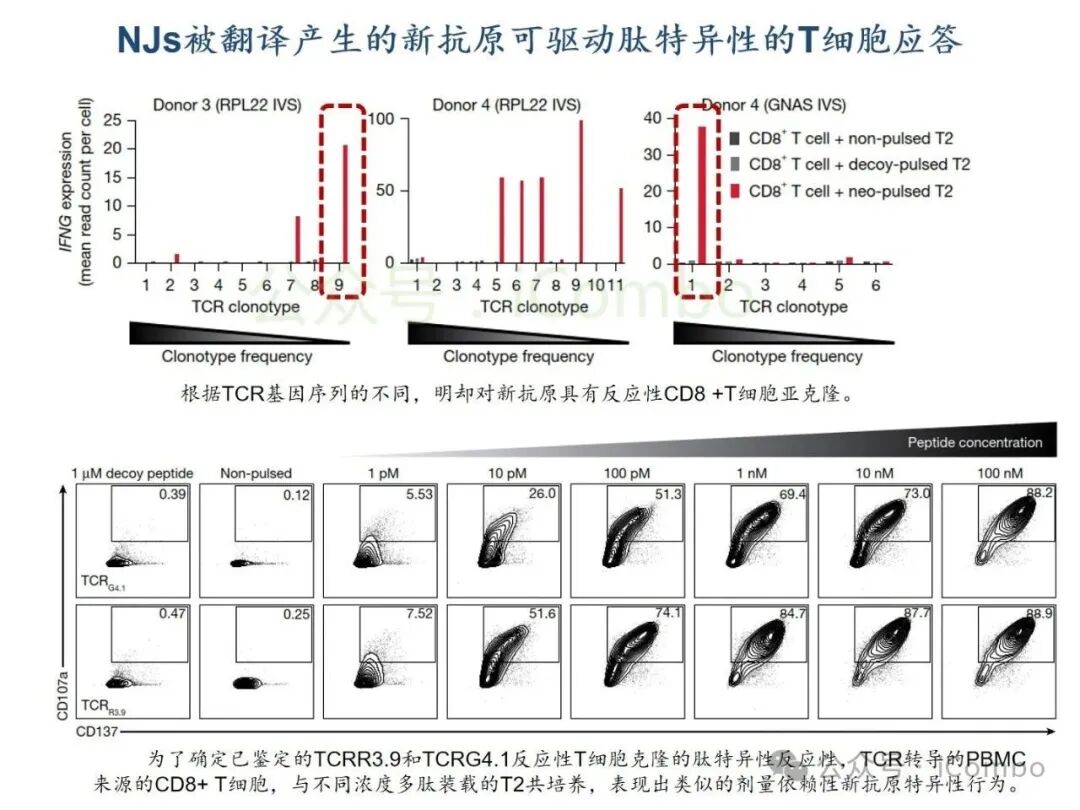
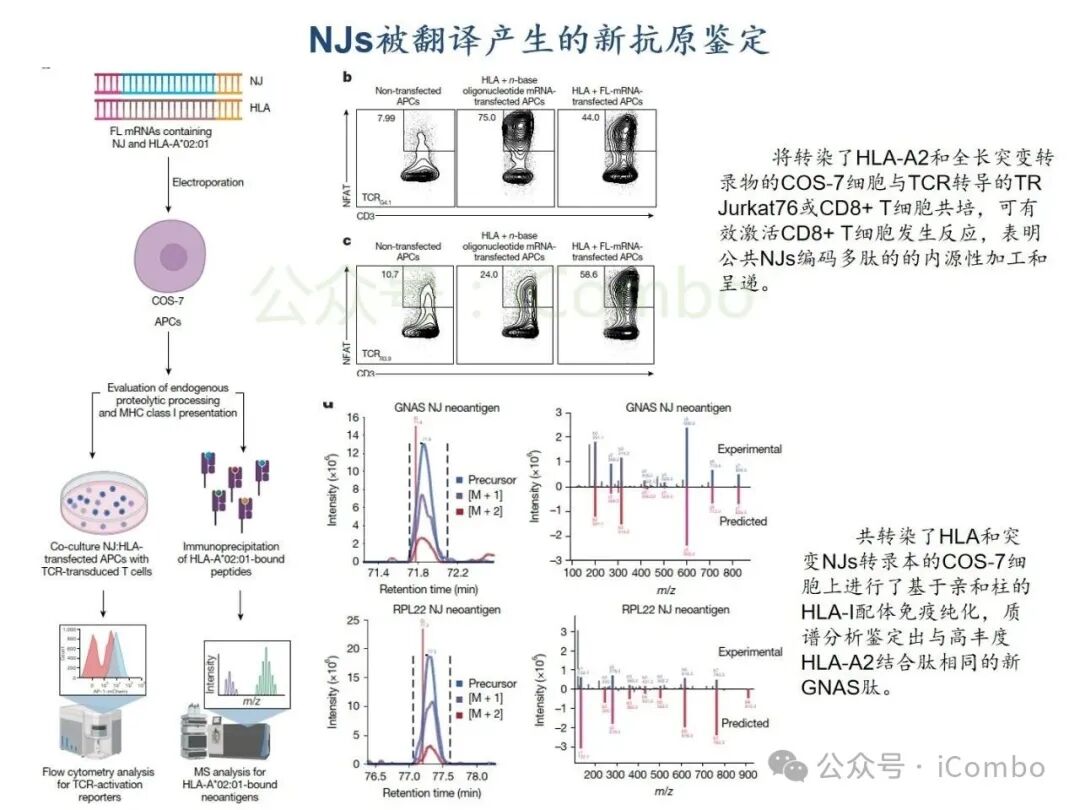
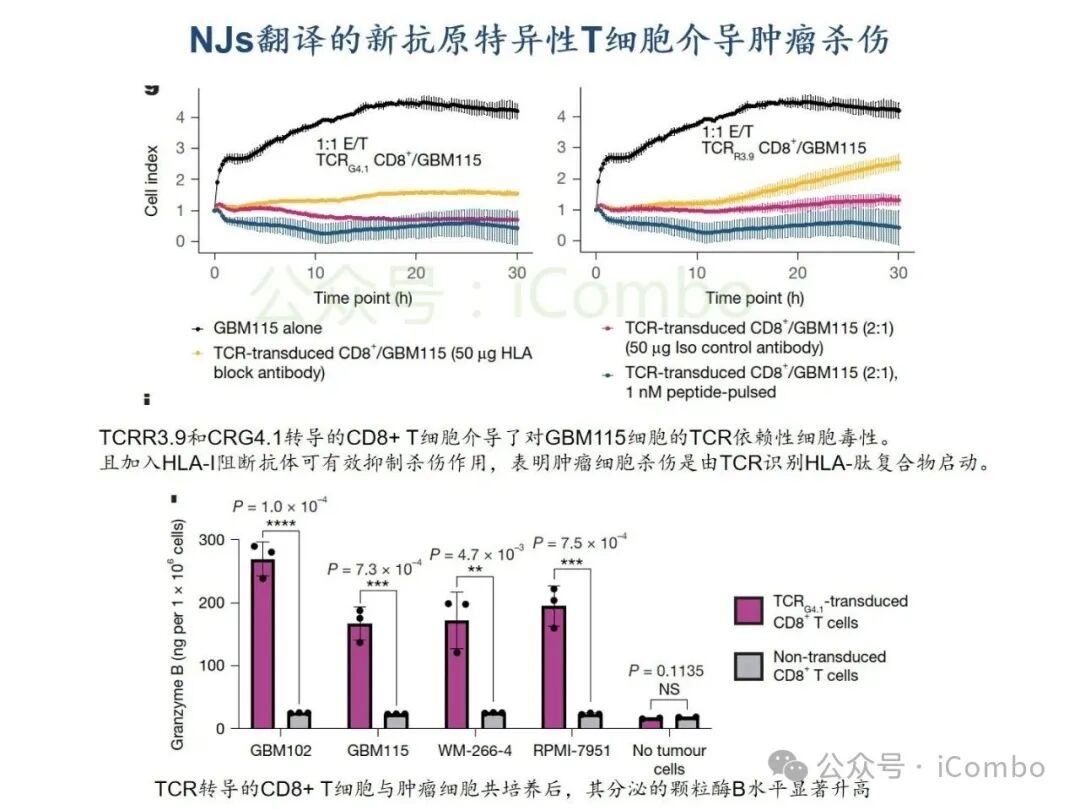
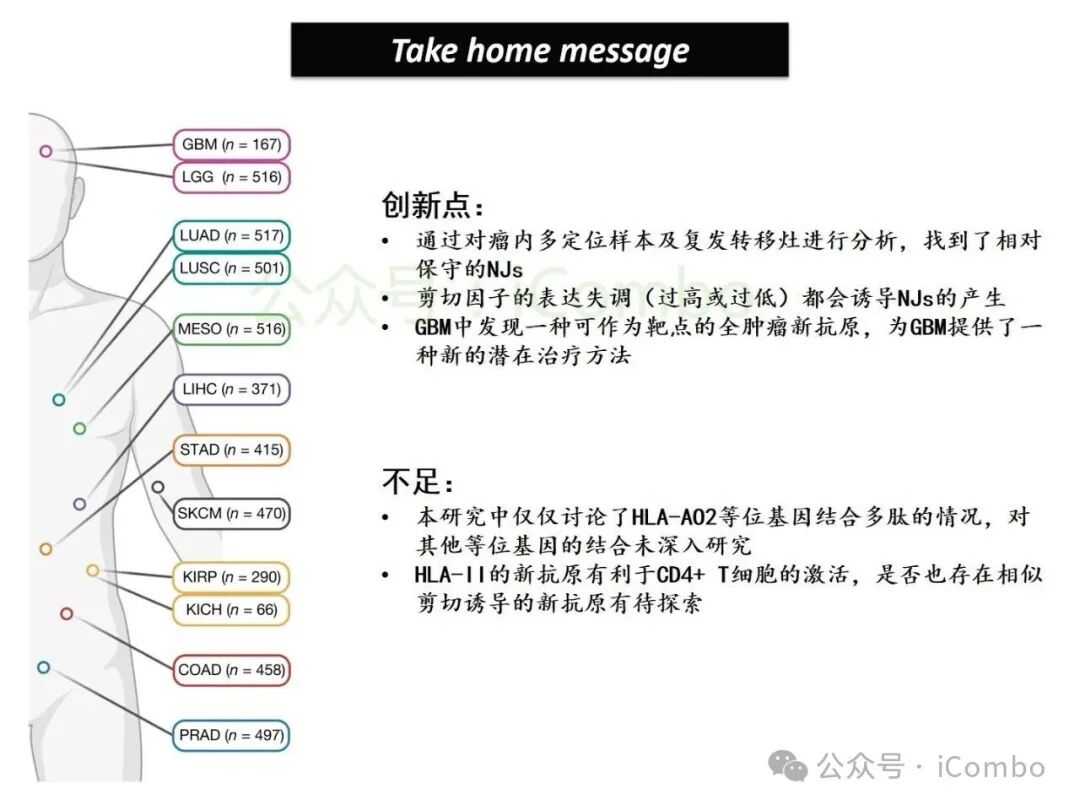
基于TCGA转录组分析,结直肠癌、肺癌、乳腺癌等实体瘤中高频剪接异常普遍存在,其中胶质母细胞瘤(GBM)和低级别胶质瘤(LGG)中异常肽段(如NeoARPL22、NeoAGNAS)通过HLA-I分子高效呈递,形成强免疫原性新抗原。质谱实验证实,患者T细胞可特异性识别并杀伤携带此类新抗原的肿瘤细胞。研究团队进一步构建TCR工程化T细胞,在GBM细胞共培养杀伤模型中实现肿瘤生长抑制率超70%,表明肿瘤内异常剪切生成的多肽,可被被内源性处理和呈递,进而使新抗原特异性CD8+ T细胞产生肿瘤细胞毒性。
该研究颠覆了传统新抗原的认知框架,揭示RNA剪接错误是深埋于肿瘤中的“抗原金矿”。公共新抗原的跨癌种保守性不仅为异质性难题提供“通用钥匙”,更推动广谱免疫疗法迈向临床。未来需突破规模化T细胞递送技术、验证临床安全性,并探索剪接因子调控网络以开发协同疗法,最终引领癌症治疗迈入“精准靶向”与“普惠广谱”并行的新纪元(Nature. 2025 Mar;639(8054):463-473. doi: 10.1038/s41586-024-08552-0)。









- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)