首页 > 医疗资讯/ 正文
组织病理学是疾病诊断的金标准,穿刺活检是获取组织的关键。脾脏具有富血供、质脆的特性[1],传统穿刺活检后,患者面临高出血风险[2](出血率为2%~5%,甚至更高[3]),极大限制了其在临床的广泛应用。细针穿刺虽相对安全,但获取的样本量常不能满足淋巴瘤分型的诊断需求。影像学检查虽能显示病变部位[4],但若要实现明确诊断,并契合现代精准医疗(如分子病理学)对组织样本的高质量需求,仍需依赖组织病理学诊断。脾脏活检不仅具有较高的出血风险[4-5],还存在0.5%~0.9%的针道种植转移风险[6]。当前,现有风险降低策略均存在一定局限性,即使实施了严格的预防措施,并发症发生率仍较高[7]。
针对此困境,本研究团队研发了一种集成射频消融(RFA)功能的新型穿刺活检针。该活检针能在取样后立即对针道进行热凝固处理,从而有效降低出血和肿瘤种植转移风险。在动物模型中已初步证实,该项技术可行、安全,并可降低出血风险[2]。本研究首次将具有RFA功能的新型活检针应用于脾脏病变需行穿刺活检的患者,前瞻性评估同轴穿刺活检与RFA系统在此类患者中应用的安全性、有效性及技术可行性,旨在为脾脏疾病诊断提供更为安全、有效的微创活检新策略。
1 对象与方法
1.1 研究对象
本研究为单臂前瞻性研究,以2023年5月—2025年2月于浙江大学医学院附属第一医院就诊的脾脏病变行穿刺活检患者为研究对象。
纳入标准:(1)年龄≥18岁;(2)有明确临床穿刺需求,需在超声引导下行经皮脾脏穿刺活检以获取组织病理学诊断,具体包括不明原因脾脏占位性病变的定性诊断、弥漫性脾脏病变或脾肿大病因探查、血液系统恶性肿瘤脾脏受累情况评估或分期等。
排除标准:(1)无法耐受局部麻醉或穿刺操作;(2)有严重合并症,不能耐受穿刺手术;(3)有严重感染或其他禁忌证。
本研究所有操作流程均严格遵守《赫尔辛基宣言》的相关准则,并经浙江大学医学院附属第一医院伦理审查委员会批准(审批号:2025B-0356)。所有入组患者参与研究前均签署书面知情同意书。
1.2 仪器与方法
1.2.1 设备介绍与工作原理
本研究采用的创新性活检器械为一套集成RFA功能的双极活检针系统(湖南伽奈维16G-120S15D),型号16 G,针体长度120 mm,直径1.6 mm。该系统主要核心组件构成见图1。

图1 射频消融电极核心组件构成
中空外鞘管:该管道是后续穿刺引导、活检取样、RFA等所有操作的工作通道;
三棱内芯针:配合外鞘管进行初始组织穿刺,引导外鞘管精准到达目标位置;
圆头内芯电极针:可替换穿刺引导针芯插入外鞘管内,其特殊设计的末端包含双极射频电极,针芯连接配套的射频发生器后,可在针道内执行局部热消融;
半自动核心活检针:规格与外鞘管内径相匹配,通过外鞘管获取诊断所需的组织条。
工作原理:该设备将核心活检取样与针道即时热凝固封堵功能整合于同一套同轴器械内。操作过程中,利用射频能量在针道内部产生局部高温,借助组织蛋白热凝固效应和组织碳化现象,迅速封闭穿刺针道,从而预防和控制出血。
1.2.2 穿刺活检与标准化操作流程
术前准备与定位:根据影像学检查结果,规划最佳穿刺路径,避开大血管和重要组织结构,确定皮肤穿刺点和目标活检区域。
穿刺活检需严格遵守无菌操作,在超声/超声造影引导下进行,并遵循以下标准化流程:
1 建立穿刺通道:穿刺区域进行常规消毒铺巾,实施充分局部麻醉。将穿刺引导针芯插入外鞘管内,组成穿刺针组。在超声/超声造影实时引导下,操作者将穿刺针组经皮肤穿刺点沿预定路径小心推进,直至针尖抵达或紧邻目标病灶预定取样位置。确认位置无误后,拔出穿刺引导针芯,仅留置外鞘管作为工作通道。
2 核心组织取样: 通过已置入的外鞘管插入半自动核心活检针。在超声/超声造影引导下,确认活检针槽位于目标组织内后,激发活检针完成切割和取样。取出活检针,获取组织条样本。根据诊断需要和术前计划,调整外鞘管位置后,重复此步骤1~2次,以获取足够样本量。
3 针道RFA封堵:完成所有取样后,立即将RFA针芯插入外鞘管,确保其末端电极位于需要封堵的针道段内。连接RFA针芯与射频发生器,并根据预设参数(功率、时间和/或温度)启动射频能量。消融过程中,可缓慢匀速地将整个装置(外鞘管+射频针芯)回撤一定距离,实现对针道的整体消融。
4 退针与术后处理:完成穿刺针道消融后,关闭射频发生器。将整个装置(外鞘管和射频针芯)一并拔出。对穿刺点皮肤进行按压止血并覆盖无菌敷料。术后常规密切监测患者生命体征、腹部症状,观察手术即刻及术后第2天超声造影结果,以评估并发症发生情况。标准化操作流程详见图2。
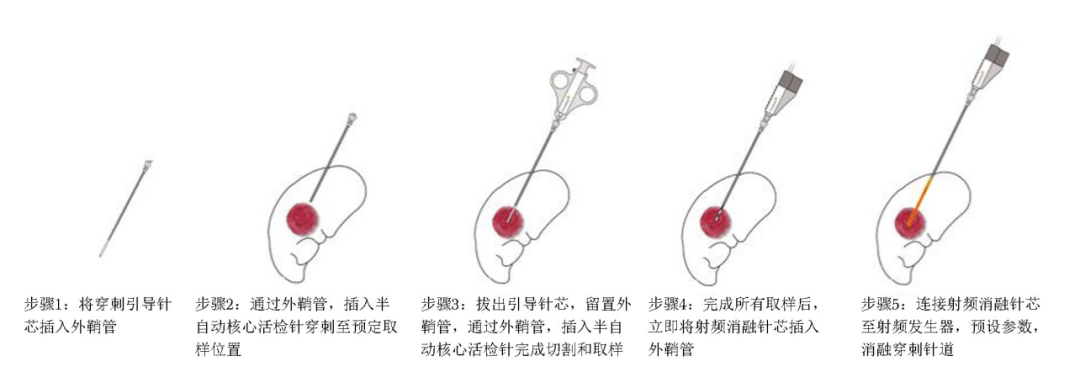
图2 射频消融针状电极标准化操作流程
1.3 观察指标与随访评估
主要观察指标:
1
患者基线特征:收集并记录研究对象的基线资料。
2
技术成功率:成功完成脾脏组织活检取样,并按照方案成功实施穿刺针道消融患者的占比。
3
组织样本诊断充分性:获取和记录术后病理诊断结果,并评估样本诊断的完整性与准确性。
4
并发症发生情况:围术期对患者进行密切观察,记录是否出现出血,术后随访期间,观察感染、针道种植转移等情况。
临床通常根据脾脏穿刺出血严重程度对出血情况进行分类。
轻度出血是指患者仅出现极轻度出血表现,如脾脏周围极少量渗血,超声及超声造影未见明显活动性出血,且出血量未见明显增多,患者生命体征稳定,一般无需特殊处理;
中度出血指出血引起了临床症状,血红蛋白有明显下降,可能需要输注1~2个单位红细胞,但通过保守治疗或少量输血能控制,患者生命体征相对稳定,无需立即侵入性止血;
重度出血表现为出血量大,导致血流动力学不稳定(休克),血红蛋白显著下降,需要大量输血(如≥2个单位红细胞),且需紧急介入治疗(如血管栓塞)或外科手术止血。
1.4 样本量估算
本研究作为一项评估新技术安全性与可行性的初步探索性研究,纳入的样本量有限,限制了研究结果的外推性,且可能无法检测到发生率较低的并发症。为向未来更大规模的验证性研究提供科学依据,本研究采用单样本优效性检验,旨在证明本研究采用的新型活检系统较传统方法在严重并发症发生率方面具有统计学优势。具体计算公式如下:
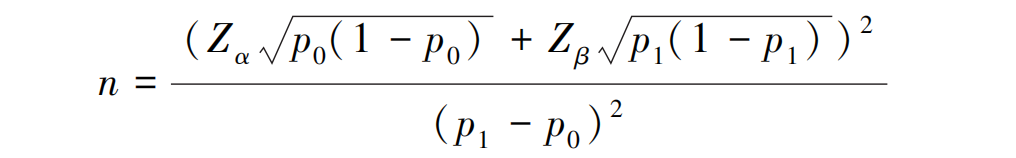
其中,将传统脾脏穿刺活检的历史严重并发症发生率(p0)设定为4%;将本研究新技术的预期严重并发症发生率(p1)设定为0.5%;检验水准α=0.05(单侧检验,Zα=1.645),检验效能(1-β)设定为80%(Zβ=0.84)。根据计算结果,为达到预期检验效能所需的样本量为119例。该计算结果从统计学上明确了本研究的探索性研究性质,并为后续开展更大规模的多中心随机对照研究提供了科学样本量计算依据。
1.5 统计学方法
采用SPSS 26以及GraphPad Prism.8.3.0软件对数据进行描述性统计分析,符合正态分布的连续变量以均数±标准差表示,分类变量以频数(百分数)表示。
2 结果
2.1 患者基线特征
本研究共纳入21例脾脏病变行穿刺活检患者,其中男性16例(76.2%),女性5例(23.8%)。年龄15~82岁,平均 (59.5±15.2)岁。
2.2 技术成功率
21例患者均成功完成穿刺活检及针道消融,技术成功率为100%,未发生穿刺路径偏移或活检失败情况。
2.3 组织样本诊断充分性
21例患者中,脾大伴弥漫性病变者7例(33.3%),脾大伴脾内多发占位者14例(66.7%)。每例患者穿刺针数2~3针。所有患者均提供足够活检组织,无严重并发症发生。最终组织样本病理学诊断:嗜血综合症2例(9.5%),弥漫性大B淋巴瘤15例(71.4%),肉芽肿性炎2例(9.5%),淋巴组织增生1例(4.8%),恶性肿瘤浸润或转移1例(4.8%)。
2.4 手术出血情况
21例患者中,3例(14.2%)出现轻微出血,未发生中重度出血事件。此外,患者术前、术后血红蛋白水平未出现明显下降。
2.5 术后随访
术后随访期间,患者未出现针道种植转移、穿刺部位感染等严重并发症,亦未发生术后长期并发症,如慢性出血、肿瘤复发等。所有患者均定期复查影像学检查(超声/CT/MRI),并进行血常规、凝血功能监测。大部分患者术后顺利恢复,未出现明显术后不适或功能障碍。
3 讨论
脾脏穿刺活检具有较高的出血风险,这一直是临床介入诊断面临的严峻挑战。文献报道,脾脏活检后严重出血发生率高于肝、肾等其他腹部实质器官[8-9]。选用细针、优化穿刺路径或术后压迫/明胶海绵填塞传统止血策略虽具有一定止血效果,但对存在凝血功能异常、脾大伴脾脏病变的患者而言,其预防严重出血的效果并不显著[10],因此临床亟需更可靠的止血技术。本研究结果初步表明,应用同轴穿刺活检与RFA系统对脾脏病变行活检的患者具有高度安全性和有效性。
本研究中,21例患者均成功完成穿刺取样及针道消融,技术成功率达100%。同时,所有病例均获取了足够病理诊断的组织样本,诊断取材成功率为100%。在安全性方面,该技术利用射频能量产生的热凝固效应(目标温度一般设置为60 ℃以上),能有效封闭针道和微小血管,在控制出血方面展现出显著优势,研究中未发生中重度出血事件,仅3例(14.3%)出现无需特殊干预的轻微出血。此外,随访期间未发现针道种植转移或其他严重并发症。以上结果证实,该技术有望解决传统脾脏活检出血风险高的核心难题,为脾脏病变诊断提供了一种更为安全的微创策略。
本研究结果与肝脏、肾脏等器官活检中应用热消融术(如RFA、微波消融)进行针道消融以减少出血的相关研究报道一致,证实热消融技术在控制实质脏器穿刺后出血方面的有效性[11]。1例46岁女性,因体检发现脾脏异常就诊。超声检查提示脾脏肿大,脾脏厚度达 4.6 cm,脾脏内可见大小约 2.3 cm×1.7 cm的低回声占位性病变。通过外鞘管插入半自动核心活检针,穿刺至脾脏占位前端,拔出引导针芯,留置外鞘管,通过外鞘管插入半自动核心活检针,对肿块进行穿刺活检。完成所有取样后,立即将射频消融针芯插入外鞘管,将射频消融针芯连接至射频发生器,消融功率设置为40 W,消融穿刺针道,消融针道后即刻进行超声造影,未见明显造影剂溢出,提示穿刺针道未见明显出血(图3)。
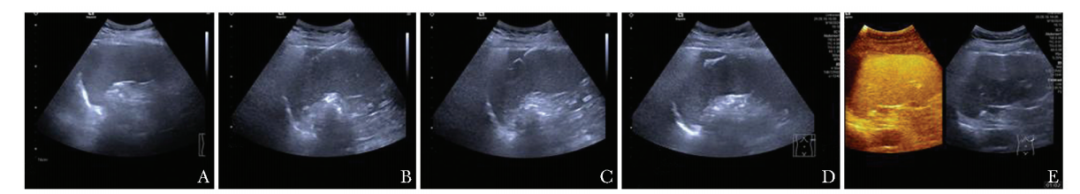
图3 1例46岁女性脾脏病变患者穿刺活检过程
A.超声定位肿大脾脏及病灶位置;B.通过外鞘管,插入半自动核心活检针穿刺至脾脏占位前端;C.激发活检针采集脾脏病变组织样本;D.将圆头内芯针电极与同轴电极针匹配,使用双极针进行针道消融止血;E.即刻超声造影显示未见明显出血
本研究初步评估结果表明,采用同轴穿刺活检与RFA系统对脾脏进行活检解决传统脾脏活检出血风险高的核心难题,为需明确诊断的脾脏病变患者提供了一种主动、高效的解决方案,有效填补了临床实践的空白。
该技术核心创新点与优势在于 “诊疗一体化”设计与“主动热凝固止血”机制,将组织获取与即时止血两个关键环节整合于单次操作,显著优于传统活检后依赖生理凝血或外部材料填塞的被动方式。射频热能可快速凝固和封闭针道组织及血管,在凝固过程中形成的碳化层可充当物理屏障,进而潜在降低肿瘤细胞沿针道播散种植的风险。在脾脏活检中针道种植较为罕见,且本研究随访期内并未观察到此类事件发生,但对于恶性肿瘤患者而言,预防肿瘤种植的潜在获益具有重要意义。若该技术未来应用于肝肺等针道种植风险更高的器官,其优势将更加凸显。这种“边取边凝”模式为处理富血供器官或合并凝血功能障碍患者的活检需求开辟了更为安全的技术路径。
随着微创介入术与精准医疗领域的不断推进,本研究采用同轴穿刺活检与RFA系统止血取得的初步成功经验不仅为其在脾脏活检中的进一步应用提供有力支撑,也为开发集成诊断取样与其他即时并发症处理功能(如封堵、药物输注等)的新型介入器械提供了有益启示。
作为一项初步评估,本研究亦存在一定局限性:首先,本研究为单臂、非对照试验设计,无法与传统活检方法或其他止血策略(如同轴技术下使用明胶海绵、弹簧圈等)进行疗效比较;其次,样本量有限,限制了结果的外推性,且可能无法检测到发生率较低的并发症;再次,随访时间较短,无法评估远期并发症(如迟发性出血、热损伤相关的邻近器官影响)以及肿瘤学结局(特别是针道种植的长期风险);最后,从直接成本层面考量,同轴穿刺活检与RFA系统因需使用RFA设备及专用针具,单次操作的器械成本高于传统细针穿刺或仅用止血材料的方法。
然而,传统方法虽耗材费用较低,但预防严重出血的效果欠佳,一旦出现出血并发症,后续处理(如输血、急诊介入栓塞或手术)费用高昂,同时会导致住院时间延长。因此,虽然本研究所用系统初始成本较高,但其能显著降低严重并发症发生率,减少并发症相关治疗费用,缩短住院时间,在整体医疗经济学上体现出潜在优势。未来研究方向应聚焦于开展设计严谨的大样本、多中心随机对照试验,将同轴穿刺活检与射频消融系统纳入不同病理类型、出血风险分层的患者群体,并进行长期随访观察和成本效益分析。
综上所述,本研究提供的初步临床数据与评估表明,同轴穿刺活检与射频消融系统为脾脏穿刺活检患者群体提供了一种安全、有效的新诊疗选择。该系统可整合取材与热凝固止血功能,显著降低操作相关出血风险,未来有望在临床得到更广泛应用与深入研究。
参考文献
[1]Madoff D C, Denys A, Wallace M J, et al. Splenic arterial interventions: anatomy, indications, technical considerations, and potential complications[J]. Radiographics, 2005, 25(Suppl 1): S191-S211.
[2]田江克, 谢霞, 武荣, 等. 超声造影引导下注射明胶基止血剂治疗犬脾脏创伤的疗效[J]. 中华医学超声杂志(电子版), 2013, 10(9): 769-775.
[3]Olson M C, Atwell T D, Harmsen W S, et al. Safety and accuracy of percutaneous image-guided core biopsy of the spleen[J]. Am J Roentgenol, 2016, 206(3): 655-659.
[4]Schiavon L H O, Tyng C J, Travesso D J, et al. Computed tomography-guided percutaneous biopsy of abdominal lesions: indications, techniques, results, and complications[J]. Radiol Bras, 2018, 51(3): 141-146.
[5]Barat M, Hoeffel C, Aissaoui M, et al. Focal splenic lesions: Imaging spectrum of diseases on CT, MRI and PET/CT[J]. Diagn Interv Imag, 2021, 102(9): 501-513.
[6]Alaggio R, Amador C, Anagnostopoulos I, et al. The 5th edition of the World Health Organization Classification of Haematolymphoid Tumours: Lymphoid Neoplasms[J]. Leukemia, 2022, 36(7): 1720-1748.
[7]Gupta S, Wallace M J, Cardella J F, et al. Quality improvement guidelines for percutaneous needle biopsy[J]. J Vasc Interv Radiol, 2010, 21(7): 969-975.
[8]Zhu S, Li J, Guan W, et al. Clinical application of radiofrequency ablation-assisted coaxial trocar biopsies for pulmonary nodules at a high risk of bleeding[J]. J Cancer Res Ther, 2023, 19(4): 972-977.
[9]Lu M D, Xu H X, Xie X Y, et al. Percutaneous microwave and radiofrequency ablation for hepatocellular carcinoma: a retrospective comparative study[J]. J Gastroenterol, 2005, 40(11): 1054-1060.
[10]Wang H Y, Bao H W, Yue L, et al. A novel biopsy method based on bipolar radiofrequency biopsy needles[J]. Front Oncol, 2022, 12: 838667.
[11]Adnan A, Sheth R A. Image-guided percutaneous biopsy of the liver[J]. Tech Vasc Interv Radiol, 2021, 24(4): 100773.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)