首页 > 医疗资讯/ 正文
摘 要
目的 对重度创伤性颅脑损伤患者术后影响预后的因素进行分析。
方法 回顾性分析我院在2020年1月至2024年5月治疗的重度颅脑损伤患者的临床资料,根据患者术后3个月格拉斯哥预后评分(Glasgow outcome scale,GOS),分为预后良好组和预后不良组。比较两组患者的基本资料,分析导致术后早期预后不良的影响因素。
结果 共有140例患者纳入研究,预后良好组58例,预后不良组82例。两组入院时格拉斯哥昏迷评分(Glasgow coma scale,GCS)(t=14.137,P=0.002)、Rotterdam CT评分(t=18.516,P=0.007)、弥漫性血管内凝血(disseminated intravascular coagulation,DIC)评分(t=10.428,P=0.008)差异有统计学意义(P<0.05)。多因素分析结果表明,入院时GCS评分低(OR=0.273,95%CI:0.126~0.671,P=0.008)、Rotterdam CT 评分高(OR=1.804,95%CI:1.026~4.557,P=0.018)、DIC评分高(OR=1.648,95%CI:1.173~2.424,P=0.020)是术后预后不良的重要危险因素。
结论 重度创伤性颅脑损伤患者术后预后不良与入院时GCS评分、Rotterdam CT评分、DIC评分有关,入院时GCS评分低、Rotterdam CT 评分高、DIC评分高的重度创伤性颅脑损伤患者术后预后不良的发生率显著提高。
关键词
重度颅脑损伤;GCS评分;Rotterdam;CT;评分;DIC评分;凝血功能;预后;影响因素
重度创伤性颅脑损伤是神经外科常见的危重急症之一,随着全球工业化和经济水平的发展,重度颅脑损伤的发病例数呈逐年上升的趋势,是世界范围内致死、致残的重要原因之一[1]。目前全球每年的颅脑损伤患者数量5000余万,其中重度颅脑损伤的死亡率超过40%,给广大家庭带来非常大的经济负担[2]。如何早期判断重度颅脑损伤患者的预后目前尚无统一的标准,有研究证实患者入院时意识障碍程度及部分血清学检验结果可能与患者预后不佳相关[3]。本研究回顾性分析镇江市第一人民医院在2020年1月至2024年5月期间收治的140例重度颅脑损伤患者的临床资料,探讨影响重度颅脑损伤患者预后的相关因素,为早期判断预后和制定后续个体化的治疗方案提供参考依据。
1 资料与方法
1.1 研究对象 将镇江市第一人民医院在2020年1月至2024年5月期间收治的重度颅脑损伤患者作为研究对象。纳入标准:①入院时格拉斯哥昏迷评分(Glasgow coma scale,GCS)3~8分;②伤后至入院时间≤48 h;③CT检查提示硬膜外血肿厚度>1 cm或硬膜下血肿>30 mL,中线偏移>5 mm;④在我院顺利完成颅内血肿清除手术。排除标准:①伴有严重多发伤;②存在严重基础疾病;③入院后72 h内死亡;④临床资料不全。本研究已通过镇江市第一人民医院伦理委员会批准(审批号:K-202400140-W)。
1.2 资料收集 通过医院电子病历系统收集患者的年龄、性别、有无高血压、有无糖尿病、有无服用抗凝、抗血小板药物、入院时GCS评分、Rotterdam CT评分、有无低血压、有无颅底骨折、瞳孔情况、弥漫性血管内凝血(disseminated intravascular coagulation,DIC)评分、受伤至手术的时间、手术时间、术中补液量、术中出血量。接受抗凝或抗血小板药物治疗3个月以上的患者,判定为服用抗凝药物或抗血小板药物。患者术前收缩压曾低于70 mmHg以下,则判定为低血压.术前患者有典型的熊猫眼、脑脊液鼻漏或耳漏的症状,则判定为颅底骨折。意识障碍评分采用GCS量表,总分为3~15分,分值越低提示病情越严重[4]。Rotterdam CT评分的具体计算方法为:基底池正常0分,受压1分,消失2分;中线移位小于5 mm 0分,大于5 mm 1分;无硬膜外血肿或占位性病灶0分,有硬膜外血肿或占位性病灶1分;无脑室或蛛网膜下腔出血0分,有脑室或蛛网膜下腔出血1分,最后总分加上 1 分,最高为 6 分。DIC评分根据国际血栓与止血学会颁布的标准[5],凝血酶原时间延长3 s以上为1分,延长6 s以上为2分;纤维蛋白原小于1 g/L为1分;D-二聚体中度升高为2分,显著升高为3分;血小板小于100 g/L为1分,小于50 g/L为2分;总分为各项相加。
根据患者术后3个月格拉斯哥预后评分标准(Glasgow outcome scale,GOS)作为判断早期预后的依据,评分 1~3 分判定为预后不良,4~5 分判定为预后良好[6]。
1.3 统计学方法 采用SPSS 26.0处理数据,使用Shapiro-Wilk法对数据进行正态性检验,年龄、GCS评分、Rotterdam CT 评分、DIC评分、受伤至手术的时间、手术时间、术中出血量等计量资料以均数±标准差描述,组间比较采用t 检验。术中补液量为偏态分布资料,采用Mann-Whitney U检验。计数资料以例表示,性别、高血压、糖尿病、服用抗凝药物、服用抗血小板药物、颅底骨折、低血压、瞳孔情况等分类资料组间比较采用χ2检验。采用logistic回归进行多因素分析,纳入组间有统计学意义的变量,采用逐步回归法筛选变量,双侧检验,检验水准α=0.05。
2 结果
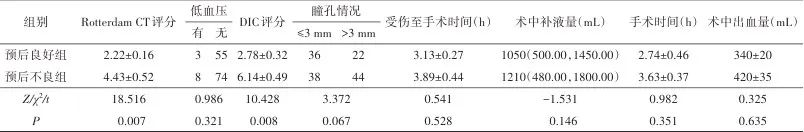
2.1 一般资料 共纳入140例重度颅脑损伤的患者,根据术后GOS评分标准分为两组,其中预后良好组58例,预后不良组82例。单因素分析结果表明年龄、性别、高血压、糖尿病、服用抗凝药物、服用抗血小板药物、颅底骨折、低血压、瞳孔情况、受伤至手术的时间、手术时间、术中补液量、术中出血量差异无统计学意义(P>0.05),而入院时GCS评分(t=14.137,P=0.002)、Rotterdam CT评分(t=18.516,P=0.007)、DIC评分(t=10.428,P=0.008)差异有统计学意义(P<0.05)。见表1。
表1 重度颅脑损伤患者临床特征及术后预后不良的单因素分析Tab.1 Clinical features and factor analysis of poor postoperative prognosis in patients with severe traumatic brain injury
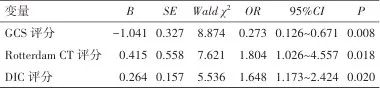
2.2 重度颅脑损伤患者术后预后不良的多因素分析 将GCS评分、Rotterdam CT 评分、DIC评分纳入logistic 回归方程中,分析结果表明,入院时GCS评分低(OR=0.273,95%CI:0.126~0.671,P=0.008)、Rotterdam CT 评分高(OR=1.804,95%CI:1.026~4.557,P=0.018)、DIC评分高(OR=1.648,95%CI:1.173~2.424,P=0.020)是术后预后不良的重要危险因素。见表2。
表2 重度颅脑损伤患者术后早期预后不良的多因素分析Tab.2 Results of multivariate analysis of poor early postoperative prognosis in patients with severe traumatic brain injury
3 讨论
重度创伤性颅脑损伤具有致残率高、致死率高的特点,需要医生早期对高危患者做出分辨,并采取个体化的治疗方法,改善患者的预后。本研究结果表明,GCS评分高、Rotterdam CT评分低、DIC评分低的患者往往会有更好的预后,而患者年龄、瞳孔情况、有无低血压、手术时间等因素与预后差异没有统计学意义。以往的研究未曾将这3种不同维度的评估体系结合起来,因此我们尝试分析这些患者的临床特征,找出有意义的影响因素,为重度颅脑损伤预后的评估提供参考依据。
国内外已有很多研究证实,GCS评分目前是临床中意识评估的重要参考工具,也在一定程度上反映出患者的受伤程度。研究表明,GCS评分高的患者脑组织损伤程度往往较轻,颅内压不高,对颅内主要动脉的压迫不严重,脑组织仍存在正常的血供,意识恢复的概率会明显提高[7-8],反之GCS评分低的患者伤情往往较重,常伴有脑疝的表现,颅内压显著增高,神经功能严重受损,即使给予手术治疗,这些患者的疗效也普遍较差。因此GCS评分可作为一项重要的预后评估的指标[9]。本研究通过分析患者的临床资料发现,入院时GCS评分会影响重度颅脑损伤患者的预后,并可作为一项重要的危险因素。
颅脑损伤患者会出现低血压,甚至休克的表现,说明颅内压力已达到较高的程度,神经中枢受到压迫,此时的伤情已十分严重,这种患者往往预后较差。有关研究表明[10],低血压不仅会降低全身器官的供血,造成多器官功能障碍,同时还降低组织代谢物质的排泄,进一步加重全身脏器的损害,对患者的预后产生严重的影响。对于这些患者我们应及时查找原因,快速纠正低血压,恢复组织灌注,改善脑组织缺血、血氧,有手术指征的患者应及时给予手术治疗。本次研究对象为术后生存期大于72 h的患者,很多出现低血压的患者术后72 h内已死亡,未能纳入研究对象中,故低血压患者的样本量较少,相信随着研究设计的优化、样本量的增多,低血压这一因素对于重度颅脑损伤术后患者预后的预测价值会逐渐显露出来。观察瞳孔的变化情况是神经外科医生常用的诊疗手段,瞳孔突然放大常是颅内压迅速增高的表现,但有些颅脑损伤的患者合并有视神经或动眼神经损伤,也会出现瞳孔散大,这种情况下瞳孔的变化就无法反映出患者真实的病情,因此本研究纳入的病例未得出有统计学意义的结果。
Rotterdam CT评分是由MASS等[11]在2005年提出的一个新的CT分类方法,根据是否有脑池受压、创伤性蛛网膜下腔出血、脑室出血、中线移位>5 mm和硬膜外血肿来进行综合评分,分值越小预后越好,在临床中作为一种客观的评估病情的手段已被广泛应用。KHAKI等[12]认为Rotterdam CT评分对重度颅脑损伤患者的预后预测具有很高的价值。THELIN等[13]的多中心前瞻性研究表明,Rotterdam CT评分为中重度颅脑损伤预后不良的预测因子。有研究结果表明,Rotterdam CT评分对于重度颅脑损伤患者的预后具有较好的预测价值[14-15]。CT检查对于急性颅脑损伤的预后具有较高价值,同时也得到了多数同行的认可[16],通过CT检查可以客观的了解患者颅内情况,尤其对于醉酒患者或镇静状态的患者,医护人员对伤情的评估存在着一些偏差,无法反映患者真实的伤情程度,而Rotterdam CT评分相对客观、准确,结合Rotterdam CT评分的结果可以更好对此类患者的病情进行评估。本研究logistic多因素分析的结果也表明Rotterdam CT评分是颅脑损伤患者术后预后不良的重要影响因素。
有研究[17]指出32.7%重度的颅脑损伤患者会出现严重的凝血功能异常,表现为进行性出血性损伤,显著增加死亡率和预后不良。弥漫性血管内凝血是一种严重的凝血功能异常,表现为血管内凝血功能激活和纤维蛋白沉着,重度颅脑损伤常为其发生的诱因之一。有研究表明,凝血酶原时间延长与重度颅内损伤患者死亡相关[18],相关机制可能为重度颅脑损伤后患者的内环境会出现严重紊乱,血小板在受损的血管内皮发生聚集,血液处于高凝状态,血小板大量减少,同时血小板和凝血因子的功能出现异常、内源性凝血途径遭到破坏,几种因素相互作用,最终出现严重凝血功能紊乱[19]。周良辅认为重度颅脑损伤的患者常会发生凝血功能障碍,是导致进展性颅内出血的重要危险因素,从而影响患者的预后[20]。重度颅脑损伤后,其他凝血指标也能够预测患者的预后,但DIC评分预测得更加准确和可靠[21-22]。袁强等[23]研究结果表明,DIC评分纳入的指标包含凝血酶原时间、纤维蛋白原、D-二聚体、血小板,能更准确的反应患者的凝血功能,对于重度颅脑损伤患者的预后预测具有重要价值。本研究结果表明DIC评分和重度颅脑损伤术后患者预后不良有相关性,并可以作为预后不良的重要影响因素,得出了与之相同的结论。
综上所述,本研究对重度颅脑损伤患者术后早期预后不良的影响因素进行了分析,得出的结果表明这GCS评分、Rotterdam CT评分、DIC评分是重度颅脑损伤患者术后早期预后不良的重要危险因素。在我们平时工作中,临床医生比较容易和快速获得这3种不同维度的评分,能够及时对重度颅脑损伤患者的伤情做出全面、客观、准确的判断,对于判定结果为预后不良的患者,应迅速启动院内重度脑损伤救治流程,协调相关科室的术前准备工作,联系输血科备足血制品,做好术中突发情况的准备工作。加强和患者家属对于病情的沟通,充分告知患者的预后,取得家属的理解,减少医患矛盾,并尽早制定准确、合理的诊疗措施,改善患者的预后。本研究为单中心回顾性分析,存在一些不足之处,总体患者病例数偏少,有些影响因素样本量不足,部分有价值的影响因素由于数据缺失未能纳入研究,后期需通过增加病例数、更加全面地收集临床数据,进行下一步研究。
参考文献:
1. 刘昊东, 武泽军, 赵君爽, 等. 骨髓间充质干细胞来源外泌体对创伤性颅脑损伤的影响研究进展[J]. 中国神经精神疾病杂志, 2023, 49(11): 700-704.
2. CAPIZZI A, WOO J, VERDUZCO-GUTIERREZ M.Traumatic brain injury: An Overview of Epidemiology, Pathophysiology, and Medical Management[J]. Med Clin North Am, 2020, 104(2): 213-238.
3. JIANG J Y, GAO GY, FENG J F, et al.traumatic brain injury in China[J]. Lancet Neurol, 2019, 18(3): 286-295.
4. DIJKLAND SA, FOKS K A, POLINDER S, et al.Prognosis in Moderate and Severe traumatic brain injury: A Systematic Review of Contemporary Models and Validation Studies[J]. J Neurotrauma, 2020, 37(1): 1-13.
5. WADA H, GABAZZA E C, ASAURA H, et al.Comparison of diagnostic criteria for disseminated intravascular coagulation (DIC): diagnostic criteria of the International Society of Thrombosis and Hemostasis and of the Japanese Ministry of Health and Welfare for overt DIC[J]. Am J Hematol, 2003, 74(1): 17-22.
6. 周挺, 董明俊.重度外伤性颅脑损伤早期预后不良危险因素分析[J]. 浙江创伤外科, 2023, 28(8): 1543-1546.
7. TOLESUC R S, ZORILĂ M V, ZĂVOI R E,et al.Correlations Between the Glasgow Score and the Survival Period in Patients with Severe Traumatic Brain Injury[J]. Curr Health Sci J, 2020, 46(4): 412-419.
8. 王艳军, 李青华, 庄禹童, 等.重型创伤性脑损伤后慢性意识障碍患者术后短期意识水平改善的相关影响因素[J]. 中华创伤杂志, 2023, 39(4): 324-330.
9. 任杰, 朱飞奇.重型颅脑损伤合并多发伤患者早期死亡的决策树模型研究[J]. 中国急救医学, 2022, 42(4): 343-346.
10. 冯爱平, 江涛, 刘伦波, 等.早期预后良好的重度颅脑损伤患者的临床特征及预后相关因素研究[J]. 中国急救医学, 2019, 39(6): 559-563.
11. MAAS A I, HUKKELHOVEN CW, MARSHALL L F, et al.Prediction of outcome in traumatic brain injury with computed tomographic characteristics: a comparison between the computed tomographic classification and combinations of computed tomographic predictors[J]. Neurosurgery, 2005, 57(6): 1173-1182; discussion 1173-1182.
12. KHAKI D, IETANEN V, CORELL A, et al. Selection of CT variables and prognostic models for outcome prediction in patients with traumatic brain injury[J]. Scand J Trauma Resusc Emerg Med, 2021, 29(1): 94.
13. THELIN E P, NElSON D W, VEHVIĂINEN J, et al.Evaluation of novel computerized tomography scoring systems in human traumatic brain injury: An observational, multicenter study[J]. PLoS Med, 2017, 14(8): e1002368.
14. 陈迁, 孙兆瑞, 廖浩宇, 等.不同CT评分对中重度颅脑损伤患者预后的价值[J]. 医学研究与战创伤救治, 2023, 36(6): 579-584.
15. 汪静静, 孟庆宇, 孙艳秋.鹿特丹CT评分用于评估颅脑损伤患者预后[J]. 中国介入影像与治疗学, 2022, 19(1): 36-39.
16. NAEIMI A, AGHAGANIAN S, JAFARABABY K, et al.Prognostic value of computed tomography and magnetic resonance imaging findings in acute traumatic brain injury in prediction of poor neurological outcome and mortality: a systematic review and meta-analysis[J]. Neurosurg Rev, 2024, 47(1): 837.
17. KALOGIROU E, VOULGARIS S, ALEXIOU G A.Coagulopathy prediction in traumatic brain injury[J]. Adv Clin Chem, 2025, 126: 199-231.
18. MACLEOD J B, LYNN M, MCKENNEY M G,et al.Early coagulopathy predicts mortality in trauma[J]. J Trauma, 2003, 55(1): 39-44.
19. 杜海平, 李刚.急性外伤性硬脑膜下血肿快速消散的病理、机制及相关因素探讨[J].创伤外科杂志, 2020, 22(4): 264-266.
20. 周良辅.重视颅脑创伤后凝血功能障碍的诊断和治疗[J].中华创伤杂志, 2015, 31(8): 673-675.
21. 王帆, 黄清, 陈祥荣, 等.颅脑损伤远隔血肿部位迟发性脑梗死预后影响因素分析[J]. 中国神经精神疾病杂志, 2021, 47(11): 641-646.
22. GREFENEDER J, KRYCHTIKU KA, BUCHTELE N, et al.The ISTH DIC score predicts outcome in non-septic patients admitted to a cardiovascular intensive care unit[J]. Eur J Intern Med, 2020, 79: 37-42.
23. 袁强, 吴惺, 卢香琼, 等.弥漫性血管内凝血评分对创伤性脑损伤患者预后的预测价值[J]. 中华创伤杂志, 2015, 31(8): 676-680.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)