首页 > 医疗资讯/ 正文
近年来,随着对肝细胞癌(HCC)组织结构和免疫微环境理解的不断加深,免疫治疗已逐步成为HCC研究的热点方向。免疫检查点抑制剂(ICIs)以及过继性细胞治疗(ACT)等策略的兴起,为HCC治疗带来了全新的希望。ACT是一种具有前景的治疗方式,通过体外激活并扩增患者自身或供体来源的免疫效应细胞,再将其输注回体内,用于治疗感染性疾病、自身免疫病和各类恶性肿瘤。随着细胞免疫疗法的不断发展,其在多种肿瘤治疗中展现出良好前景,已被广泛用于临床实践。特别是CAR-T细胞在实体瘤治疗中的探索不断深入,CAR-NK细胞也显示出独特优势,使得研究者开始将目光聚焦于新型的CAR-M(嵌合抗原受体巨噬细胞)疗法。目前,CAR-M细胞的来源主要包括外周血单个核细胞(PBMC)、诱导性多能干细胞(iPSC)以及人单核细胞白血病系THP-1,相关研究已在多种癌症模型中展开尝试。
肝脏是一个高血流灌注的器官,天然富含先天免疫细胞,特别是各种类型的巨噬细胞。包括来源于单核细胞的募集型巨噬细胞(MDMs)以及肝内常驻的组织巨噬细胞(TRMs),它们在介导吞噬、清除病原体以及抑制肿瘤在肝内扩散中发挥重要作用。因此,靶向巨噬细胞的细胞治疗策略在HCC中展现出巨大的应用潜力。然而,当前巨噬细胞治疗仍面临两项主要挑战:其一是细胞数量受限,由于巨噬细胞本身不具备显著的扩增能力,患者可供回输的细胞数量较少,影响治疗效能;其二是巨噬细胞的吞噬功能相对有限,提升其吞噬活性仍是亟需攻克的技术瓶颈。
2025年5月,北京大学三〇二临床医学院李爽博士作为第一作者,陆荫英教授为通讯作者,在《Gut》期刊发表了一项研究,系统探讨了NLRP6在肝癌相关巨噬细胞功能中的作用。研究团队通过患者组织的免疫荧光染色,结合多种HCC小鼠模型(包括自发性、原位种植及皮下移植模型),在野生型、Nlrp6基因敲除小鼠及巨噬细胞特异性敲除模型中,开展了转录组测序、流式细胞术和组织病理学分析,并利用肿瘤细胞和荧光微粒评估了巨噬细胞的吞噬能力。进一步结合多组学技术、免疫共沉淀质谱、Western blot和Co-IP实验,揭示了NLRP6的PYD结构域与E-Syt1的SMP结构域之间的相互作用。结果表明,NLRP6通过该分子互作轴抑制了巨噬细胞的浸润及吞噬功能,进而促进HCC的发生与发展。此外,研究提出将Nlrp6缺失型巨噬细胞进行过继转移,有望增强其抗肿瘤活性,从而成为一种潜在的HCC治疗策略。
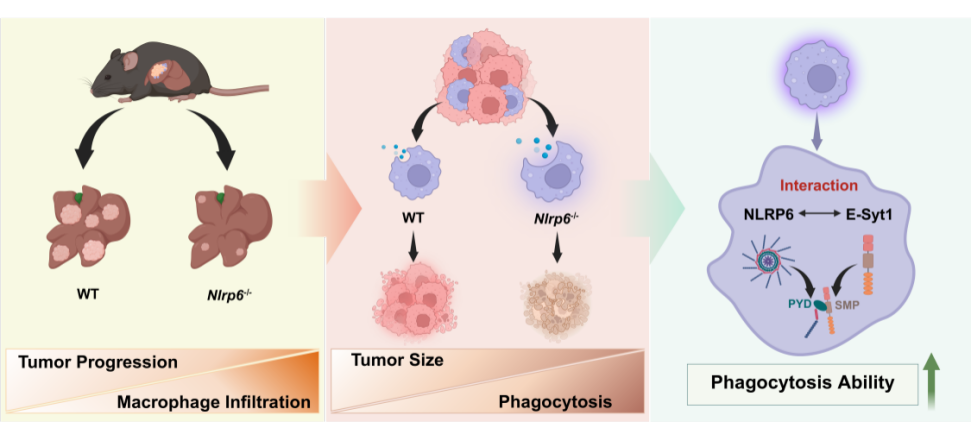
综上所述,本研究旨在揭示NLRP6通过与E-Syt1的相互作用,抑制巨噬细胞浸润及吞噬活性,从而促进HCC进展的作用机制。其具体作用位点为NLRP6的PYD结构域与E-Syt1的SMP结构域。在治疗方面NLRP6缺失型(Nlrp6-/-)巨噬细胞进行过继转移显著抑制了体内肿瘤生长,为靶向巨噬细胞开发新型HCC免疫治疗策略提供了新的方向。
6月15日,法国国家健康与医学研究院肝癌专家Angelique Gougelet教授在Gut撰写专文点评(DOI: 10.1136/gutjnl-2025-335795),高度肯定了本研究价值,强调NLRP6/E-Syt1轴在肿瘤免疫治疗中的潜力,同时呼吁进一步机制探索和临床前安全性评估。该研究为HCC及其他实体瘤的巨噬细胞疗法提供了新思路,未来需跨学科合作以解决转化医学中的复杂性。
摘自:LI S, FU Y, JIA X, et al. NLRP6 deficiency enhances macrophage-mediated phagocytosis via E-Syt1 to inhibit hepatocellular carcinoma progression[J]. Gut, 2025. DOI: 10.1136/gutjnl-2024-334448. [Epub ahead of print].

- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)