首页 > 医疗资讯/ 正文
纳米催化剂在生物医学领域具有广泛的应用前景,尤其是在调节生物微环境和刺激治疗效果方面。然而,传统纳米催化剂存在金属原子利用率低和催化活性不足的问题,限制了其在生物医学中的应用。近年来,单金属原子催化剂(SACs)因其明确的结构和最大化的原子利用率而受到关注。这些催化剂不仅具有更高的催化活性和选择性,还能够通过改变金属中心和配位结构来精确调节其催化性能。此外,SACs在肿瘤治疗中展现出巨大潜力,能够通过类过氧化物酶活性在肿瘤微环境中生成活性氧物种,从而破坏细胞的氧化还原平衡并诱导细胞死亡。因此,开发高效的SACs并将其应用于生物医学领域具有重要意义。
这篇文章的核心内容是关于单金属原子催化剂(SACs)的制备、表征及其在生物医学应用中的研究。文章详细介绍了基于氮掺杂碳载体(N-C)的SACs的设计、制备方法、表面修饰策略、物理化学和生物学特性表征,以及它们在肿瘤治疗中的潜在应用。这些SACs因其明确的结构和最大化的原子利用率而展现出更高的催化活性和选择性,使其在生物医学领域具有广阔的应用前景。相关内容以“Preparation and biomedical applications of single-metal atom catalysts”为题由南洋理工大学赵彦利、Liu Yang等人研究团队发表在《Nature Protocols》上。

【主要内容】
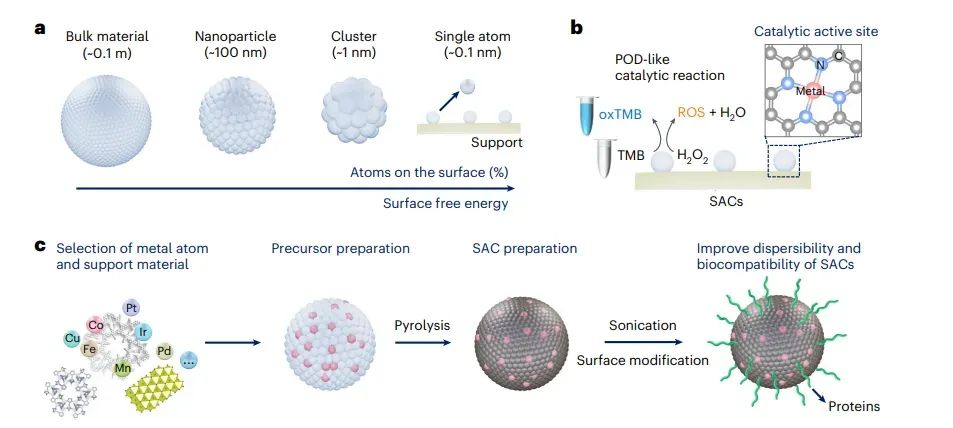
图1 SACs的结构和合成过程示意图
图中说明了SACs通过将单金属原子嵌入氮掺杂的碳载体中,能够显著提高表面原子比例和表面自由能,从而增强催化活性。合成过程包括前驱体的制备、热解以及表面修饰等步骤,最终形成具有特定配位结构的SACs。此外,图中还展示了SACs在肿瘤微环境中通过类过氧化物酶活性产生活性氧物种(ROS),从而实现对肿瘤的治疗效果。
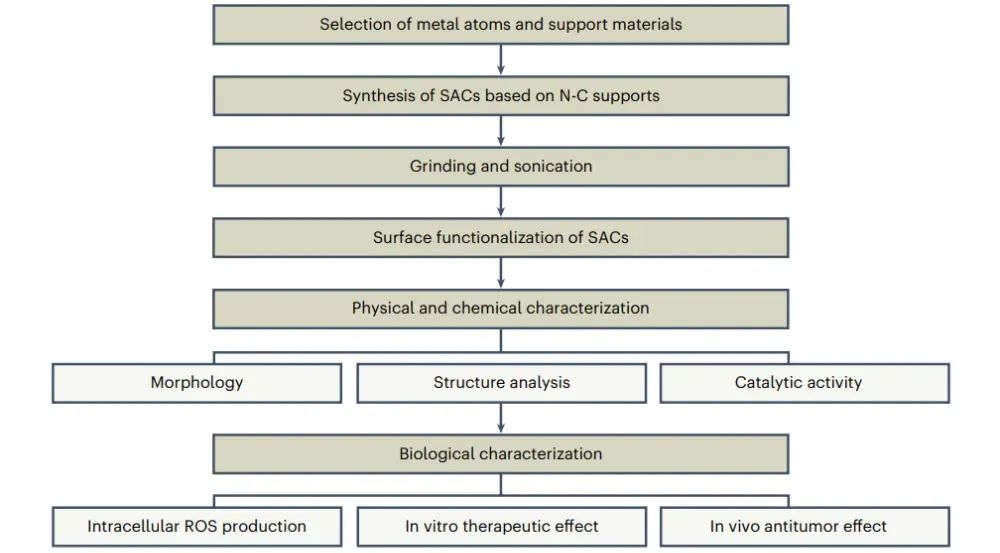
图2 协议流程图
图中以流程图的形式概述了SACs的制备和生物医学应用的全过程。流程包括金属原子和载体材料的选择、SACs的合成、表面修饰、物理化学特性表征以及生物学特性评估等步骤。图中还强调了在实验过程中需要注意的关键点,如高温热解条件的控制、表面修饰对分散性和生物相容性的影响,以及在细胞和动物模型中评估SACs的治疗效果。
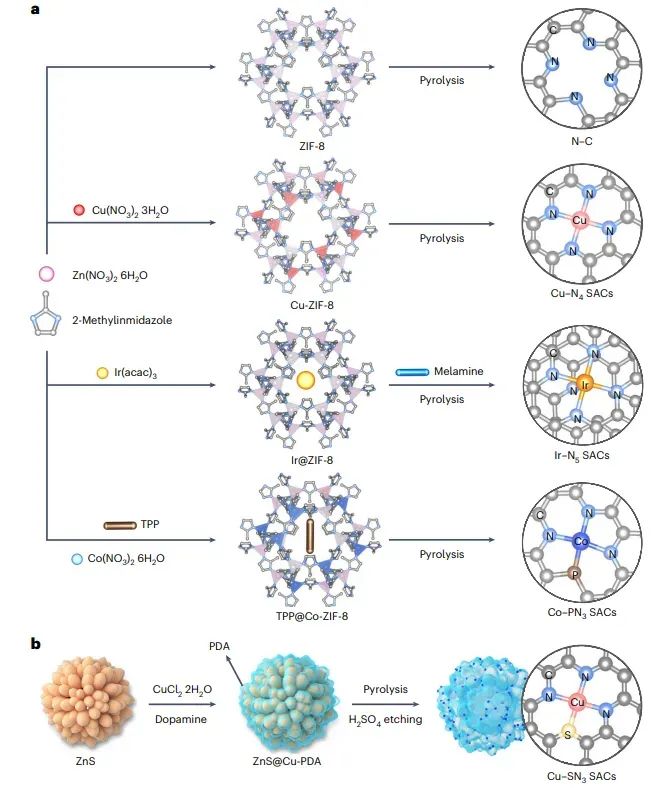
图3 SACs的合成方案
图中通过化学结构式和反应步骤清晰地说明了从金属盐和有机配体出发,经过配位、热解和后处理等步骤,最终形成具有不同配位结构的SACs(如Cu-N4、Cu-SN3、Ir-N5和Co-PN3)。此外,图中还标注了关键的反应条件,如温度、时间和气氛,为实验操作提供了具体指导。
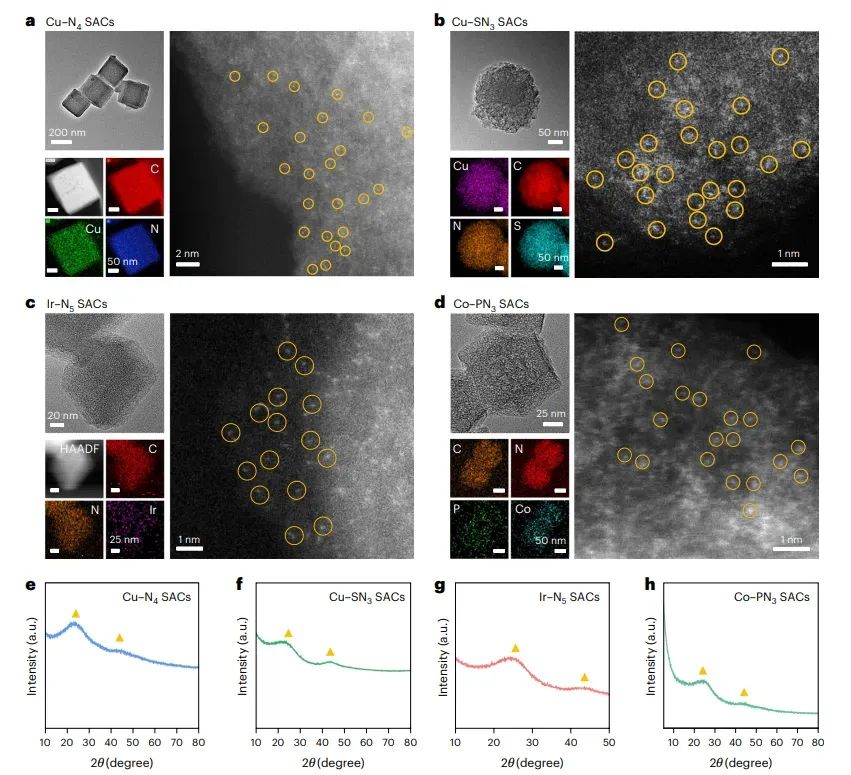
图4 SACs的TEM图像和XRD图谱
图中展示了四种SACs(Cu-N4、Cu-SN3、Ir-N5和Co-PN3)的透射电子显微镜(TEM)图像和X射线衍射(XRD)图谱。TEM图像显示了SACs的均匀分散性和规则形态,没有明显的金属聚集,证明了单金属原子的成功锚定。XRD图谱则表明,经过热解处理后,前驱体的特征峰消失,取而代之的是石墨碳的宽峰,且未检测到金属的晶态峰,进一步证实了金属原子以单原子形式存在。
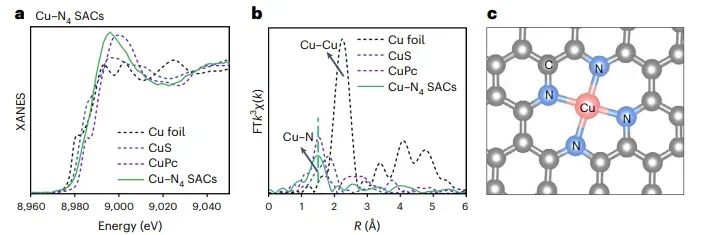
图5 Cu-N4 SACs的XAS表征
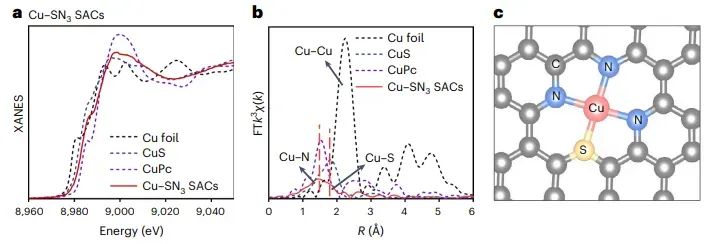
图6 Cu-SN3 SACs的XAS表征
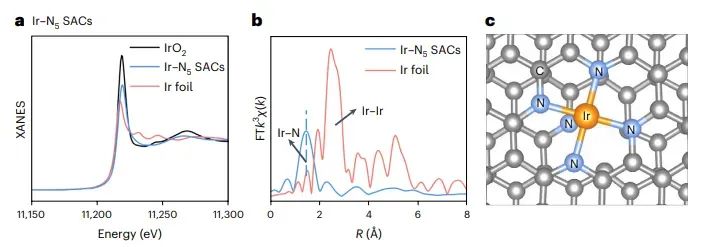
图7 Ir-N5 SACs的XAS表征
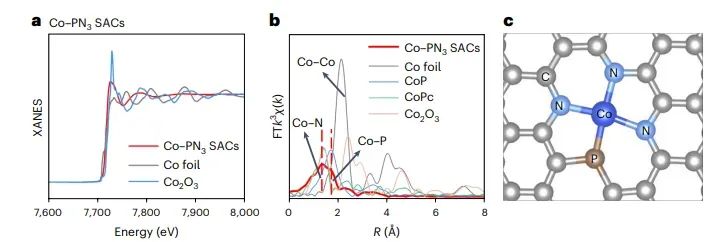
图8 Co-PN3 SACs的XAS表征
图5-图8分别展示了Cu-N4、Cu-SN3、Ir-N5和Co-PN3 SACs的X射线吸收光谱(XAS)表征结果。XAS分析包括X射线吸收近边结构(XANES)和扩展X射线吸收精细结构(EXAFS)。这些图谱揭示了金属原子的价态、配位数和配位原子类型等信息。例如,Cu-N4 SACs的FT-EXAFS谱图显示了Cu与N原子的配位,而Cu-SN3 SACs则额外显示出Cu与S原子的配位,表明了配位结构的成功调控。
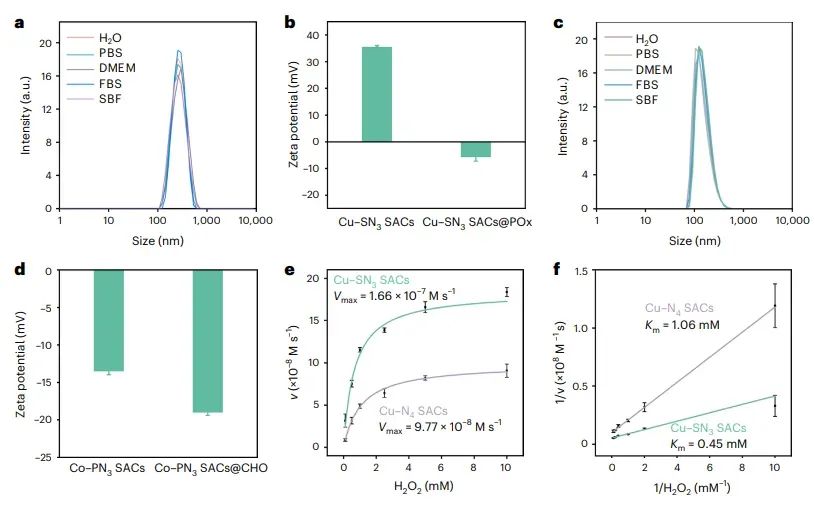
图9 SACs的DLS测量和催化性能测试
图中展示了SACs的动态光散射(DLS)测量结果和类过氧化物酶活性测试。DLS结果显示,经过蛋白质修饰后的SACs在水溶液中具有更好的分散性,且表面电荷更负,表明蛋白质成功修饰在SACs表面。催化性能测试则通过TMB显色反应评估了SACs的类过氧化物酶活性,发现Cu-SN3 SACs相较于Cu-N4 SACs具有更高的催化活性,表明配位结构的调控能够显著影响SACs的催化性能。
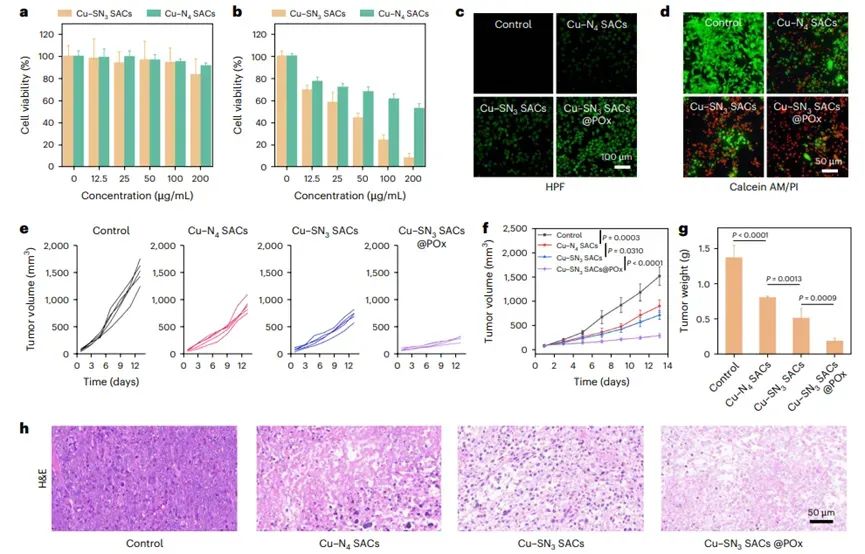
图10 SACs的生物医学应用实验结果
图中汇总了SACs在生物医学应用中的实验结果。包括细胞毒性实验、细胞内活性氧(ROS)产生检测、活/死细胞染色以及体内肿瘤抑制效果评估。结果显示,SACs在模拟肿瘤微环境条件下对癌细胞具有显著的抑制作用,且经过蛋白质修饰的SACs@蛋白复合物在体内展现出更强的肿瘤抑制效果,证明了其在肿瘤治疗中的潜在应用价值。
【全文总结】
本研究详细介绍了基于氮掺杂碳载体(N-C)的单金属原子催化剂(SACs)的设计、制备、表征及其在生物医学中的应用。通过热解金属-有机框架(MOF)或聚多巴胺衍生材料,成功制备了具有不同配位结构的SACs,如Cu-N4、Ir-N5、Co-PN3和Cu-SN3。这些SACs在物理化学表征中展现出良好的分散性和催化活性,特别是在模拟肿瘤微环境(TME)条件下,表现出优异的类过氧化物酶活性。细胞实验和动物模型实验进一步证实了这些SACs在抑制肿瘤生长方面的潜力。研究结果表明,通过合理设计和表面修饰,SACs可以作为一种高效、低毒的纳米催化剂,为肿瘤治疗提供新的策略。
原文链接:
https://www.nature.com/articles/s41596-025-01199-9
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)