首页 > 医疗资讯/ 正文
来自肿瘤生态位的牛磺酸促进白血病进展
骨髓生态位如何影响白血病进程仍然是未知的
众所周知,来自肿瘤微环境(TME)的信号可以调节肿瘤的发生、进展和免疫逃逸。虽然scRNA-seq分析已经确定了细胞 TME 成分,尤其是实体瘤,但一直缺乏将不断变化的TME景观中的配体与癌细胞上的同源受体联系起来的研究。侵袭性难治性髓系白血病,例如急变期慢性髓系白血病(bcCML)和 AML,在复杂的骨髓微环境中起源和扩展。尽管以前的研究已经描述了正常骨髓生态位的细胞组成,但它们在白血病进展期间的动态改变仍未定义。
牛磺酸为髓系白血病的关键调节因子
在这项研究中,罗切斯特大学Jeevisha Bajaj团队利用单细胞RNA测序(scRNA-seq)技术识别了白血病干细胞(LSC)恶性进展过程中来自骨髓间质微环境的关键调控因子。研究通过整合LSC转录组数据和体内CRISPR筛选结果,发现了LSC-微环境相互作用的关键环节,鉴定了牛磺酸-牛磺酸转运子(TAUT)轴作为急性髓系白血病的关键依赖性因子。作者发现牛磺酸合成酶CDO1的表达在髓系疾病进展中逐步增加。敲除骨骼祖细胞中的CDO1可以抑制LSC的生长,并改善生存预后。利用TAUT基因敲除小鼠模型和白血病细胞实验证明,TAUT抑制可显著抑制髓系白血病的进展。机制研究表明,牛磺酸摄取的降低会抑制RAG-GTP介导的mTOR信号通路和下游糖酵解过程。总之,这项研究绘制了白血病进展过程中间质微环境信号的时间谱系,并发现牛磺酸-TAUT轴是髓系恶性肿瘤的关键调控因子,具有潜在的临床应用价值。相关工作以“Taurine from tumour niche drives glycolysis to promote leukaemogenesis”为题发表在Nature。

【文章要点】
一、髓系白血病骨髓微环境的时间scRNA-seq分析
作者利用慢性髓性白血病(CML)干细胞模型,通过单细胞RNA测序(scRNA-seq)技术,对髓系白血病进展过程中骨髓非免疫微环境细胞群的时间变化进行了定义。基于基因表达聚类,作者鉴定出21种间质细胞谱系,包括内皮细胞、软骨细胞、成纤维细胞、周细胞、间充质干细胞(MSC)和骨骼相关细胞群。这些间质细胞群在白血病进展过程中发生了显著的重塑,如MSC、骨骼祖细胞和动脉内皮细胞增加,而静脉窦内皮细胞减少。作者对主要细胞谱系的基因表达模式分析发现,MSC和骨骼细胞的成骨分化和骨矿化相关基因下调,内皮细胞的细胞黏附和迁移相关基因也下调,表明这些间质功能可能在疾病进展中受损。综上所述,这一对间质微环境细胞群的时间序列分析,揭示了它们在髓系白血病进展中发生的动态转录变化。
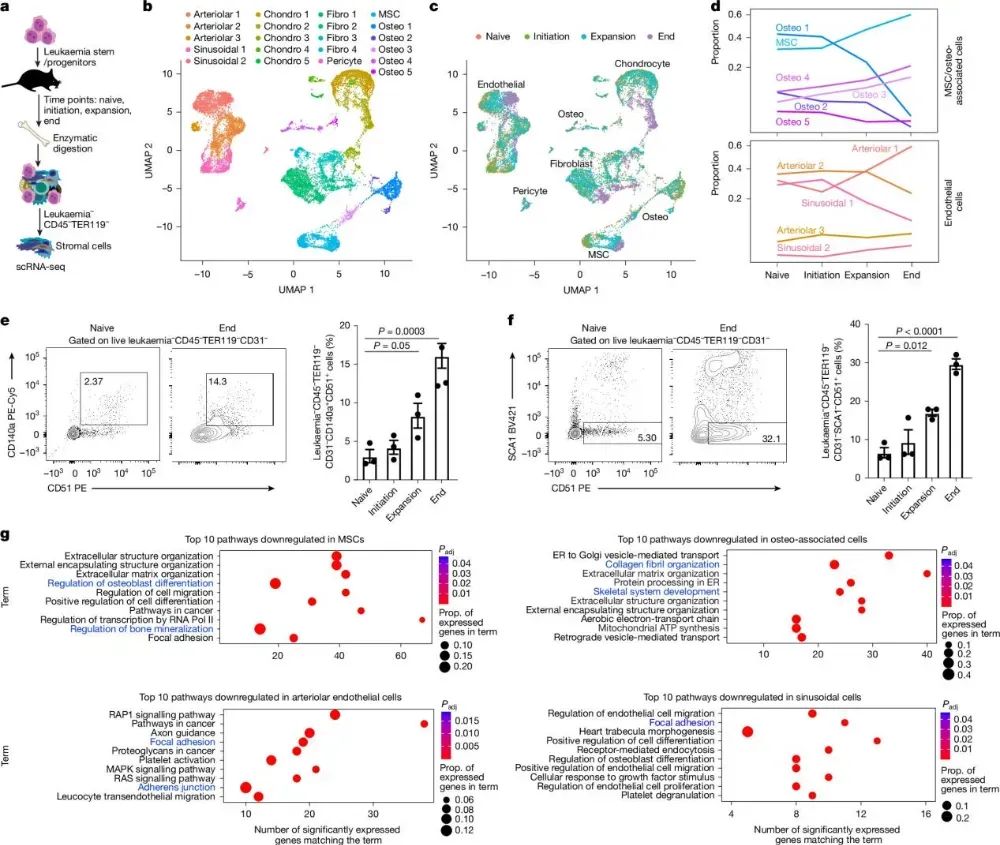
图1 髓系白血病骨髓微环境的时间scRNA-seq分析
二、LSC特异性细胞表面受体的骨髓微环境配体
作者通过LSC-微环境相互作用网络分析,发现多个信号通路可能在白血病进展中发挥功能作用。进一步分析发现,在人类AML LSC中上调的22个基因中,只有低密度脂蛋白受体(LDLR)和SLC6A6与AML患者预后不良有显著相关。作者检测AML患者样本发现,在从骨髓增生异常综合征(MDS)进展到二次AML或复发的病例中,牛磺酸合成酶CDO1蛋白明显上调。体外实验证明,抑制MSC衍生的骨骼祖细胞中的CDO1,可以降低共培养AML细胞的生存和集落形成。白血病患者骨髓间质液中牛磺酸水平较正常对照显著升高1.7倍。在小鼠模型中,敲除骨骼祖细胞中的Cdo1基因可延长小鼠生存时间约13.5%。此外,SLC6A6编码TAUT,作为牛磺酸转运子在bcCML和AML LSC中都显著富集,是一个值得进一步研究的广谱依赖因子。
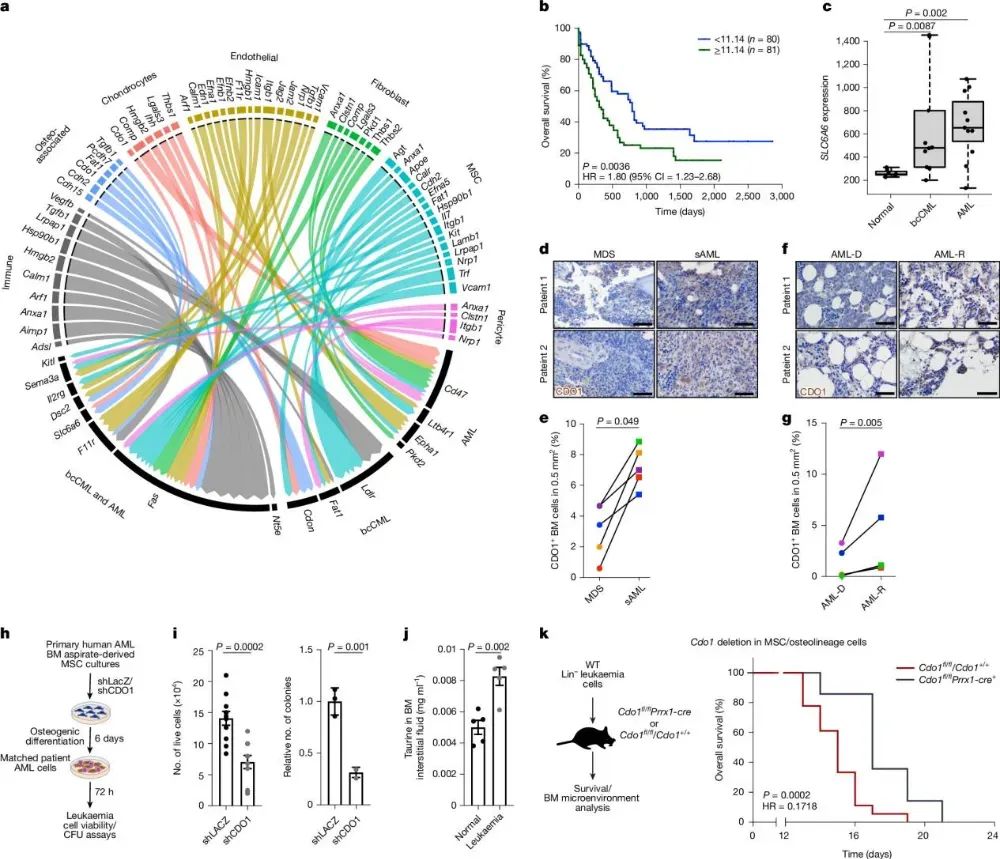
图2 LSC特异性细胞表面受体的骨髓微环境配体
三、TAUT 缺失减少小鼠模型中髓系白血病的发生
作者进一步验证了TAUT在白血病进展中的功能作用,使用全基因敲除Slc6a6(TAUT)小鼠模型发现,TAUT缺失显著延长了慢性髓性白血病(bcCML)小鼠的生存时间,并且不能被外源性牛磺酸补充所拯救。TAUT缺失导致bcCML干细胞(LSC)的集落形成能力下降2.3倍,以及在次级移植实验中LSC功能的明显丧失。此外,TAUT缺失明显延迟了由MLL-AF9/NRAS(G12V)和AML-ETO9a/NRAS(G12V)驱动的急性髓系白血病(AML)的发生。综上所述,这些结果证实了TAUT在髓系白血病的发生发展过程中起关键作用,是一个潜在的治疗靶标。TAUT缺失能显著抑制LSC的功能并延长生存期,表明干扰TAUT可能是一种有效的治疗策略。
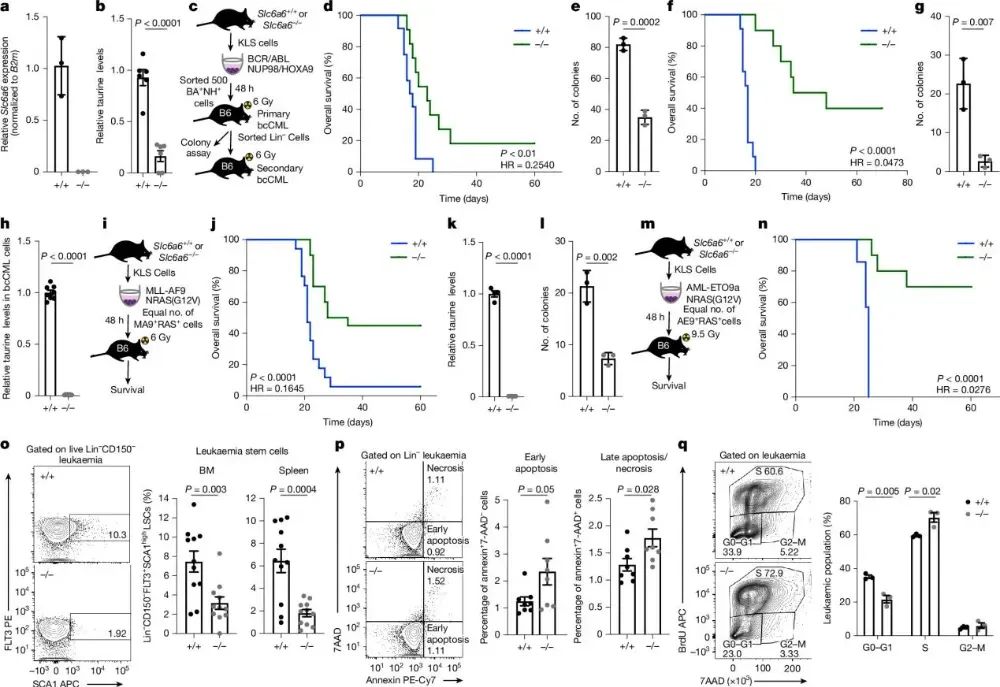
图3 TAUT 缺失减少小鼠模型中髓系白血病的发生
四、TAUT 对人类 AML 生长至关重要
转录组数据分析显示,TAUT在白血病干/祖细胞中普遍表达较高,这一特征与临床上观察到的一些不利预后因素相关。TAUT高表达在具有RAS基因突变的AML细胞中尤为显著,而这类AML往往对常规药物venetoclax产生耐药性。进一步分析发现,TAUT在ROS水平较低的粒-单核细胞系AML干细胞中也高度富集,这一亚型临床上更易出现venetoclax耐药。实验结果显示,TAUT特异性抑制剂TAG和GES能明显抑制原发人AML细胞的增殖,但对正常造血干细胞几乎无影响。此外,TAUT抑制剂与venetoclax联合应用,可以产生显著的协同抑制作用。敲低AML细胞中的TAUT也大幅降低了它们在体外和体内移植模型中的增殖和集落形成能力,却不影响正常造血干细胞的功能。这些发现表明,TAUT是AML干细胞的一个关键依赖性因子,干扰TAUT功能可能成为治疗具有venetoclax耐药性的恶性髓系白血病的新策略。
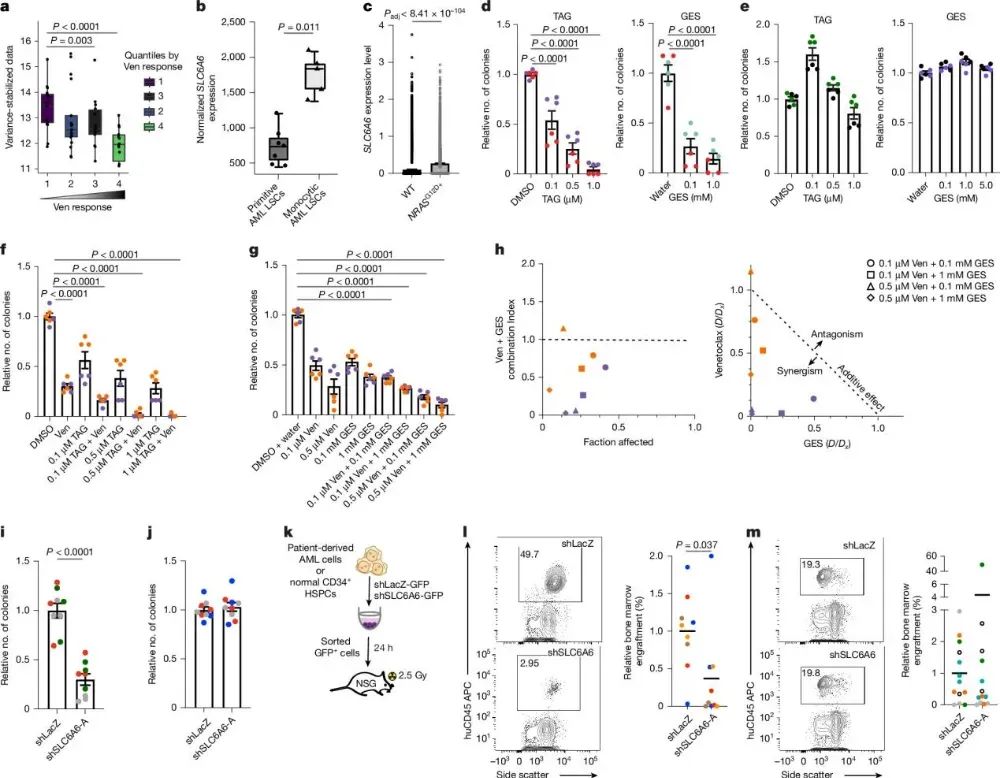
图4TAUT对人类AML生长至关重要
五、TAUT丢失会损害髓系白血病细胞中的糖酵解和mTOR信号传导
代谢组学分析发现,Slc6a6(TAUT)基因敲除后,LSC中糖酵解和TCA循环相关代谢物如丙酮酸、甘油醛-3-磷酸等明显下调,提示牛磺酸可能调控能量代谢。功能实验显示,Slc6a6缺失LSC的基础糖酵解、最大氧消耗量和备用呼吸能力都有降低。添加丙酮酸、乙酸钠和乳酸可以部分恢复其集落形成能力,说明这些代谢产物是牛磺酸调控的下游效应。同位素示踪实验发现,添加的13C标记牛磺酸仅被转化为N-乙酰牛磺酸和谷氨酰牛磺酸。转录组、蛋白质组和磷酸化蛋白质组分析发现,TAUT缺失导致糖酵解相关基因下调,以及MYC和mTOR通路的明显抑制。机制研究表明,TAUT缺失或其抑制剂均可降低mTOR、p70S6K和eIF4B的磷酸化水平。添加mTOR激活剂MHY1485或RAG GTPase突变体(RAGA(Q66L))可以部分或完全逆转这一缺陷。此外,牛磺酸可促进mTOR与溶酶体的共定位,这一过程依赖RAG GTPase,而TAUT缺失则降低了这种相互作用。综上所述,这些结果阐明了牛磺酸-TAUT轴通过调控RAG-mTOR信号通路,从而调节白血病细胞糖酵解代谢,进而影响疾病进展。
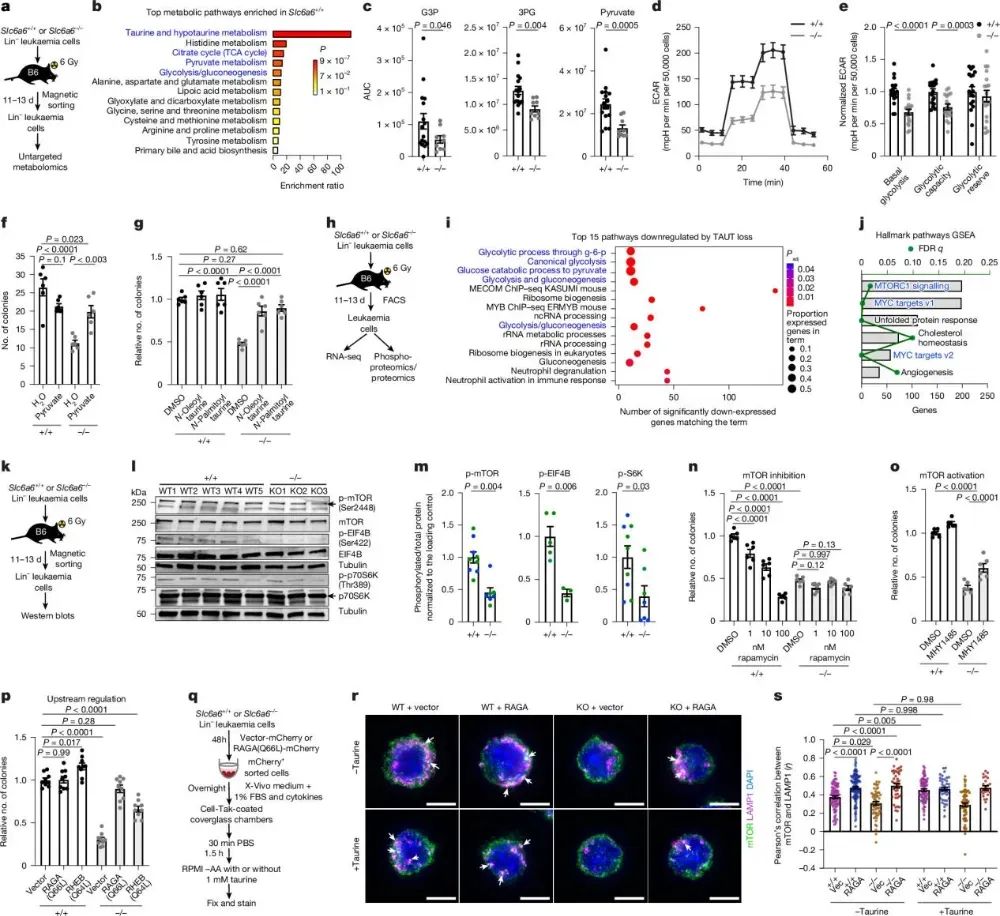
图5TAUT丢失会损害髓系白血病细胞中的糖酵解和mTOR信号传导
【结论与展望】
作者使用scRNA-seq来确定骨髓微环境群体的时间变化,以及疾病进展过程中生态位驱动的信号。为了定义对白血病发生至关重要的TME配体,作者关注了与健康对照相比LSC富集的同源细胞表面受体,以及对体内白血病进展至关重要的同源细胞表面受体,这种方法确定了已知对癌症生长至关重要的信号。在这些信号中,由SLC6A6编码的 TAUT 与人类白血病的不良预后密切相关,并成为AML的关键调节因子。由于牛磺酸可以保护神经,因此可以减轻化疗的副作用或支持抗癌免疫,尚未考虑牛磺酸的促癌作用。作者使用代谢组学、蛋白质组学和转录组学方法,确定了牛磺酸调节白血病发生的下游机制。
原文链接:
https://www.nature.com/articles/s41586-025-09018-7
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)