首页 > 医疗资讯/ 正文
高甲基化肿瘤抑制基因的转录沉默是肿瘤发生的一个标志,但其潜在机制仍不清楚。
2025年4月30日,复旦大学温文玉团队在Nature Cell Biology在线发表题为“Targeting redox-sensitive MBD2–NuRD condensate in cancer cells”的研究论文,该研究表明甲基CpG结合域蛋白2 (MBD2)在不同的癌细胞中形成核凝聚体,在那里它聚集并引导染色质重塑NuRD复合物到这些基因位点进行转录抑制,从而促进肿瘤生长。
MBD2凝聚体的干扰降低了NuRD复合物特异性蛋白的水平,使异染色质焦点不稳定,促进染色质松弛,从而阻碍肿瘤进展。MBD2凝聚体是氧化还原敏感的,由C359介导。促氧化干预驱散MBD2–NuRD凝聚体,从而减轻肿瘤抑制基因的转录抑制。该发现阐明了MBD2凝聚体在维持癌细胞增殖所必需的抑制性染色质状态方面迄今未被重视的功能,并提出了一种针对MBD2凝聚体过量的恶性肿瘤的氧化应激靶向方法。

癌症是由失调的遗传和表观遗传过程引发的累积表型变化的集合体,包括驱动细胞存活、增殖、侵袭和转移的基因的异常转录。这种转录混乱的主要原因是异常的DNA甲基化,这是基因组稳定性、印记和组织特异性基因表达的重要调控因素。在肿瘤中,肿瘤抑制基因启动子内CpG岛的超甲基化很普遍,使甲基化读码器强制转录沉默—这一过程助长了未受抑制的细胞增殖和肿瘤发展。因此,通过靶向DNA甲基化读码器在治疗上逆转这种基因沉默成为癌症治疗的一种引人注目的策略。
甲基CpG结合域(MBD)蛋白家族是DNA甲基化的主要“解读者”。其中,MBD2作为核小体重塑和脱乙酰酶(NuRD)复合物的核心成分,对肿瘤抑制基因启动子中的甲基化DNA表现出明显的亲和力,导致其转录抑制。值得注意的是,MBD2经常被上调以促进多种人类癌症中的肿瘤生长和转移。例如,在胶质细胞瘤形成过程中MBD2的过度表达可能通过抑制关键肿瘤抑制因子BAI1的抗血管生成功能来驱动肿瘤生长。在结肠直肠癌细胞和肺腺癌细胞中发现MBD2表达增强,同时转移抑制因子Maspin和DDB2的表达分别降低,而MBD2的沉默显著减弱了肿瘤转移。最近,过度表达的MBD2被发现通过调节上皮细胞向间质细胞的转化来驱动乳腺癌的进展。
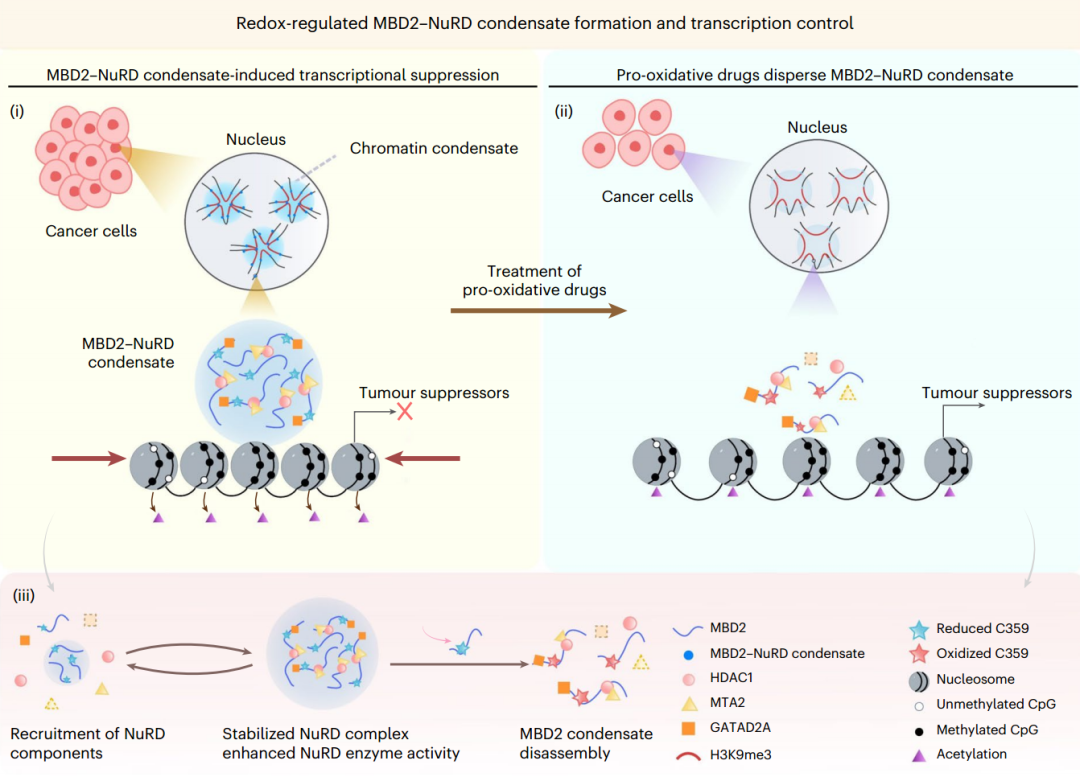
氧化还原调节的MBD2凝聚体的形成和转录控制(图源自Nature Cell Biology)
这项研究表明,MBD2通过液-液相分离(LLPS),在各种癌细胞系中形成动态核凝聚体,对NuRD复合物的装配和染色质致密活性施加控制。具体来说,在宫颈癌细胞中,MB D2–NuRD凝聚体显示出抑制含有高甲基化启动子的肿瘤抑制基因,从而促进宫颈癌细胞的增殖。重要的是,暴露于活性氧物种(ROS)有效地分散MBD2凝聚体并减轻肿瘤细胞中的转录抑制,这表明一种有前途的氧化应激驱动的MBD2丰富的癌症治疗方法。该研究揭示了MBD2通过形成相分离凝聚体组装并激活NuRD复合物,进而阻遏抑癌基因转录以促进癌细胞增殖的分子机制,并为MBD2高表达肿瘤提供了基于氧化还原调控的靶向治疗策略。
参考信息:
https://www.nature.com/articles/s41556-025-01657-2
猜你喜欢
- 医养结合,保障老人健康生活(为了幸福美满的晚年④)
- Redox Biol 华中科技大学同济医学院付琴团队揭示靶向抑制磷酸二酯酶PDE4D对心衰的保护作用
- 张伯礼建言上千年药乡甘肃:中医学与中药“两条腿”行走
- 克罗米酚、来曲唑等7种常用促排药用法用量全解析!
- 24小时尿蛋白测定的意义及留取方法
- 三甲基巴豆酰辅酶A羧化酶缺乏症
- 严重脓毒症和感染性休克中氧摄取与灌注指标:诊断、治疗及预后的意义
- Gut:郑州大学张明智/李兆明等发现肠道菌群作为自然杀伤/T细胞淋巴瘤的无创性诊断和预后生物标志物
- 国家卫健委回应新冠疫情防控热点问题 “乙类乙管”绝不是放任不管
- 北京清华长庚医院超声乳化波切一体机设备招标公告
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)