首页 > 医疗资讯/ 正文
白细胞介素-13(Interleukin-13, IL-13)是白细胞介素家族中由活化的T细胞产生的细胞因子之一,参与调节辅助型T细胞1(T helper 1 cell, Th1)和辅助型T细胞2(T helper 2 cell, Th2)功能与分化,并作用于B细胞的一种细胞因子,有促进炎症作用,与瘙痒感觉密切相关,同时,其也参与皮肤病的发病及转归过程。
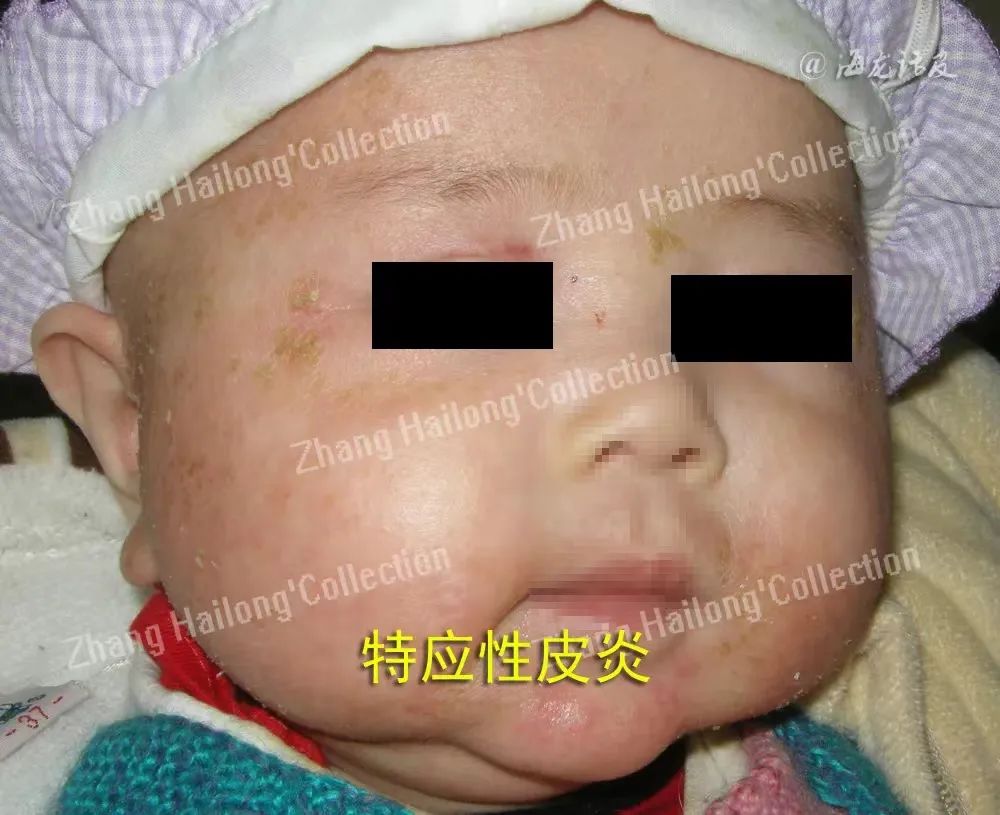
特应性皮炎、结节性痒疹、大疱性类天疱疮、慢性自发性荨麻疹、干皮症等瘙痒疾病患者的血清及皮肤中都检测到IL-13的高表达,这提示IL-13在瘙痒性疾病中扮演了重要角色。
一
IL-13的生物学特性
1、IL-13的基因结构:
IL-13是一种细胞因子,属于细胞因子家族中的白细胞介素家族。人的IL-13基因定位于5q31染色体,小鼠的基因定位于11号染色体(对应人类5号染色体的区域),故人和小鼠的IL-13在基因水平上有66%的同源性,因为人IL-13与小鼠IL-13在结构上相似,所以也具有类似的功能。IL-13和白细胞介素-4(Interleukin-4, IL-4)都是由单链多肽组成,具有相似的三维结构。其都与共享的受体亚单位IL-4受体α亚基(Interleukin-4 receptor subunit alpha, IL-4Rα)结合,形成三聚体复合物,此外,两者都是由4个反向平行的α螺旋组成的蛋白,结构和序列的同源性使IL-13和IL-4在生物学功能上有着相似性。
2、IL-13的来源:
产生并释放IL-13的细胞种类很多。最早发现能释放IL-13是T细胞,主要是由Th2细胞产生,但嗜酸性粒细胞、嗜碱性粒细胞、肥大细胞、巨噬细胞、单核细胞、成纤维细胞、朗格汉斯细胞及角质形成细胞等也可分泌IL-13。有文献报道,角质形成细胞来源的白细胞介素-25(Interleukin- 25, IL-25)可以激活Ⅱ型固有淋巴细胞(type Ⅱ innate lymphoid cells, ILC2s),驱动过敏性皮肤炎症,促进IL-13的生成。除此之外,还有研究发现辅助性T细胞22(Helper T cell 22, Th22)是T细胞亚群,也是IL-13的来源之一。
二
IL-13受体
IL-13受体属于二聚体,由IL-13受体α1(Interleukin-13 Receptor α1,IL-13Rα1)与IL-13受体α2(Interleukin-13 Receptor α2,IL-13Rα2)组成,在IL-13作用过程中均发挥非常重要的作用。IL-13Rα1主要表达在气道上皮、平滑肌、成纤维细胞和肥大细胞上,而IL-13Rα2一般由多种促炎细胞因子诱导,表达在角质细胞和上皮细胞,这些诱导因子包括IL-13、IL-4、干扰素γ(Interferon-γ, IFN-γ)、肿瘤坏死因子α(tumor necrosis factor-α, TNF-α)和白细胞介素-17(Interleukin-17, IL-17)等。
IL-13主要通过由IL-13Rα1和IL-4Rα组成的二聚体受体发挥作用。IL-13以低亲和力单独结合IL-13Rα1,但当IL-13Rα1与IL-4Rα结合形成异质二聚体受体后,IL-13则可以与其二聚体高亲和力结合形成三聚体发挥作用。IL-13与其受体结合后,激活了受体内部的酪氨酸激酶Janus激酶1(Janus Kinase 1, JAK1)和Janus激酶2(Janus Kinase2, JAK2),这两种酶进而磷酸化了受体上的酪氨酸残基。这些磷酸化的酪氨酸残基提供了结合位点,使信号传导及转录激活蛋白6(signal transducer and activator of transcription 6, STAT6)结合到受体上。STAT6进一步被磷酸化,并形成二聚体,进入细胞核并结合到特定的DNA序列上,从而激活下游基因的转录和表达。除IL-13Rα1外,IL-13还可以与IL-13Rα2高亲和力结合。
三
IL-13诱导瘙痒的机制
IL-13能够直接引起瘙痒。OETJEN等观察到感觉神经元上存在IL-13Rα1受体,研究人员在小鼠皮下注射IL-13,发现小鼠的搔抓次数增加,这表明IL-13可以直接激活感觉神经元上的受体引起瘙痒。CAMPION等将IL-13单独 和/或联合IL-4注射到小鼠脸颊皮下,发现均能引起小鼠的瘙痒行为,但联合应用时瘙痒行为更加显著。这一研 究也佐证了IL-13不仅能够单独致痒,而且能够间接提高其他致痒因子的敏感性。
瞬时受体电位香草素1 (transient receptor potential vanilloid 1, TRPV1)和瞬时受体电位通道锚蛋白1(transient receptor potential ankyrin 1, TRPA1)是介导瘙痒的重要离子通道。OETJEN等研究发现,敲除了TRPV1后,细胞对IL-13的反应减少,这提示TRPV1是其下游离子通道。MENG等使用IL-13转基因小鼠特应性皮炎模型测试了TRPA1通路在特应性皮炎瘙痒中起的作用时,发现TRPA1表皮和真皮区域的表达显著增强并且小鼠的搔抓次数增多,给予 TRPA1拮抗剂后,搔抓的行为明显减少。
综上所述,IL-13可直接激活神经末梢的IL-13受体,通过打开TRPV1和TRPA1引起钙离子内流,向高级中枢传递痒觉信号。而IL-13激活神经末梢的IL-13受体后,是经背跟神经节(dorsal root ganglia, DRG)向中枢传递痒觉信号,发生搔抓行为。IL-13也能间接引起瘙痒。胸腺基质淋巴细胞生成素(thymic stromal lymphopoietin, TSLP)也是表皮/免疫神经元引起瘙痒的主要瘙痒原因之一。3β-羟基类固醇脱氢酶1(3β-Hydroxysteroid Dehydrogenase 1, HSD3B1)表达于皮脂腺,其高表达可以引起皮肤屏障功能的破坏,IL-13可以刺激HSD3B1的高表达来驱动人皮脂细胞和角质形成细胞中的脂质异常,造成屏障功能障碍,引起瘙痒。此外,研究发现,IL-13与DRG神经元中TRPA1的表达增强有关,IL-13可以使真皮神经肽分泌传入神经纤维的生长增强,同时强烈诱导DRG中功能性TRPA1的表达升高,刺激产生瘙痒行为。
四
IL-13参与相关皮肤疾病的瘙痒
1、特应性皮炎:
IL-13是引起特应性皮炎慢性瘙痒的关键细胞因子之一。临床研究表明,特应性皮炎患者的搔抓次数与IL-13水平呈正相关。在特应性皮炎患者的皮损和外周血中都发现 了IL-13mRNA的高表达。YUN等的研究发现,特应性皮炎模型小鼠皮肤损伤部位的IL-13mRNA水平显著升高,小鼠的瘙痒程度也与IL-13mRNA的表达相关。此外, IL-13在特应性皮炎病变皮肤中的表达明显高于IL-4,对炎症细胞的招募、皮肤微生物组的改变和表皮屏障功能的降低有着重要作用。环孢素A治疗特应性皮炎有良好效果;IL-13抑制剂曲罗芦单抗(Tralokinumab)在临床试验中也已被验证能够有效缓解特应性皮炎患者的瘙痒症状。
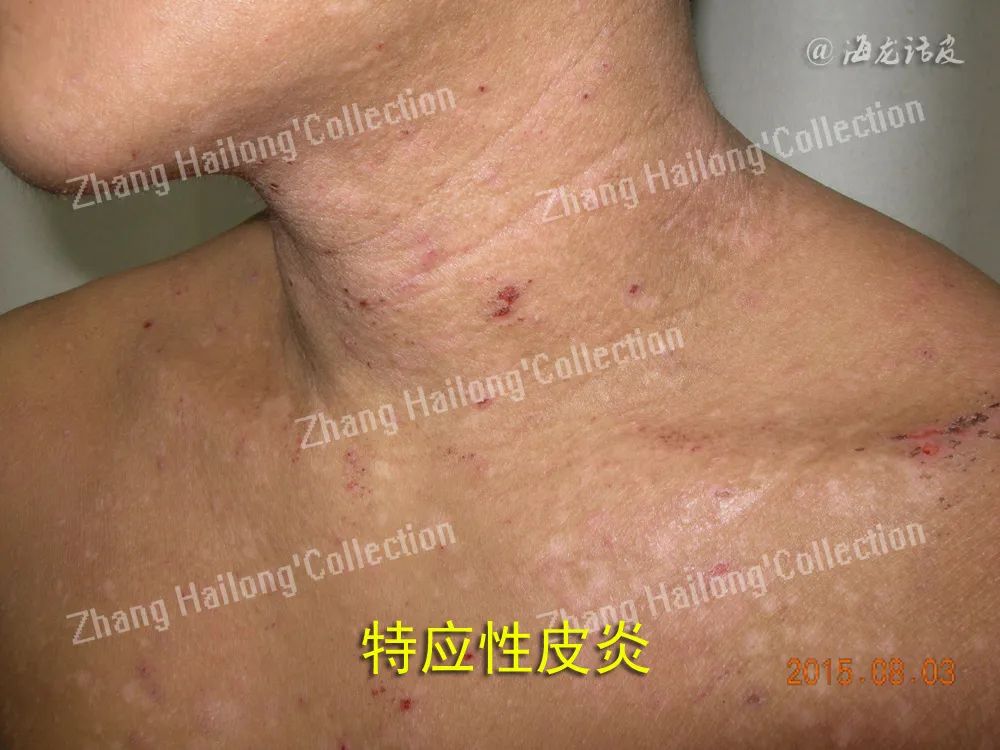
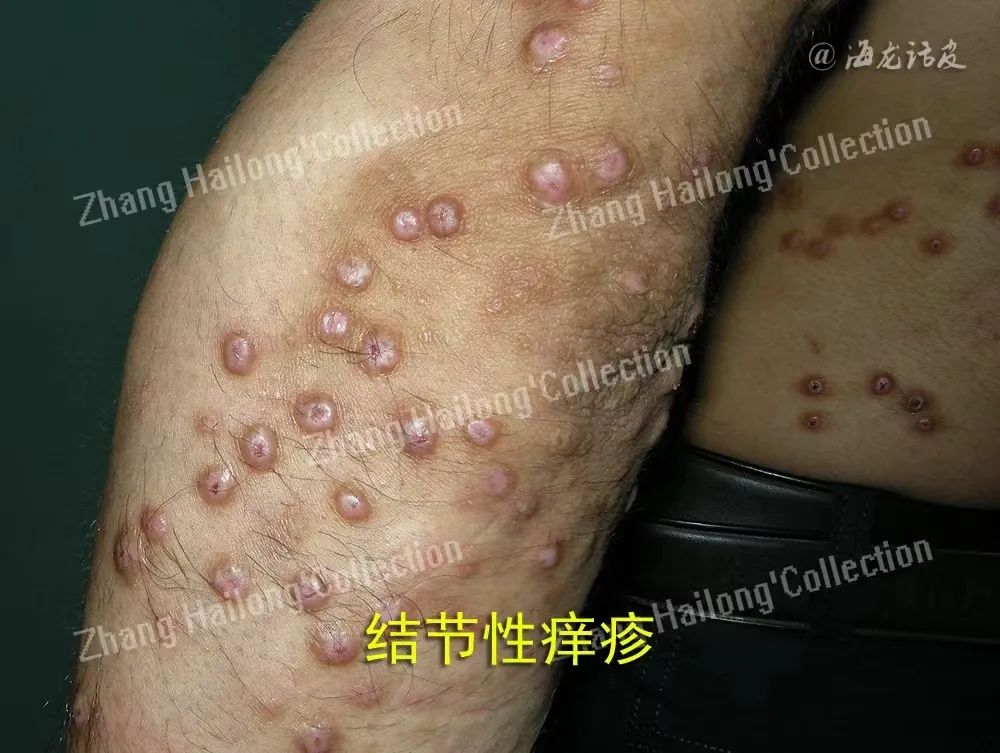
2、结节性痒疹:
结节性痒疹是一种慢性炎症性皮肤病,表现为四肢和躯干极度瘙痒、角化过度的结节,严重降了患者的生活质量。PARTHASARATHY等从结节性痒疹患者和无瘙痒的对照患者中获取全血,血浆检测IL-4、白细胞介素-5(Interleukin-5, IL-5)、 IL-13和骨膜蛋白的浓度,结果结节性痒疹中的循环血浆IL-13和骨膜蛋白浓度与对照组相比,显著升高。IL-4和IL-5则没有显著升高。这说明IL-13参与了结节性痒疹的瘙痒。
3、干皮症:
2020年,土耳其学者FUJII等报道了IL-13与白细胞介素-31(Interleukin-31, IL-31)参与干皮症瘙痒的研究。FUJII团队用丙酮/乙醚以及蒸馏水建立了小鼠干皮症模型,并用RT-PCR和免疫组织化学法评估IL-13和IL-31在皮肤组织中的基因和蛋白表达,发现干皮症模型组的IL-13、IL-31与对照组比较显著升高,提示IL-13和IL-31在干皮症慢性瘙痒中扮演了重要角色。
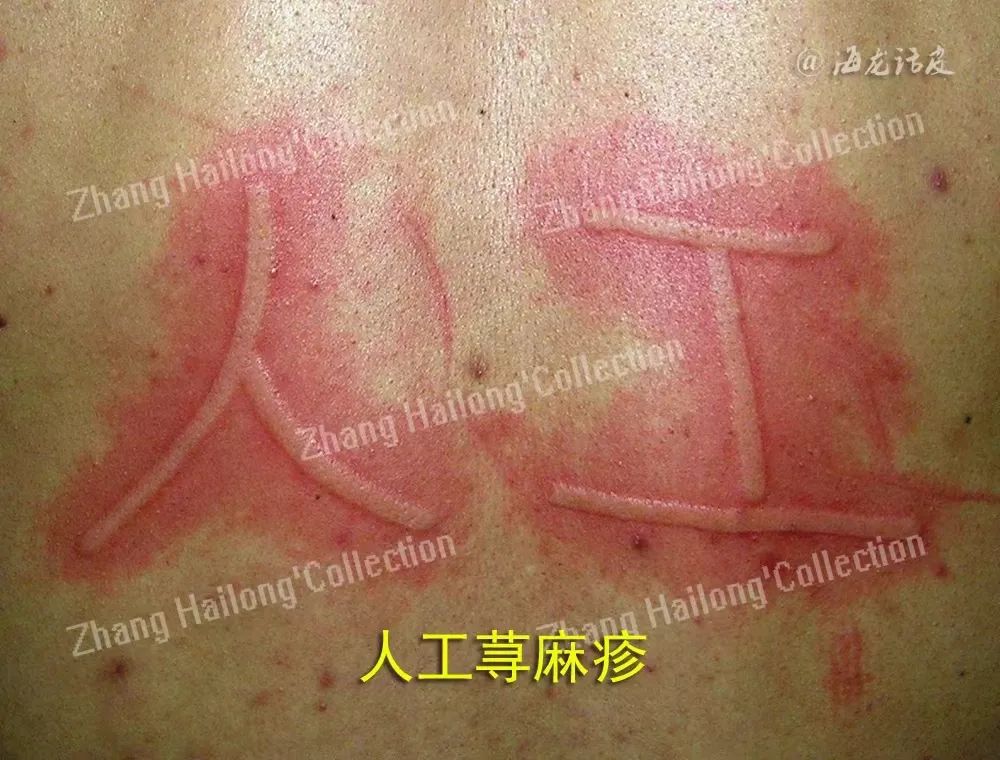
4、慢性自发性荨麻疹:
慢性自发性荨麻疹是一种以瘙痒为主要临床特征的皮肤疾病。研究发现,虽然肥大细胞脱颗粒是导致慢性自发性荨麻疹发病的关键环节,但IL-13的也发挥了重要作用,BAE等发现慢性自发性荨麻疹患者的IL-13的水平明显高于正常人,提示IL-13可能参与了慢性自发性荨麻疹的瘙痒。
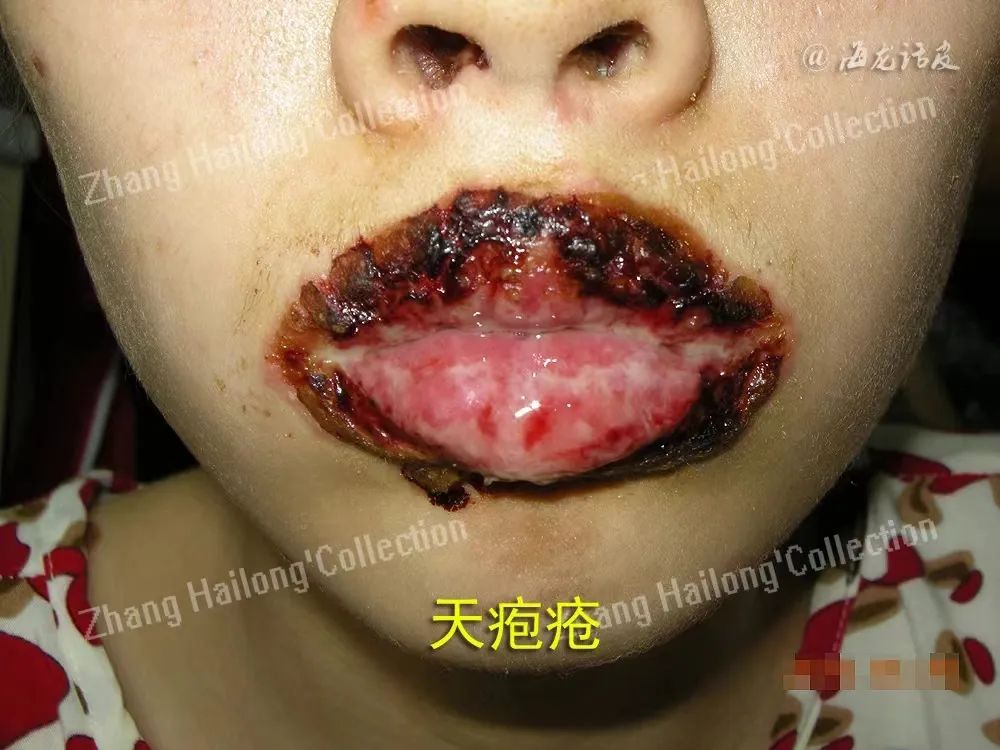
5、大疱性类天疱疮:
大疱性类天疱疮是一种复发率高的老年性慢性自身免疫性大疱性皮肤病,瘙痒是其主要的临床表现。WANG等检测正常患者和大疱性类天疱疮患者血清IL-13水平,发现正常患者和大疱性类天疱疮患者血清IL-13水平均升高,但是大疱性类天疱疮患者的IL-13水平升高更明显,表明IL-13与大疱性类天疱疮的发病机制相关。TERAKI等的研究也发现大疱性类天疱疮患者外周血IL-13水平明显高于健康人,其水疱中IL-13水平则明显高于外周血,这也提示IL-13是参与大疱性类天疱疮发病过程中的细胞因子。还有一项研究也对比了大疱性类天疱疮患者和健康人真皮中IL-13的差异,发现大疱性类天疱疮患者IL-13水平较健康人显著增多,并且其增加的水平与瘙痒程度相关,表明IL-13可能参与大疱性类天疱疮瘙痒。
五
以IL-13为靶点的治疗
由于IL-13是参与过敏性疾病的关键细胞因子,对炎症反应的发生、进展以及皮肤屏障功能的维持有着重要的影响,因此临床很多针对IL-13为靶点的药物开发。目前有两种针对IL-13药理学作用途径的方法用于治疗与IL-13相关的皮肤疾病:一是影响IL-13细胞内信号通路相互作用的小分子激酶抑制剂。二是阻断IL-13与其受体位点结合的生物制剂。
1、激酶抑制剂:
JAK激酶(Janus kinase, JAK)是通过JAK-STAT信号途径发挥作用的细胞内酪氨酸激酶,介导细胞因子的产生,也是IL-13信号通路的关键酶。JAK-STAT通路的激活需要受体与其配体结合,从而激活JAK激酶。激活的JAK激酶会磷酸化受体和自身,从而形成结合位点,进一步促进STAT蛋白磷酸化。磷酸化的STAT蛋白会形成二聚体,进入细胞核,与DNA结合,从而调节基因转录和表达。一些对JAK蛋白有选择性的抑制剂如巴瑞替尼、阿布替尼和乌帕替尼等,可用于治疗JAK-STAT通路相关的皮肤瘙痒,如特应性皮炎。
在一项临床对照研究 (BREEZE-AD PEDS)中,中度至重度特应性皮炎儿童患者按1∶1∶1∶1随机分配,然后每日分别给予巴瑞替尼 1、2、4mg和安慰剂持续16周。结果显示,巴瑞替尼在16周内改善了中度至重度特应性皮炎患者的临床体征和症状,并使瘙痒快速减轻。在另外一项临床试验中,患者按2∶2∶1随机分配,每日口服阿布替尼200、100mg和安慰剂,持续12周,结果显示每日口服阿布替尼单药治疗对中度至重度特应性皮炎有良好效果。此外,PALLER等一项3期试验也显示,给予患者15mg和30mg 剂量的乌帕替尼治疗,患者的皮炎和瘙痒情况得到明显改善。这些结果都提示了JAK抑制剂可以通过抑制IL-13的信号通路缓解瘙痒症状。
2、生物制剂:
度普利尤单抗(Dupilumab):是一种单克隆抗体药物,用于治疗特定类型的炎症性疾病,如特发性皮肤病(例如银屑病和湿疹)和哮喘,Dupilumab的作用机制是通过抑制IL-4和IL-13的信号传导。Dupilumab通过对IL-4和IL-13信号的直接抑制,降低了2型炎症相关标志物表达水平,还通过对嗜酸性粒细胞的作用,减少了IL-31分泌,从而使外周瘙痒感觉神经元信号降低。一项给予Dupilumab治疗的结节性痒疹的队列研究报告结果显示,给予患者Dupilumab后,50%的患者瘙痒症状和皮肤病变完全消退,41.7%的患者部分消退,只有1例患者无改善,这说明Dupilumab对结节性痒疹的瘙痒和症状 有显著的治疗效果。
BLAUVELT等的研究评估了采用Dupilumab治疗中度至重度特应性皮炎成年患者,在4年的治疗期间是否增加了感染的风险。患者接受 Dupilumab300mg1次/周或1次/2周,并且允许局部使用皮质类固醇和钙调磷酸酶抑制剂。研究结果显示,在Dupilumab治疗期间,患者的感染风险并未增加。这表明Dupilumab不仅可以治疗特应性皮炎,而且在长期治疗中能降低特应性皮炎的感染风险。
曲罗芦单抗(Tralokinumab):是一种全人源IgG4单克隆抗体,能够特异性结合IL-13,抑制IL-13与IL-13Rα1、IL-13Rα2受体链的结合。WOLLENBERG等对中至重度特应性皮炎成人患者进行了Tralokinumab单药的治疗效果评估,每2周1次皮下注射300mg的Tralokinumab,每日瘙痒情况 得到了显著改善。SIMPSON等对Tralokinumab治疗特应性皮炎进行了研究,他们将患者随机分配到接受Tralokinumab治疗组或安慰剂组;Tralokinumab治疗组患者皮下注射Tralokinumab1次/2周,而安慰剂组的患者接受了相应的安慰剂注射;研究结果表明,Tralokinumab治疗组在1年的治疗期间显示出显著的疗效,相较于安慰剂组,Tralokinumab治疗组的患者在改善皮肤症状、减轻瘙痒和提高生活质量方面表现出显著优势,在皮肤清晰度和病情严重度方面也有显著改善。这些结果都提示Tralokinumab可治疗IL-13参与的特应性皮炎瘙痒。
来金珠单抗(Lebrikizumab):是一种能与IL-13高亲和力结合,并能阻断IL-13信号传导的新型单克隆抗体。一项为期52周的3期研究(MP444681KB)中,PALLER等研究人员招募了来自澳大利亚、加拿大和美国的12~18岁、体重≥ 40kg患有中度至重度特应性皮炎的患者。这些患者在第0周和第2周接受500mg的 Lebrikizumab负荷剂量,然后每2周接受250mg,持续52周。研究结果表明,62.6%的患者在试验结束时皮肤得到显著改善,而且Lebrikizumab还提高了患者的生活质量。此外,BLAUVELT等也进行了两项相同的3期临床试验,Advocate1(ADv1)和 Advocate2(ADv2),以评估Lebrikizumab作为单一疗法治疗中重度特应性皮炎患者的有效性和安全性,结果显示在52周的治疗期间,Lebrikizumab持续改善了疾病严重程度和皮 肤瘙痒感,且安全可控。这些发现支持Lebrikizumab是治疗中度至重度特应性皮炎患者的潜在选择。
六
小结
近年来,关于皮肤瘙痒性疾病的研究得到了不断深入。在瘙痒的调节过程中,细胞因子起着重要的作用,其中包括IL-4、IL-13、IL-31、IL-33和TSLP等。然而,IL-13在瘙痒中的作用越来越受到人们的关注。IL-13通过与其受体结合,激活细胞内的信号传导通路,从而引起瘙痒感觉。IL-13也可以影响与瘙痒有关的离子通道 TRPA1和TRPV1的活性,进一步增强瘙痒感觉的传导。未来,IL-13在其他瘙痒性疾病中的作用机制及以IL-13为靶点的药物研发将是研究的重点。希望通过深入研究IL-13的作用机制,开发更有效的治疗方法,为患者提供更好的缓解瘙痒和提高生活质量的选择。
参考文献:
1.梁小玲,何爽,伍师坚等.白细胞介素-13参与瘙痒的研究进展[J].中国现代医学杂志, 2024, 34(11): 59-65.
2.倪慕兰, 李燕维, 刘斌.IL-13a1及IL-13Ra2在特应性皮炎患者皮损中的表达[J].医学理论与实践, 2023, 36(21): 3728-3730.
3.贾海平, 万慧颖, 张丁丁.老年特应性皮炎患者外周血Th1、Th2、Th17细胞与鳞状上皮细胞癌抗原水平的变化及意义[J].中国现代医学杂志, 2023, 33(19): 85-91.
4.其他文献略。
- 上一篇:手脚冰凉,居然可以打肉毒毒素改善?
- 下一篇:益生菌促进伤口愈合的作用机制的研究进展
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)