首页 > 医疗资讯/ 正文
针对衰老的药物研究现状及局限性
衰老是众多疾病的关键诱因,针对衰老进行药物干预是当前药物研发领域追逐的热点之一。主流抗衰老药物按照其作用机制可分为Senolytic和Senomorphic两类,前者通过活化细胞死亡途径,直接杀伤衰老细胞,对于药物剂量具有较强的依赖性;而后者作用于炎性信号通路,用于降低SASP(炎症相关分泌表型)因子的分泌,对于药物剂量的需求低于Senolytic,但缺乏对衰老细胞的选择性。如何利用单一制剂融合二者优势,规避相应的风险,是当前衰老药物研发领域亟待突破的关键瓶颈。
本研究的内容概况
近日,南京医科大学霍达教授团队、陈宏山教授团队联合江苏省人民医院丁清清主任团队基于晶相/手性双工程化策略构建了衰老细胞选择性纳米酶。生理学及病理学屏障的存在造成了纳米酶在给药后在病变部位呈现出剂量差异性分布,双工程化纳米酶的核心优势在于能够基于剂量及针对微环境衰老程度的感知,发挥出多层次抗衰老活性。结合临近光标记辅助的蛋白质组学分析及转录组学分析,研究进一步揭示了双工程化纳米酶的抗衰老活性与其在衰老微环境下所呈现出的针对无膜细胞结构的浓度依赖选择性密切相关。本项工作以”Combating Atherosclerosis with Chirality/Phase Dual-Engineered Nanozyme Featuring Microenvironment-Programmed Senolytic and Senomorphic Actions.” 为题发表在Advanced Materials。

[文章要点]
1)甲硫氨酸配体在赋予高熵合金产物手性同时,能够同时诱导其晶相无序化;
2) 无序化(又称玻璃态或无定形)高熵合金相较于晶态产物展现出更高的纳米酶催化活性;
3)纳米酶在衰老微环境下表现出手性依赖性蛋白吸附行为,吸附蛋白的液液相分离能力发生改变,引发相关无膜细胞器重构,通过调控无膜结构-有膜细胞器作用网络,纳米酶诱发衰老细胞结构及代谢重塑,发挥抗衰老效果;
4)在较高剂量下,纳米酶的抗衰老活性来自于其对硫辛酸化修饰的DLAT蛋白的招募及衰老微环境激活的类过氧化物酶活性,两者分别促进了铜死亡和铁死亡途径的活化,系统性发挥Senolytic效果;
5)当多重结构屏障限制了纳米酶向深层衰老组织的扩散时,在有限摄取纳米酶的衰老细胞内,纳米酶通过诱发NONO为核心的核旁斑异位,重塑异染色质,削弱SASP基因表达,发挥Senomorphic效果;
6)双工程化纳米酶通过发挥多层次抗衰老效果,显著改善了动脉粥样硬化的症状。
[研究结果速览]
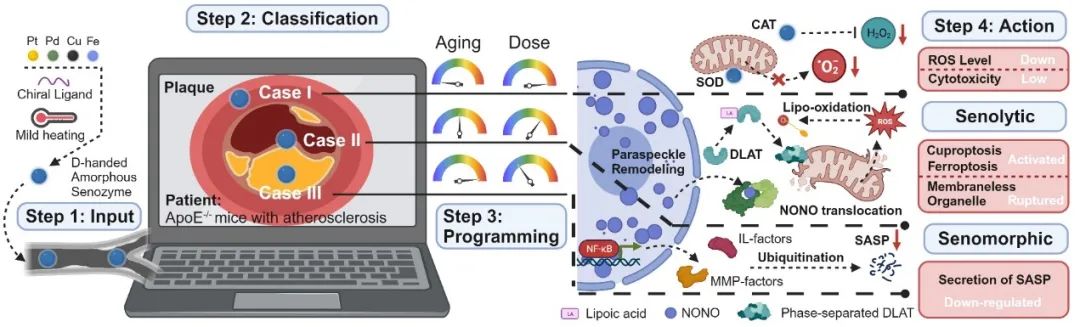
图一. 双工程纳米酶基于环境编程的抗衰老行为作用机制。
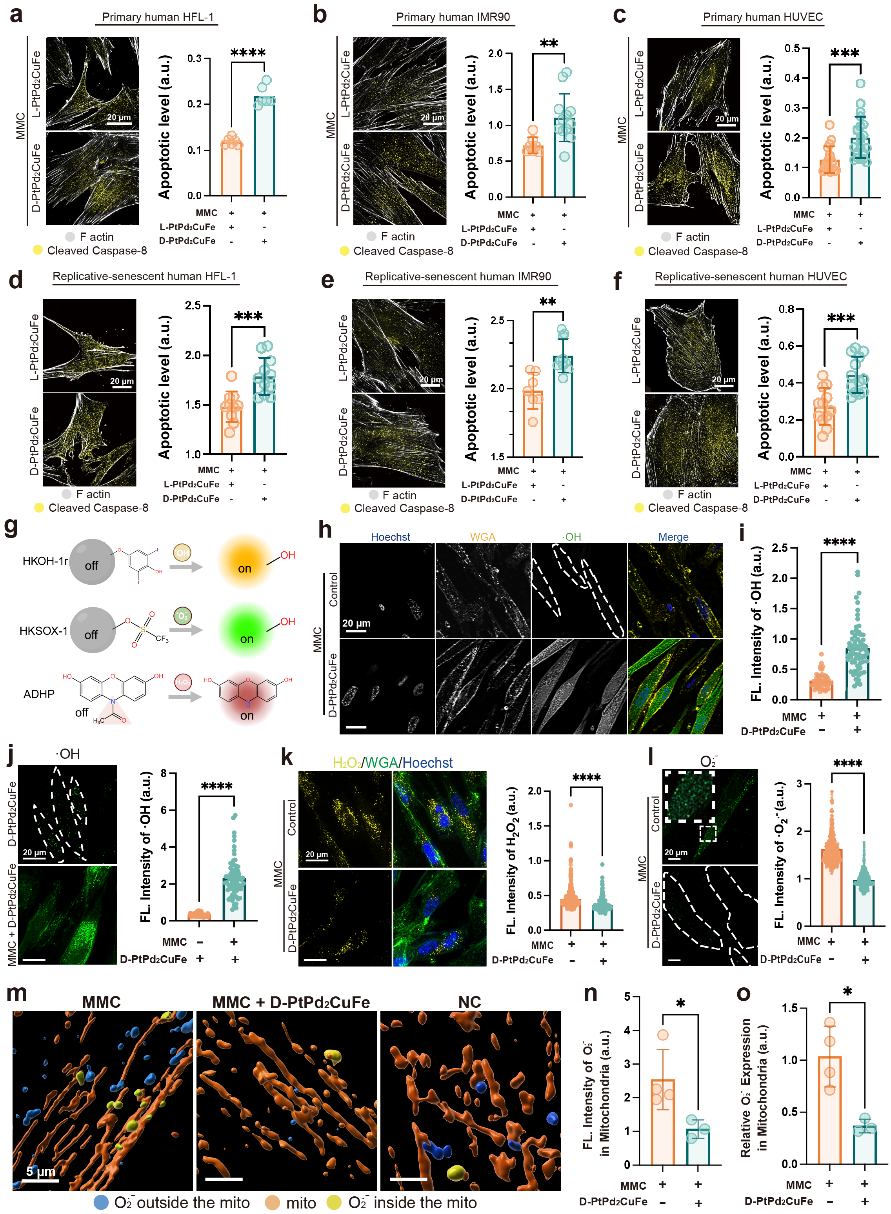
图二. 纳米酶Senolytic效果探究。
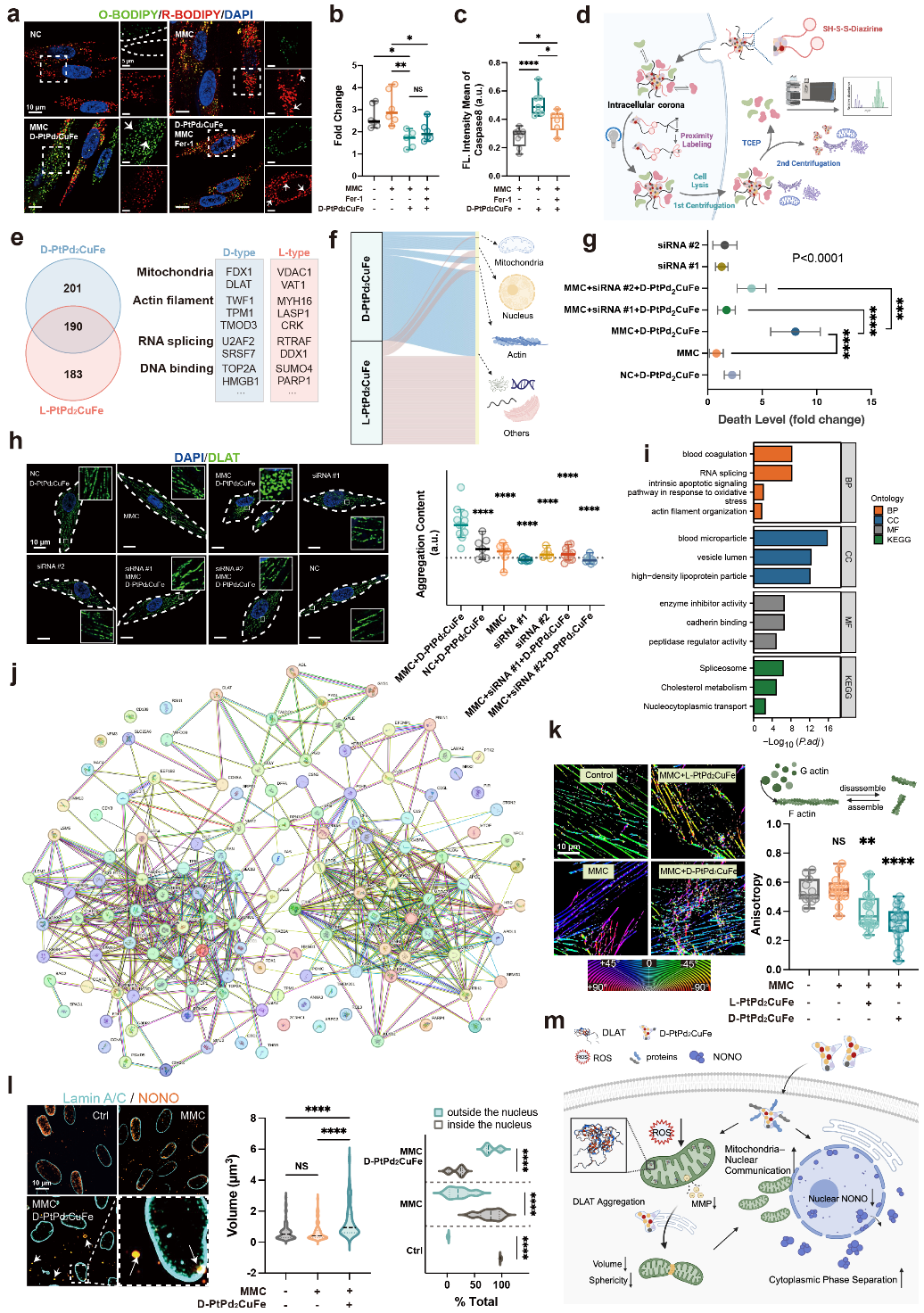
图三. 纳米酶调控细胞内无膜结构的作用机制。
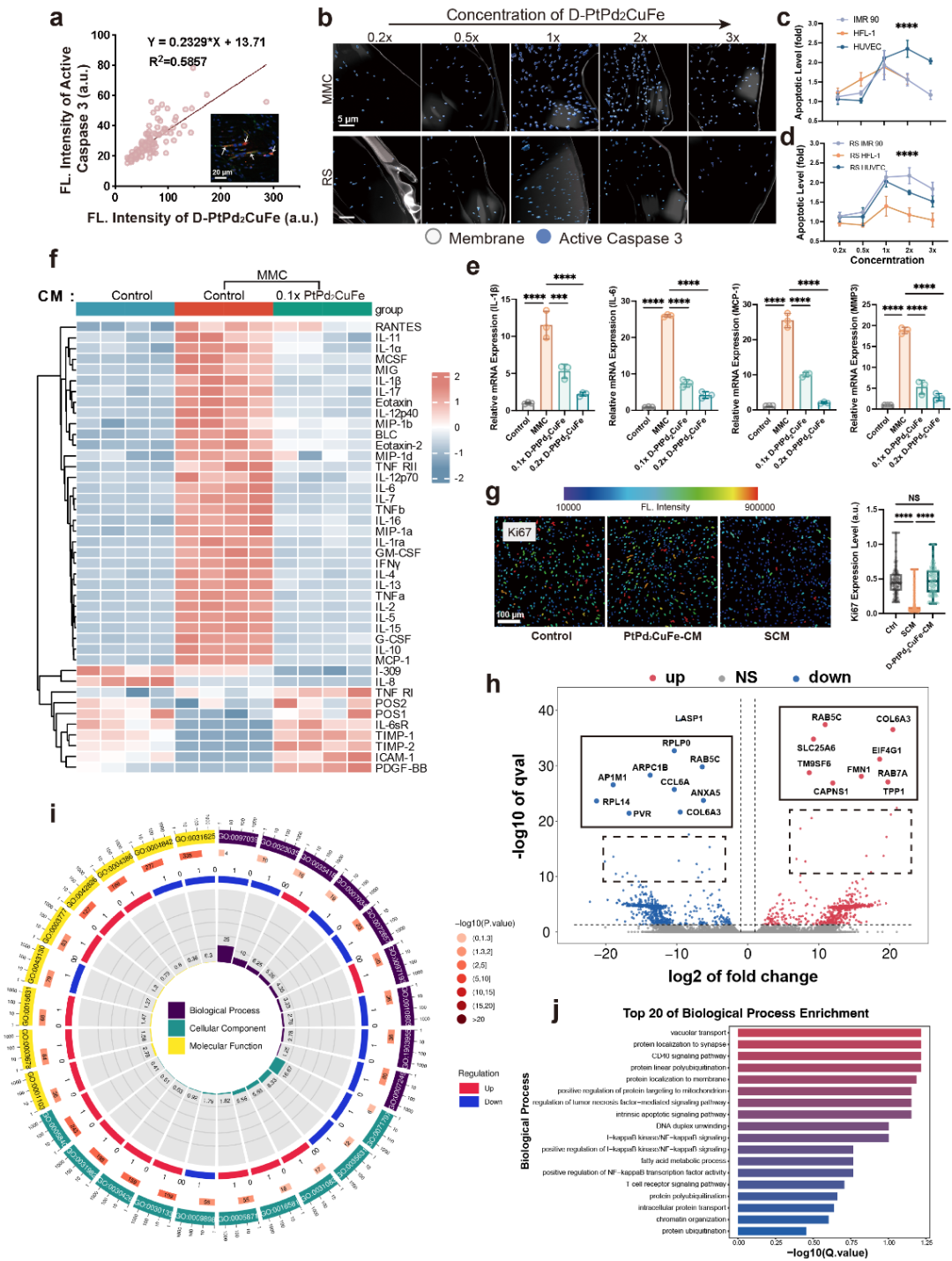
图四. 纳米酶Senomorphic效应及其分子机制。
原文链接:
https://onlinelibrary.wiley.com/doi/10.1002/adma.202401361?af=R
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)