首页 > 医疗资讯/ 正文
心脏移植是治疗终末期心脏病的最有效方法,全球每年心脏移植手术数量超过4000例,并且呈现增长趋势。心脏移植术后的免疫抑制治疗是解决移植后排斥的主要方法,对患者生存至关重要,环孢素等免疫抑制剂可有效抑制急性排斥并显著提升移植物的生存时间,但同时增加感染和肿瘤风险,限制了受者的生存期和生活质量,诱导心脏移植免疫耐受是器官移植的研究热点和难点。
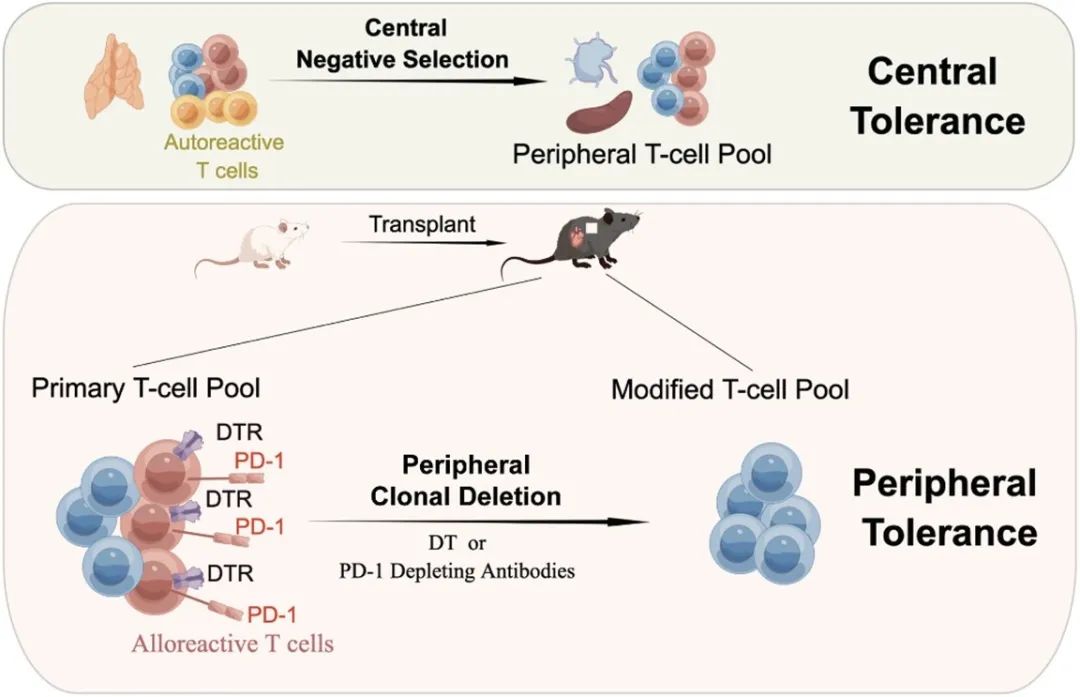
移植免疫创始人彼得·梅达沃(Peter Brian Medawar, 1915-1987)因“发现获得性免疫耐受(The Discovery of Acquired Immunological Tolerance)”,于1960年获得诺贝尔生理学医学奖,其是小鼠胸腺内的T细胞的中枢克隆清除(Central Clonal Deletion)的结果,因为人与小鼠胸腺发育的差异,该成果并未实现临床转化。心脏移植后同种异体反应性T细胞接触到异体抗原、活化、增殖并分化成效应细胞,浸润到心脏移植物介导了排斥反应和移植物失功。然而,是否可以模拟中枢阴性选择对同种异体反应性T细胞进行外周克隆清除(Peripheral Clonal Deletion)以实现心脏移植后的免疫耐受尚不清楚。
2024年4月26日,华中科技大学同济医学院附属协和医院心脏大血管外科的夏家红、吴杰教授团队在免疫学顶刊Science大子刊Science Immunology上发表了题为“Targeted depletion of PD-1-expressing cells induces immune tolerance through peripheral clonal deletion”的研究论文,揭示了一种通过靶向PD-1的诱导移植免疫耐受和治疗自身免疫疾病的新策略。

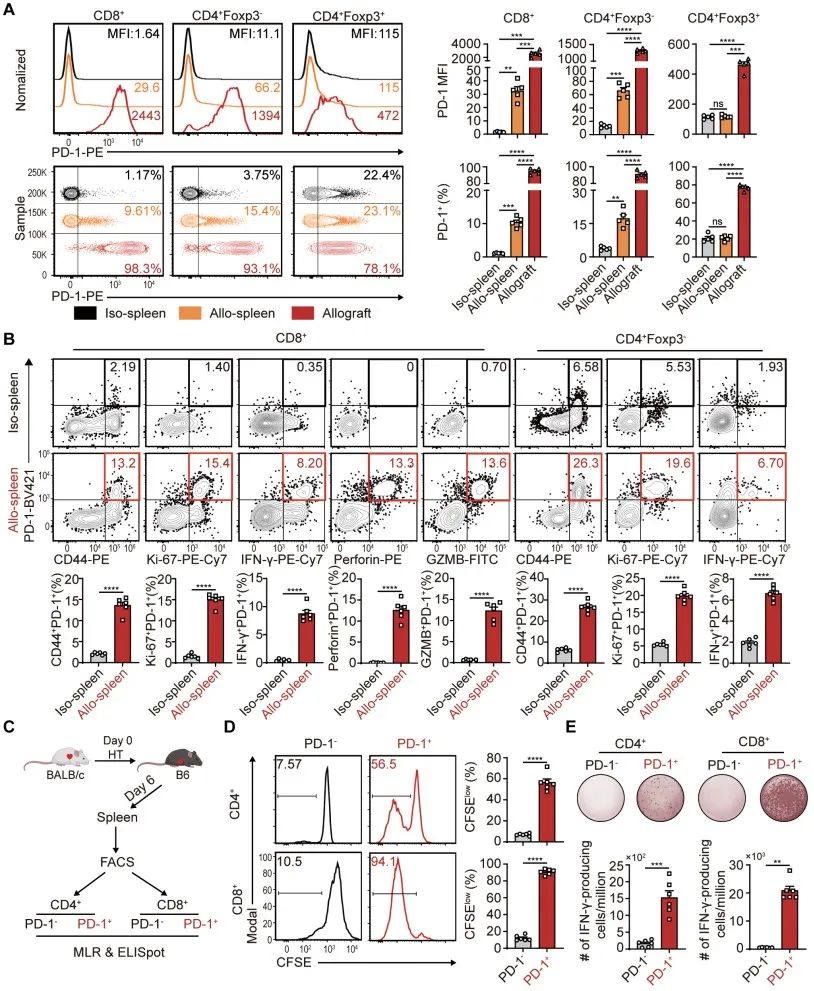
首先,为了筛选外周克隆清除的理想靶点,作者构建了TEa细胞转输的小鼠心脏移植模型,随后通过转录组测序及流式细胞术分析,发现接触同种异体抗原刺激的TEa细胞显著上调PD-1表达。进一步对小鼠心脏移植模型进行流式细胞分析及单细胞转录组联合TCR测序明确了在移植排斥反应中,PD-1在移植物浸润及部分脾脏T细胞上显著高表达,且PD-1的表达与T细胞的克隆扩增状态相关;MLR和ELISpot等实验也证实同种异体反应性T细胞主要存在于PD-1阳性的T细胞中。
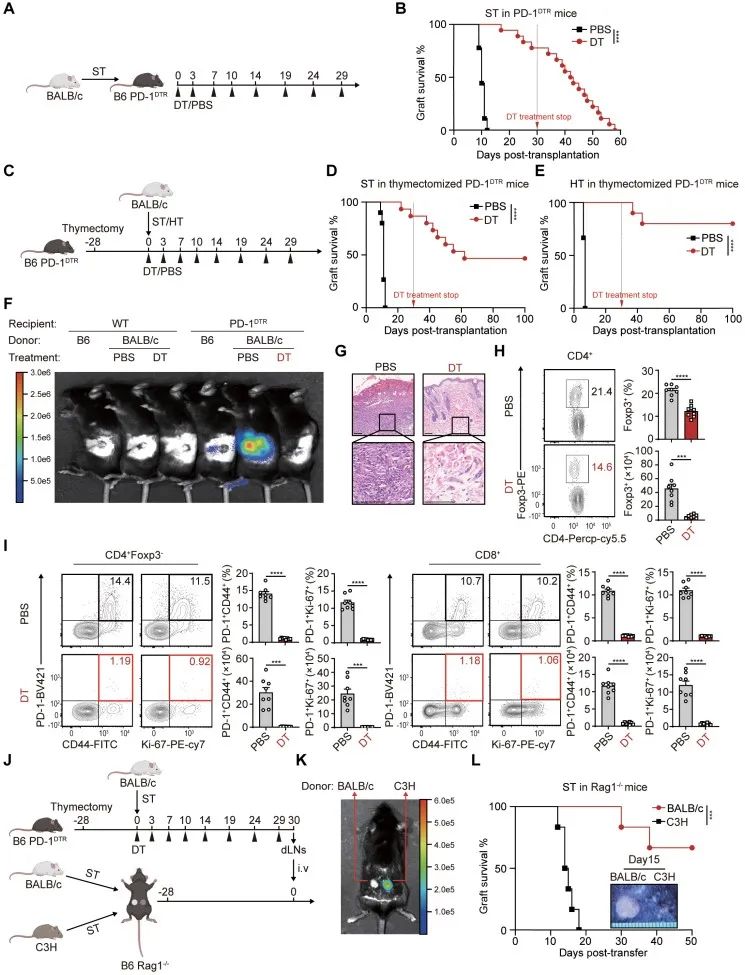
随后,作者设计并构建了一种PD-1DTR小鼠,通过白喉毒素(DT)清除表达PD-1的细胞显著延长了PD-1DTR小鼠的皮肤及心脏移植物的生存期,而联合胸腺切除术以排除胸腺内新产生的TCR克隆的影响后则实现了部分移植物的长期存活。
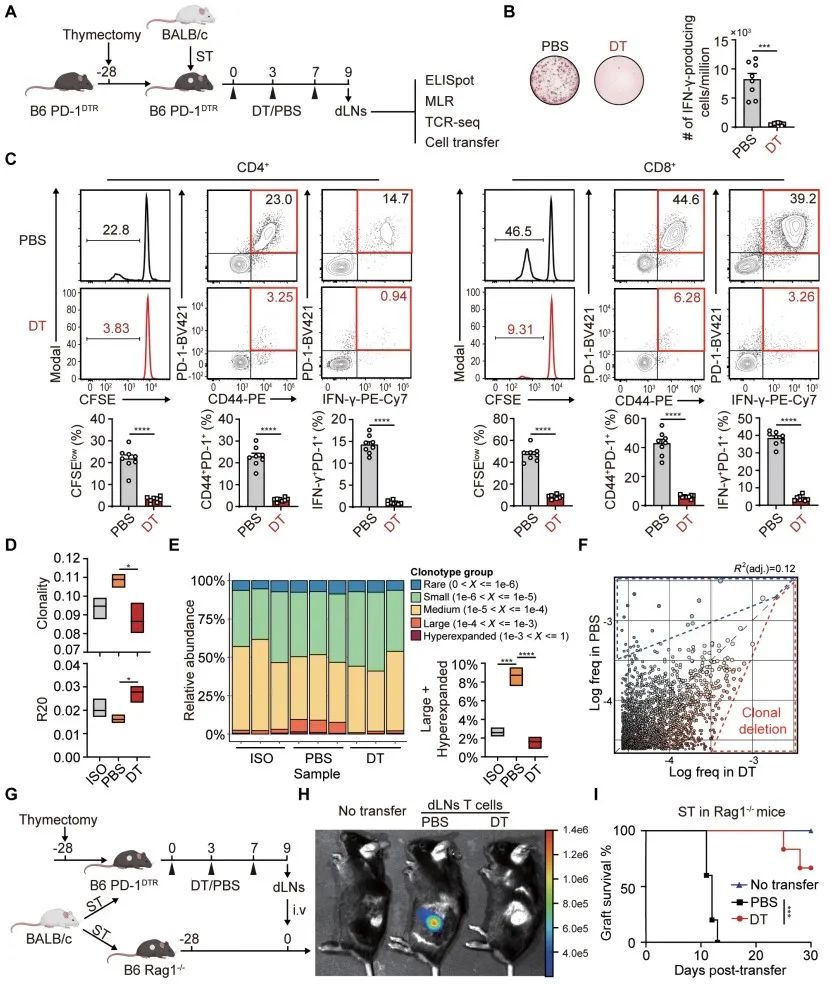
机制上,通过T细胞受体(TCR)测序作者发现通过外周克隆缺失选择性地消除过度扩增的同种反应性T细胞克隆,重塑了TCR库,是一个从外周去除自身反应性T淋巴细胞的过程;细胞过继转输模型进一步证明清除表达PD-1的细胞对移植物的保护作用是供体特异性的。这些结果提示,清除表达PD-1的细胞可以介导同种异体反应性T细胞的外周克隆清除并促进移植耐受形成。
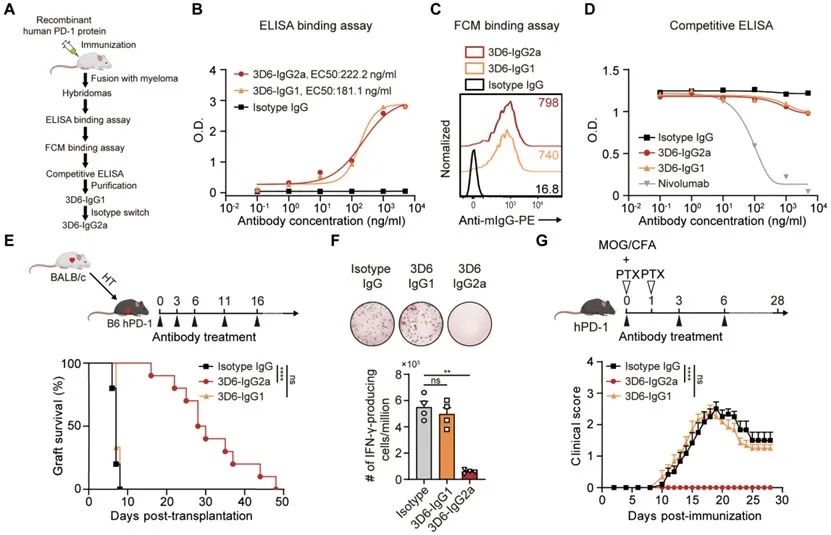
最后,作者构建并筛选出了抗人的PD-1非阻断型清除性抗体(Nonblocking Anti-human PD-1 Depleting Antibody),与癌症免疫疗法中使用的常规PD-1阻断抗体不同,该抗体不干扰PD-1/PD-L1相互作用,而是促进了抗体依赖性细胞毒性(ADCC),导致PD-1表达细胞的清除,并在人源化PD-1小鼠心脏移植中进一步验证了这种方法的治疗潜力。
综上所述,作者系统地证明了清除表达PD-1的细胞通过外周克隆清除促进免疫耐受,开发靶向PD-1表达细胞的新型免疫疗法具有重要意义,通过选择性地清除同种反应性和自身免疫性T细胞,同时保留剩余的T细胞库,这种方法为诱导免疫耐受提供了一种很有前途的策略,而不会出现与传统疗法相关的全局免疫抑制。该研究成果有望开拓治疗器官移植排斥反应及自身免疫性疾病的新靶点,为研发新一代特异性更高的免疫抑制剂奠定基础。
该研究由华中科技大学同济医学院附属协和医院心脏大血管外科夏家红、吴杰教授指导完成。崔济开博士、许恒博士、于济彰博士后、冉栓博士为该论文的共同第一作者。该工作得到了国家自然科学基金重点项目、面上项目、湖北省自然科学基金重点项目及中国博士后科学基金等项目的资助。
原文链接:
https://www.science.org/doi/10.1126/sciimmunol.adh0085
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)