首页 > 医疗资讯/ 正文
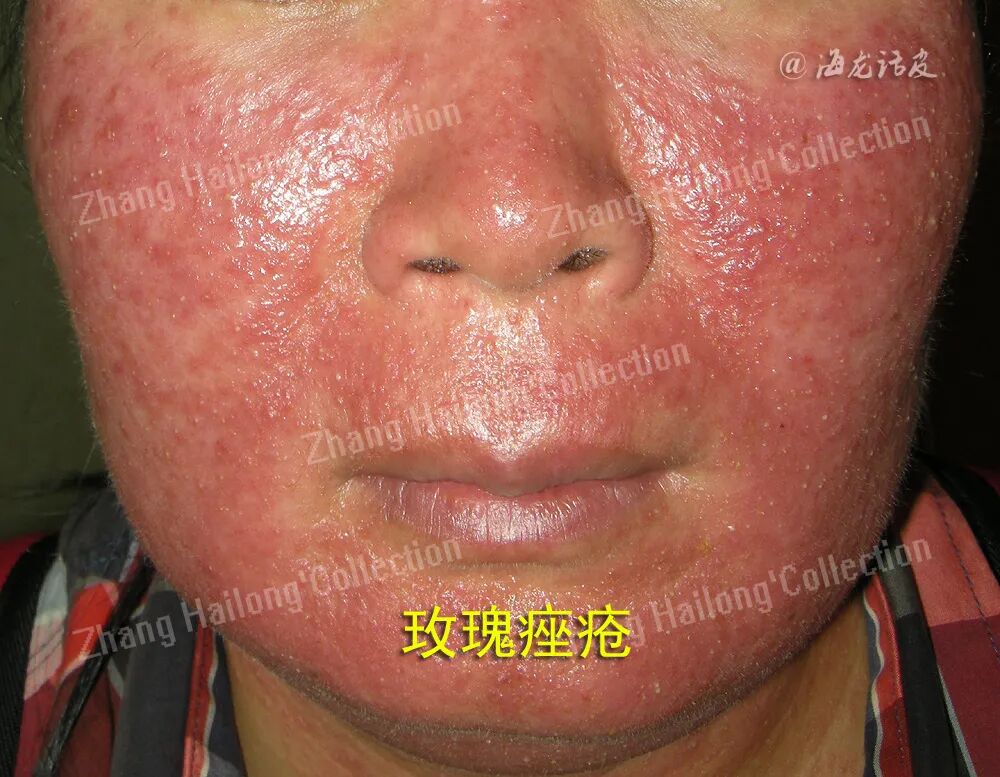
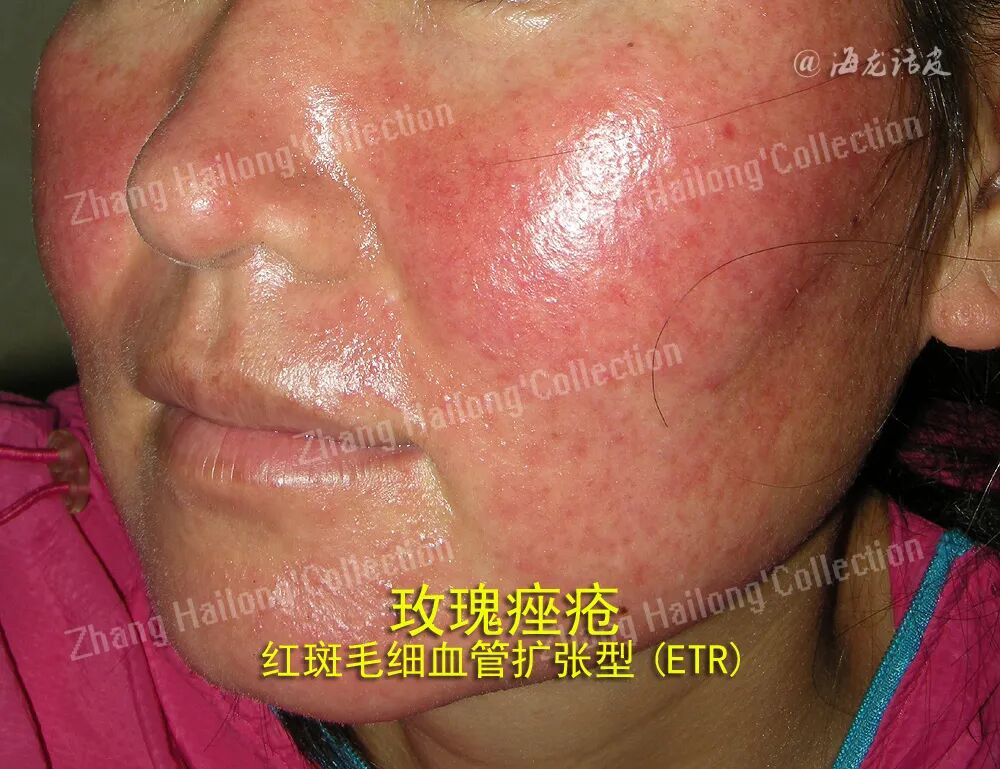
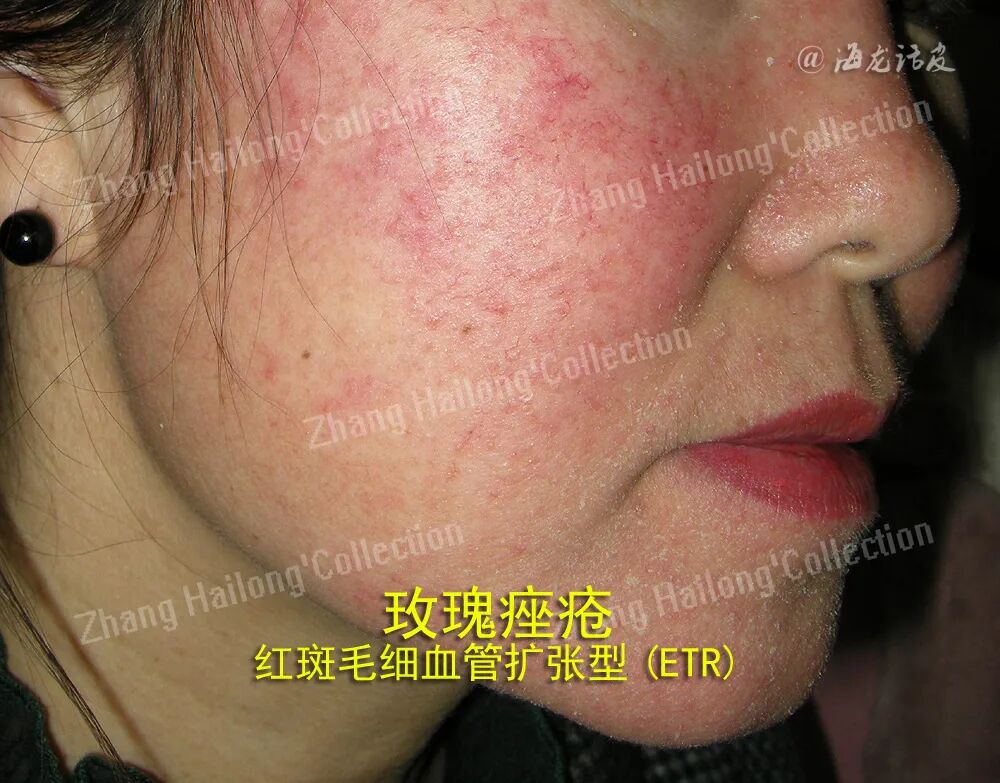
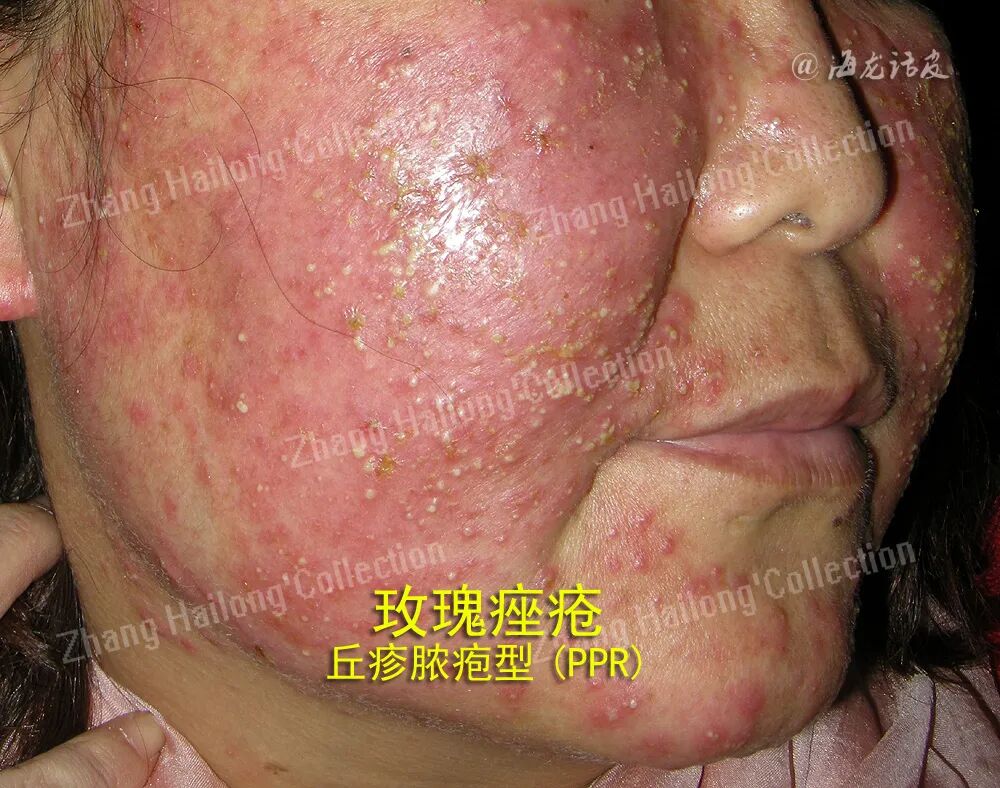
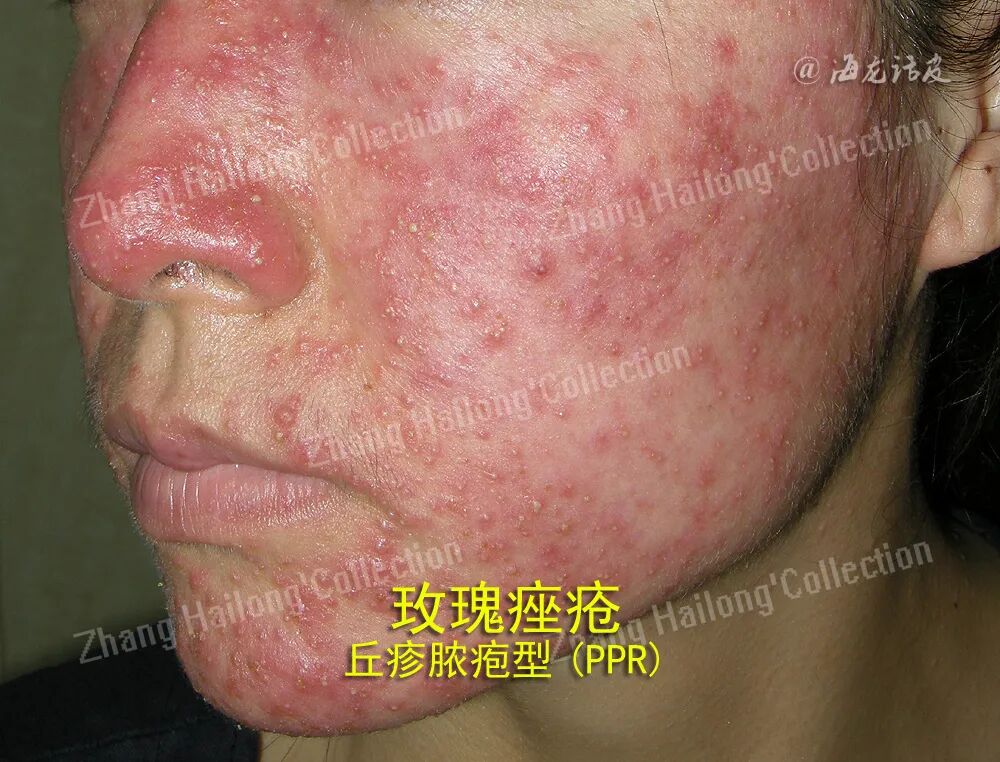
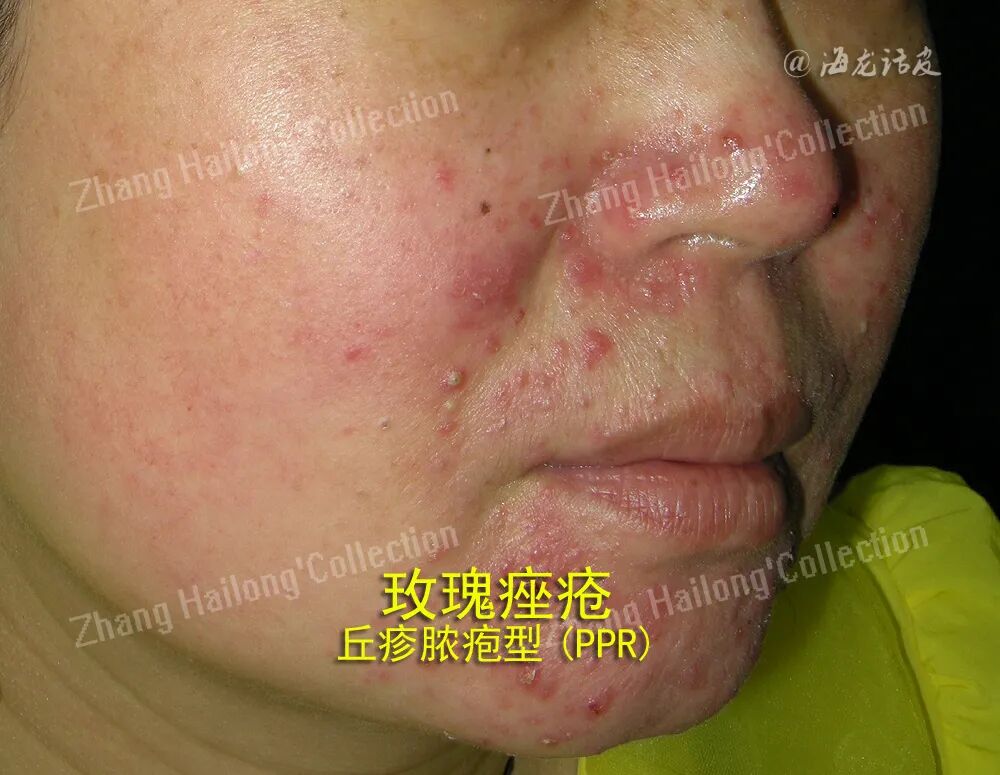
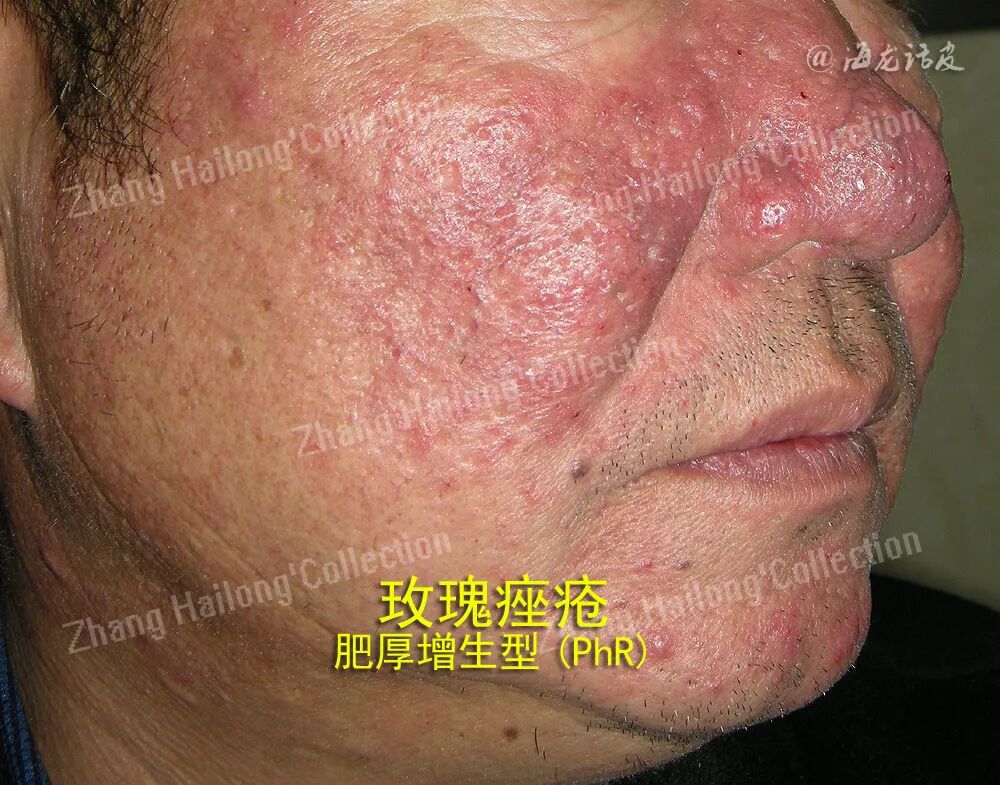
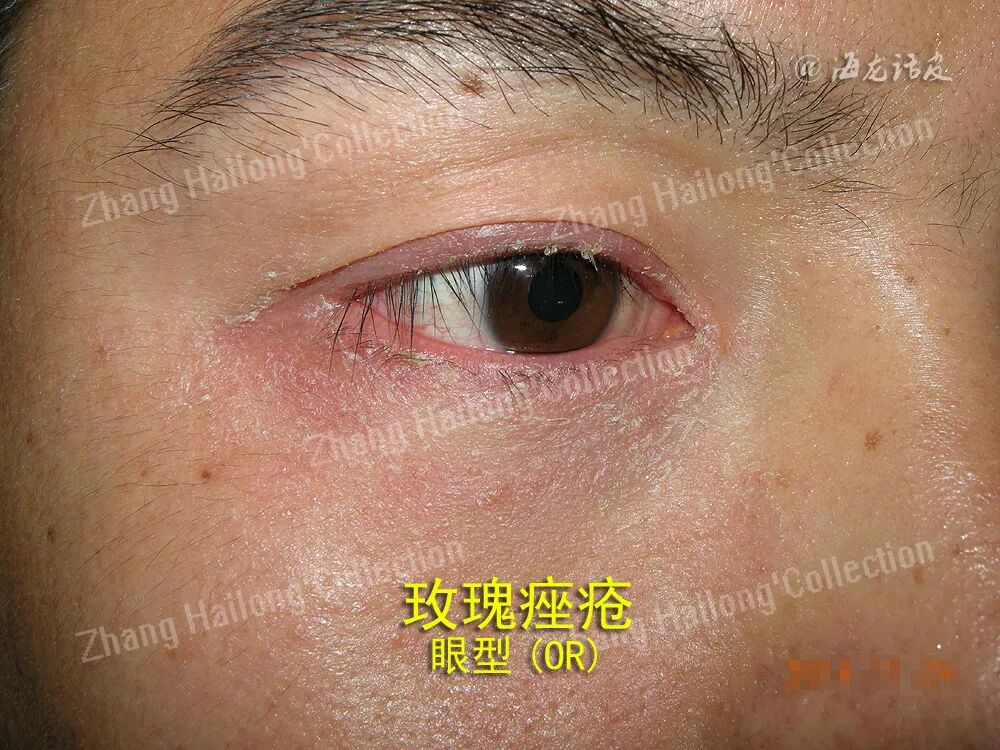
玫瑰痤疮是一种慢性易反复性的炎症性疾病,主要表现为累及面中部的阵发性潮红、持续性红斑及毛细血管扩张,可伴有丘疹脓疱,或出现增生肥大,也可伴发眼部症状,病变中可伴有干燥、瘙痒、紧绷、刺痛感等不适。根据其临床表现可分为四型:红斑毛细血管扩张型(ETR)、丘疹脓疱型(PPR)、肥厚增生型(PhR)及眼型。根据研究结果,内源性因素如遗传因素、精神因素、肥胖,外源性因素如紫外线、微生物感染、吸烟、饮酒等。以上致病因素会通过不同的机制,激活体内先天及适应性免疫,或影响皮肤中神经血管系统的调节功能,参与到玫瑰痤疮的发生发展中。
玫瑰痤疮的治疗一般从以下几方面入手:①皮肤护理(长期使用温和的洁面、保湿修复功能性护肤品及防晒霜);②局部疗法(甲硝唑、溴莫尼定等);③系统疗法(多西环素、羟氯喹等);④激光/光疗法(脉冲染料激光、强脉冲光等);⑤注射疗法(肉毒毒素)等。识别和解决发病机制对于改善玫瑰痤疮治疗的结局至关重要。免疫系统的平衡对于皮肤屏障的完整性具有重要作用。近年来,与玫瑰痤疮发病机制相关的免疫学研究迅速增加,香草素型(TRPV)的瞬时受体电位(TRP)离子通道的异常激活、Toll样受体(TLR)在内的模式识别受体被激活、LL-37(Cathelicidin抗菌肽)和激肽释放酶5(KLK5)的增加及其相互作用、mTORC1信号传导,包括免疫细胞,如:肥大细胞等增加都有促炎和促血管生成作用,也是目前玫瑰痤疮发病机制的研究热点。
1.TRPV(瞬时受体电位香草素亚家族)受体与玫瑰痤疮的相关性
TRPV亚家族,包括TRPV1、TRPV2、TRPM3、TRPV4等,是一类广泛表达在多种细胞类型中的细胞膜离子通道蛋白,它们不仅在神经细胞中有显著表达,如感觉神经元、角质形成细胞、肥大细胞等,也在非神经元的细胞,例如内皮细胞、免疫细胞等中也有所表达。这些成员以其独特的结构和生化特性,参与了多种生理和病理过程,包括天然免疫、促发炎症、感知疼痛和热刺激以及血管调节等生理功能。TRP通道被激活后,可以导致SP(外周神经末 梢释放的P物质)及CGRP(降钙素基因相关肽)等血管活性神经肽释放。这些物质的释放可以引起皮肤血管流量增加、血管扩张和血管通透性增加,引起组织水肿;还能使WBC诱导产生蛋白酶和ROS(活性氧)。TRP和神经肽的表达不仅对血管有调节作用并与玫瑰痤疮中多种炎症过程相关。Sulk M等研究发现TRPV2、TRPV4的皮肤免疫反应性在ETR和PPR中增强,TRPV2与CD68和MC类胰蛋白酶共定位,在玫瑰痤疮发病中上调,在红斑型玫瑰痤疮中观察到免疫细胞和成纤维细胞中TRPV3的免疫染色增加。
另外,Cheng X 等发现TRPV3在32℃~39℃时激活,参与热感觉和角质形 成细胞分化。Pecze L等发现TRPV1可以被辣椒素(“辛辣食物”)、热(>42℃)或在炎症条件下激活。Kim HB等通过从酒渣鼻患者和正常人身上获取了皮肤组织进行体内研究得出结论,TRPV1拮抗剂(辣椒平)可减少玫瑰痤疮LL-37、TNF-α、IL-1α、IL-1β、IL-8和PAR2等神经炎症介质的表达。TRPV亚家族在神经元和非神经细胞中均表达,通过参与天然免疫、促发炎症、感知疼痛和热刺激以及血管调节等多种生理及病理过程,显示出它们在玫瑰痤疮发病中的重要性。因此,进一步探索这些通道如何具体参与玫瑰痤疮的发病机制将会为玫瑰痤疮的治疗提供新的方向。
2.LL-37(Cathelicidin 抗菌肽)与玫瑰痤疮的相关性
LL-37(Cathelicidin抗菌肽)是一种重要的抗菌肽,广泛参与人体的防御机制和疾病调节。近年来,其在玫瑰痤疮(Rosacea)中的研究逐渐增多,成为该领域的一个热点。Cathelicidin是在哺乳动物皮肤中发现的第一个抗菌肽,Cathelicidin在红斑型玫瑰痤疮皮肤中高度表达,并且与增加的丝氨酸蛋白酶活性相结合,其裂解产物LL37可触发许多炎症过程,包括肥大细胞(MC)活化。激肽释放酶5(KLK5)是一种皮肤角质层胰蛋白酶,它参与细胞更新和皮肤屏障功能的调节,与正常皮肤比较,玫瑰痤疮患者皮损部位角质层KLK5表达及活性增强,可将hCAP18裂解使LL37生成异常升高,由此得知LL-37和KLK5是诱导玫瑰痤疮疾病发生发展的核心蛋白。郑峥妮等将LL37注射至小鼠剃毛后背部成功建立小鼠玫瑰痤疮炎症模型,通过RT-qPCR得出结果,造模小鼠皮损的玫瑰痤疮发病机制通路关键因子(TLR-2、cAMP、KLK-5)、炎症因子(IL-1β、IL-6、TNF-α)、肥大细胞相关因子(MMP-9)、CD4+T细胞相关因子(IFN-γ、STAT1、CCR5、STAT3)及微血管增生因子(VEGF)表达量均升高证实LL37是玫瑰痤疮的炎症发生过程中的关键靶向之一。
冯春梅等研究人员通过小鼠实验验证了OA(Oroxylin A是一种中药)能有效抑制LL-37产生的ROS的产生,以及随后NF-κB信号通路的激活,进而使玫瑰痤疮患者病症改善。李阳帆等通过研究结果确定并验证了二甲双胍通过抑制LL37和TNF-α诱导角质形成细胞中ROS产生和MAPK-NF-κB信号激活,进而抑制炎症反应和红斑型玫瑰痤疮的血管生成来缓解病理症状,是红斑型玫瑰痤疮的新型治疗候选药物。有研究证明,SSA(超分子水杨酸)可以抑制LL-37的产生、秋水仙碱可以在体内抑 制TLR2和LL37的结合、卡维地洛通过降低TLR2的表达而进一步降低了KLK5分泌和LL-37的表达,它们通过这些机制最终抑制了玫瑰痤疮的炎症反应。总之,LL-37作为玫瑰痤疮中一个关键的分子,通过促进炎症、血管生成和免疫调节等多种机制影响玫瑰痤疮的发展。探索LL-37在玫瑰痤疮中的作用机制及其潜在的治疗方法,以期为玫瑰痤疮等慢性炎症性皮肤病的治疗提供新的思路和手段。
3.TOLL样受体与玫瑰痤疮的相关性
天然免疫系统,作为生物体抵抗外来侵袭的第一道防线,对于识别并迅速响应各种高危致病因子至关重要。其中,TOLL样受体(TLR)是这一防御机制中的关键模式识别受体。TLR家族包括多个成员,TLR2在识别病原体和触发免疫反应中发挥着核心作用。尤其TLR2在玫瑰痤疮等疾病中 的过度表达及其功能的激活引起了广泛关注。TLR2是一种重要的先天免疫受体,能够感知到病原体、自身抗原等多种刺激物,从而促进炎细胞因子、趋化因子的释放,进而导致血管高反应性。有关研究证实,TLR2mRNA在玫瑰痤疮患者皮损中表达显著高于健康对照组,并揭示了KLK5的表达可由TLR2通过钙依赖性途径促进,KLK5可进一步增加LL-37的表达,这表明,TLR2信号传导在玫瑰痤疮中扮演了关键角色。Colombo S等开发了一种靶向TLR2的小RNA干扰(siRNA),并在活性赋形剂(如甘油/尿素)存在的情况下将乳化siRNA应用于小鼠耳朵的内表面和外表面。这导致TLR2水平显著降低,表明siRNA有可能在转录水平上管理玫瑰痤疮。
有研究证明,SSA(超分子水杨酸)通过减少炎症细胞浸润,抑制与玫瑰痤疮相关的Toll样受体2、基质金属肽酶9、激肽释放酶5、LL-37的产生来治疗玫瑰痤疮。袁昕等研究证明秋水仙碱可以通过抑制TLR2通路激活的中性粒细胞炎症来缓解玫瑰痤疮症状。张佳雯等通过小鼠实验证明卡维地洛可通过抑制巨噬细胞上表达的TLR2水平进而治疗玫瑰痤疮。李健、金东熙等通过临床实验证明卡维地洛对于患有面部潮红和红斑的玫瑰痤疮患者来说是一种有效且安全的治疗选择。Toll样受体在玫瑰痤疮的发病机制中扮演了核心角色。这提示了在治疗玫瑰痤疮中,靶向调控Toll样受体及其下游信号通路可能具有重要的应用前景。通过对TLR2等受体的深入理解,可以为玫瑰痤疮的预防和治疗提供新的策略和靶向。
4.mTORC1信号传导与玫瑰痤疮的相关性
mTORC1是一种丝氨酸/苏氨酸蛋白激酶,负责调控细胞生长、分裂和能量代谢等多个方面,当mTORC1被激活时,它会激活其下游的信号传导途径,这些途径进一步调控细胞的生物化学过程,如蛋白质、脂质和核苷酸的合成,以及细胞的分化和死亡。因此,mTORC1是免疫功能的重要调节剂。LL37通过与TLR2结合激活mTORC1信号传导,这一过程不仅增加了cathelicidin在角质形成细胞中的表达,而且TLR刺激可激活先天免疫,导致核因子-κB(Nuclear factor-κB,NF-κB)信号转导的受控激活,随后产生细胞因子、趋化因子和组织素以防御宿主,进一步产生LL37,mTORC1信号转导的过度激活促进和加重了玫瑰痤疮的发展。
Deng Z等通过小鼠实验验证了mTOR抑制剂雷帕霉素可以减弱LL37诱导的玫瑰痤疮样小鼠皮肤中Cathelicidin的表达增加,进而减轻玫瑰痤疮病症发展。因此,上皮mTORC1缺失或体内mTORC1信号抑制可以预防玫瑰痤疮的病理变化,有效缓解疾病发展。mTORC1信号传导的激活与NF-κB信号激活、LL37的增加之间的相互作用,也为理解疾病发生中的细胞信号转导提供了一个新视角。Celastrol是一种植物来源的药物,具有抗炎和抗氧化活性,可作为调节炎症和血管生成的另一种潜在药物,曾庆宇等通过研究证明该药物通过抑制Ca2+-CaMKII依赖性mTOR-NF-kβ信号转导通路发挥治疗玫瑰痤疮症状的作用。未来需要更多的研究来深入了解这一相互作用的具体机制及其在疾病中的作用,以便开发新的治疗策略。
5.肥大细胞与玫瑰痤疮的相关性
肥大细胞(MCs)也是目前研究玫瑰痤疮发病机制的热点,肥大细胞是骨髓来源的细胞,作为未成熟的造血祖细胞循环,到达驻留组织后局部成熟,MC激活后,通过释放促炎细胞因子、趋化因子、蛋白酶和抗菌肽来吸引其他免疫和炎症介质,导致血管舒张、血管生成和组织纤维化。Aroni K等的一项研究表明,在ETR和PPR患者中,病变中MC的数量明显高于临床上未受累的皮肤,并且MC密度与玫瑰痤疮病发持续时间之间存在正相关。Metcalfe D及其同事进一步扩展了这一发现,证明缺乏MCs的小鼠在注射与酒渣鼻有关的抗菌肽Cathelicidin LL-37(LL-37)后不会发生炎症。
MCs可以通过释放多种炎症因子和介质来促进炎症反应,包括但不限于基质金属蛋白酶(Matrix Metalloproteinase,MMPs)、白细胞介素(Interleukin,IL)、转化生长因子(Transforming growth factor,TGF-beta)、肿瘤坏死因子(Tumor necrosis factor,TNF-α)和血管内皮生长因子(Vascularendothelial growth factor,VEGF)。这些物质不仅能够募集和激活中性粒细胞,还能进一步激活MCs,放大其炎症反应的效应。另外,MCs也是LL-37、激肽释放酶5(KLK5)及组胺的主要来源之一,这些物质均为玫瑰痤疮发病机制中的重要物质。
因此,肥大细胞在玫瑰痤疮的发病过程中发挥着至关重要的作用,涉及到炎症因子的产生、炎症细胞的募集以及血管通透性的增加等多个方面。有研究证明,特定波长低能量IPL可以稳定MC膜,通过抑制MC激活来减少MMP-9、KLK5和Cathelicidin的分泌,并进一步缓解酒渣鼻炎症反应。Choi JE及其同事发现A型肉毒毒素可以通过阻断肥大细胞脱颗粒进而用于治疗玫瑰痤疮。He G等通过纳入22项临床应用肉毒毒素治疗玫瑰痤疮研究(包含720例病例),证明肉毒杆菌毒素在玫瑰痤疮中发挥的作用有抑制肥大细胞脱颗粒的功能,当然还可以阻止乙酰胆碱和神经肽的释放,抑制TLR2、LL-37功能,从而阻断相关介质的释放,抑制炎症和病理性血管生成,进而治疗玫瑰痤疮。临床应用的有效性证明针对肥大细胞的治疗策略对于改善玫瑰痤疮的临床症状和预防病情恶化具有重要意义。研究对于肥大细胞更有效的干预措施以开发出针对玫瑰痤疮的治疗方法是一种治疗新趋向。
6.小结
本文对玫瑰痤关于免疫应答失调和神经血管功能障碍方面等热点发病机制进行了详细阐述,证明了主要致病机制之间的复杂性及相互联系性,引起玫瑰痤疮发展的恶性循环。探索参与玫瑰痤疮发病机制的核心分子可能会开发出解决该疾病根本原因的药物。目前,玫瑰痤疮的发生机制仍具有不明确性,临床病症反复发作增加了治疗的难度。因此,玫瑰痤疮的发病机制仍需要进一步深入探索,从而更好地帮助确定这种疾病的新治疗靶点。
参考文献:
1.高峰,孙立.玫瑰痤疮的发病机制及其相关治疗新进展[J].中国美容医学,2025,34(11):194-197.
2.中国医师协会皮肤科分会注射美容学组,广东省医师协会皮肤科医师分会皮肤美容与外科学组,于波.肉毒毒素注射在皮肤美容中应用的专家共识(2023版)[J].中国美容医学,2023,32(11):1-9.
3.杨乐妍,张翰林,唐珂韵.玫瑰痤疮的发病机制、合并症及相关研究进展[J].中国美容医学,2022,31(10):187-190.
4.其他文献略。
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)