首页 > 医疗资讯/ 正文
CD47是一种表达于正常细胞表面的“勿食我”信号分子,通过与髓系细胞上的信号调节蛋白α(SIRPα)结合,向巨噬细胞发出抑制吞噬的信号,帮助细胞逃避免疫清除。肿瘤细胞常通过高表达CD47,逃避机体免疫系统的识别和清除。阻断CD47-SIRPα通路因此成为近年来肿瘤免疫治疗的一个热点策略。然而,现有的CD47抑制剂在临床开发中面临“靶点相关毒性”如严重贫血和活性不足的挑战,限制了其应用。

研究团队通过大规模结构导向的SIRPα胞外域突变体库筛选,设计出带有六处特异突变的SIRPα变体,再与人IgG4 Fc融合,形成HCB101。该融合蛋白结合CD47的能力及其特异性通过多项体外实验得到验证,包括与人类及恒河猴CD47的亲和力测定、肿瘤细胞系上的结合特异性,以及阻断SIRPα-Fc与CD47结合的竞争实验。HCB101对巨噬细胞吞噬肿瘤细胞的促进作用进行了比较分析,并与现有药物比较其对红细胞的结合及诱导吞噬的能力。多种人源肿瘤异种移植(CDX)动物模型被用于评估其体内抗肿瘤效力,并开展与抗HER2及抗EGFR单抗的联合治疗研究。非人灵长类动物模型用于安全性和药代动力学分析。
结果显示,HCB101对人类及恒河猴CD47显示了极高的结合亲和力,且特异性强,能有效阻断SIRPα-Fc与CD47的结合。其介导的巨噬细胞吞噬肿瘤细胞能力远超TTI-622,且与Hu5F9-G4相当。与Hu5F9-G4相比,HCB101对红细胞的结合亲和力明显降低,且不诱导红细胞吞噬,提示更佳的安全性。 在多种肿瘤模型中,HCB101表现出显著的肿瘤生长抑制作用(TGI),剂量依赖性明显。包括Raji、Daudi、KG-1a、NCI-H82、WiDr、MDA-MB-453和SNUC1等模型均证实其强效抗肿瘤活性。特别是在NCI-H82肿瘤模型中,HCB101单药治疗可使肿瘤体积降至零,显著优于Hu5F9-G4。与其它CD47抑制剂相比,HCB101在WiDr模型中表现出更优的效果。 联合抗HER2单抗曲妥珠单抗及抗EGFR单抗西妥昔单抗时,HCB101展示出协同抗肿瘤效果,显著提升抗体依赖性吞噬作用(ADCP)。
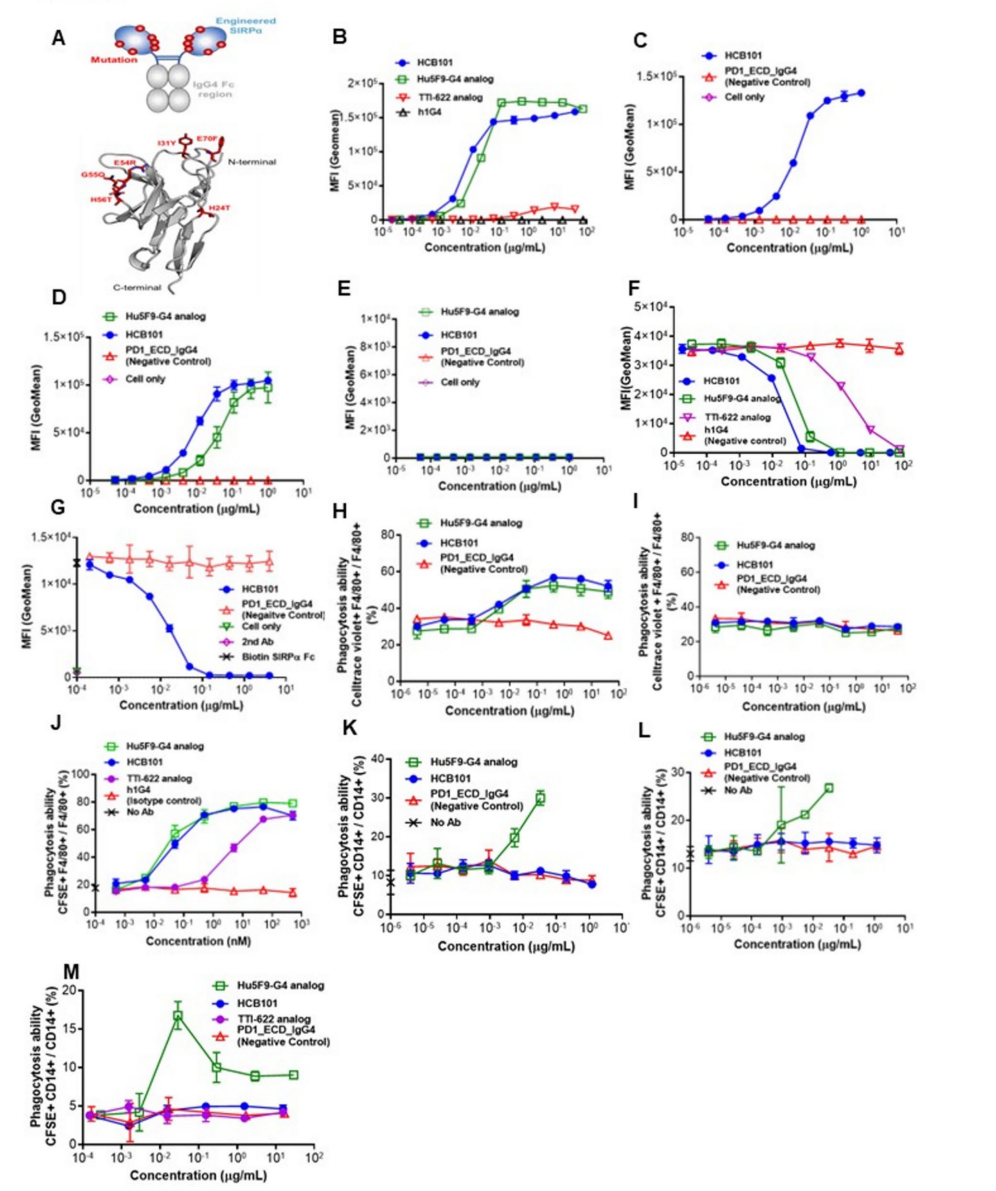
图:HCB101的结构与体外活性分析
此外,HCB101治疗显著提高肿瘤微环境中M1型巨噬细胞与M2型巨噬细胞的比例,表明其可能促进肿瘤相关巨噬细胞向促炎表型转化,改善肿瘤免疫微环境。 在小鼠及非人灵长类动物中,HCB101未观察到剂量限制性毒性及显著的血液学不良反应。药代动力学显示剂量依赖性良好,且有效达到靶标占有率,支持进一步临床开发。
总之,HCB101通过优化结构减少了对红细胞的结合与抗原库效应,显著提升了安全性和可用剂量,突破了CD47-SIRPα通路阻断剂以往存在的疗效与毒性难以兼顾的瓶颈。其强效抗肿瘤活性、良好的安全性及改善肿瘤微环境免疫状态的能力,使其成为未来实体瘤及血液肿瘤免疫治疗的有力候选药物。
原始出处
Wang, JT., Tseng, CL., Teng, HF. et al. HCB101: a novel potent ligand-trap Fc-fusion protein targeting the CD47-SIRPα pathway with high safety and preclinical efficacy for hematological and solid tumors. J Hematol Oncol 18, 87 (2025). https://doi.org/10.1186/s13045-025-01742-x
本文相关学术信息由梅斯医学提供,基于自主研发的人工智能学术机器人完成翻译后邀请临床医师进行再次校对。如有内容上的不准确请留言给我们。
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)