首页 > 医疗资讯/ 正文
2025年10月6日17点30分,2025年诺贝尔生理学或医学奖揭晓。Mary E. Brunkow、Fred Ramsdell 与 Shimon Sakaguchi获奖,以表彰在“外周免疫耐受”领域的重要贡献。

人类的免疫系统每天都在抵御成千上万种试图入侵的微生物。这些病原体形态各异,且许多在进化过程中发展出“伪装”策略——通过模拟人体自身细胞的分子特征,逃避免疫识别。那么,免疫系统如何在精准清除外来威胁的同时,避免误伤自身组织?这一关键问题的答案,正是2025年诺贝尔生理学或医学奖的核心所在。
Mary E. Brunkow、Fred Ramsdell 与 Shimon Sakaguchi 因其在外周免疫耐受领域的开创性研究,荣获2025年诺贝尔生理学或医学奖。他们共同揭示了免疫系统中一群至关重要的“安全卫士”——调节性T细胞(regulatory T cells, Tregs),这类细胞专门负责抑制过度免疫反应,防止免疫系统攻击人体自身组织。
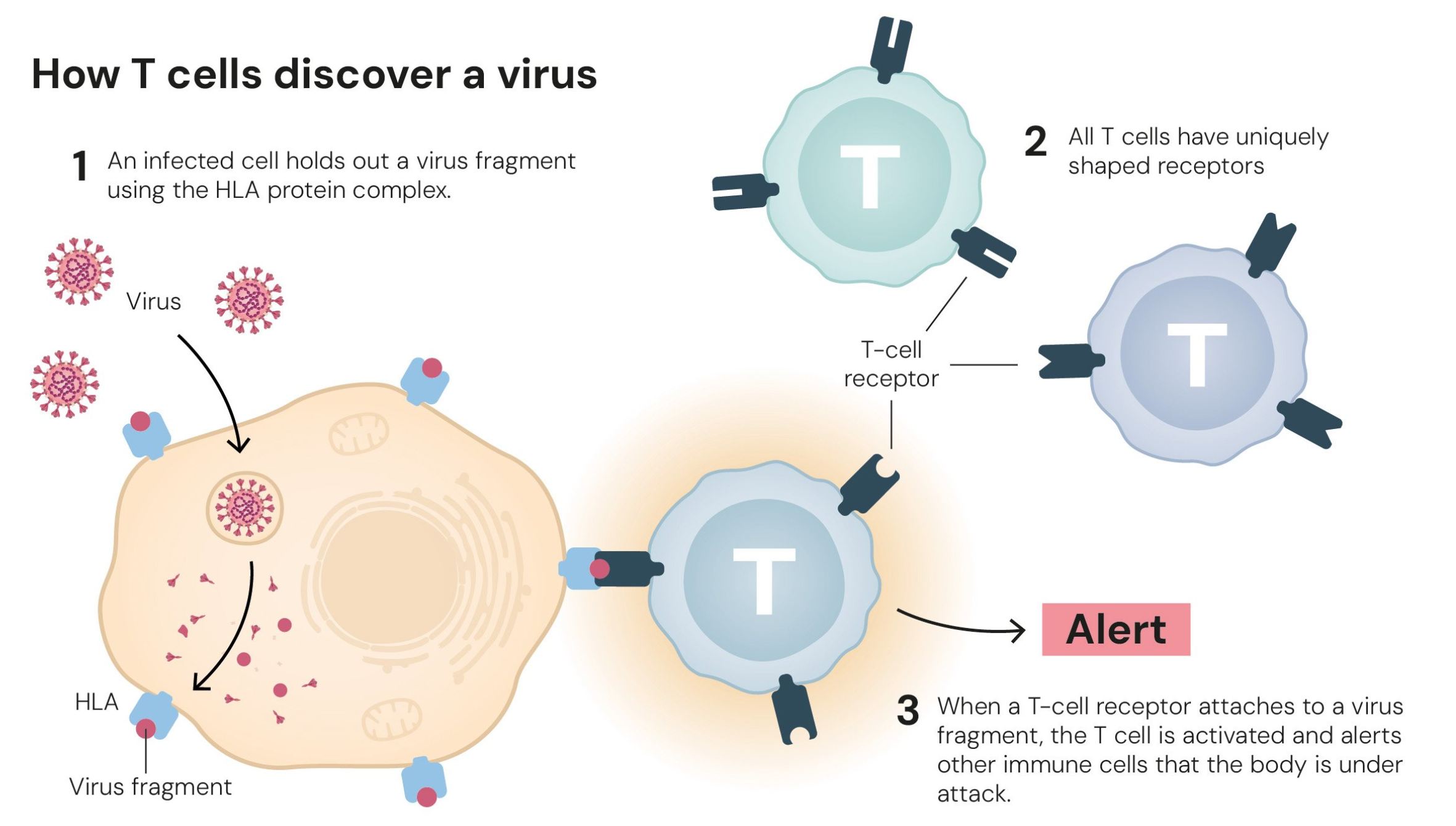
诺贝尔委员会主席 Olle Kämpe 表示:“他们的发现彻底改变了我们对免疫调控机制的理解。正是这些机制,解释了为何大多数人并未罹患严重的自身免疫性疾病。这一成果具有里程碑意义。”
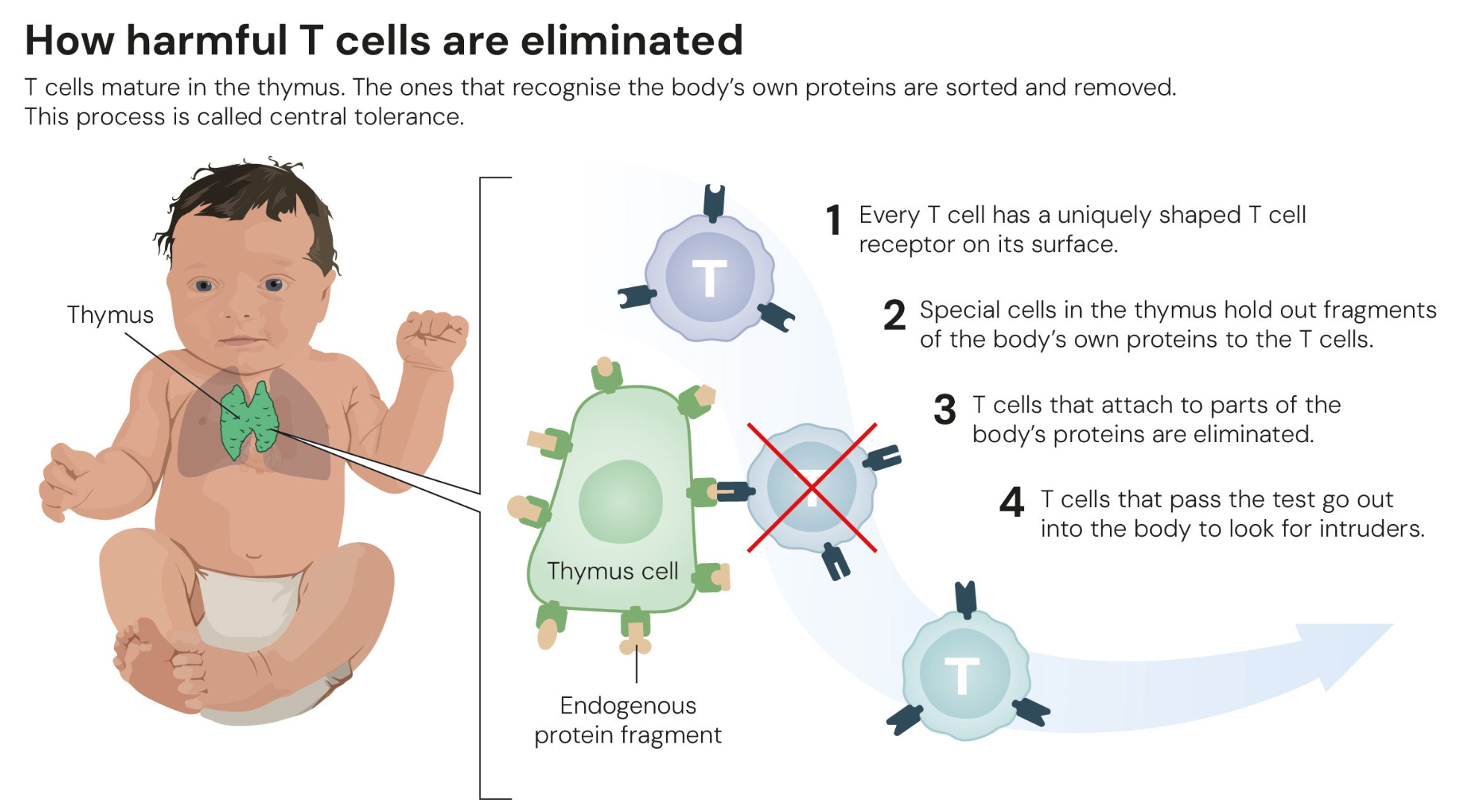
1995年,Shimon Sakaguchi 的研究突破了当时的主流认知。彼时,科学界普遍认为免疫耐受主要依赖于“中枢耐受”机制——即在胸腺中清除可能攻击自身组织的T细胞。然而,Shimon Sakaguchi 发现,即使经过胸腺筛选,仍有一部分潜在致病性T细胞进入外周组织。他首次识别出一类具有免疫抑制功能的T细胞亚群,能够主动维持免疫系统的自我耐受。这一发现为“外周免疫耐受”概念奠定了基础。
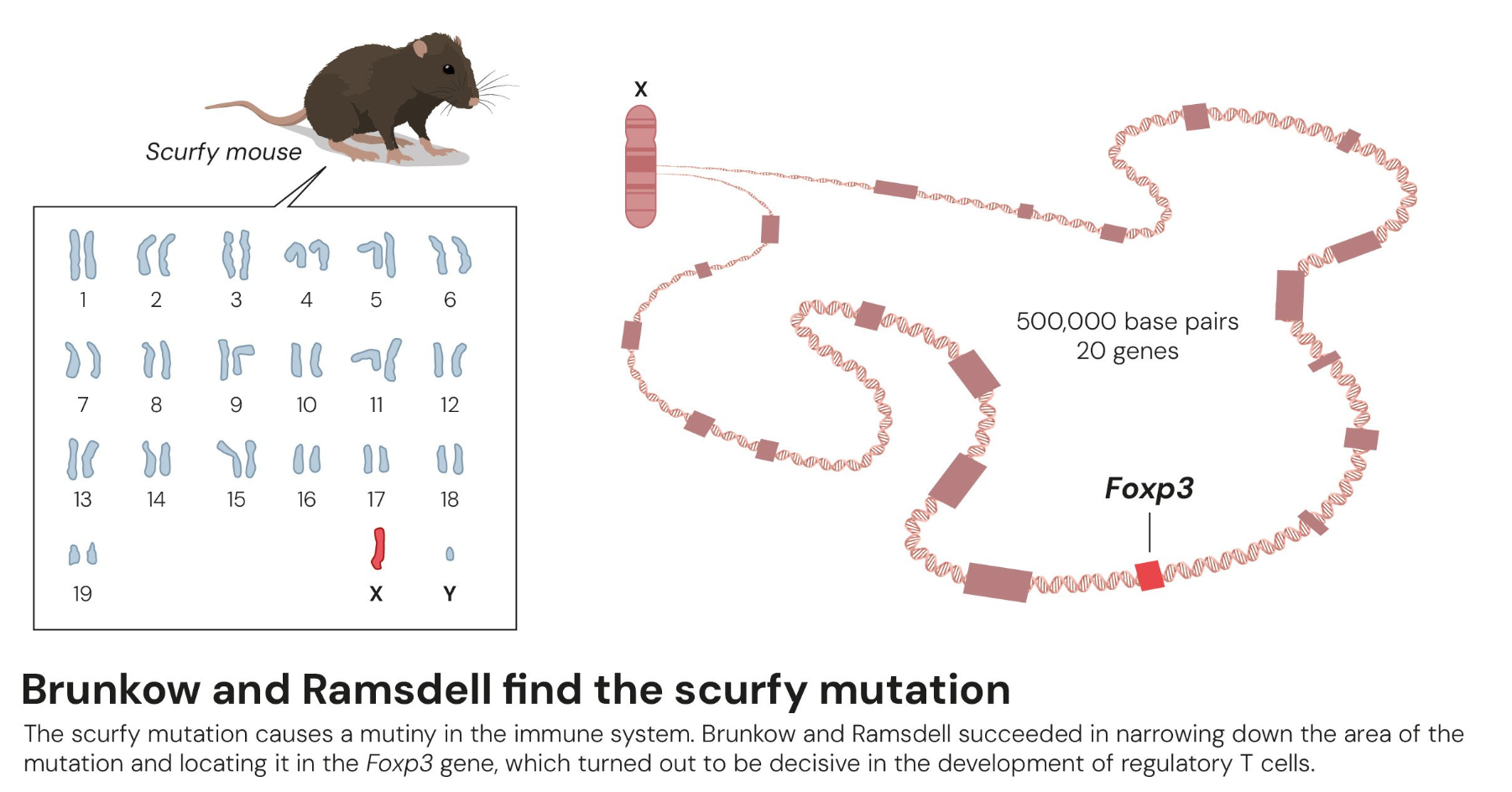
2001年,Mary E. Brunkow 与 Fred Ramsdell 在研究一种易患多器官自身免疫病的小鼠模型时,发现其病因源于一个关键基因的突变。他们将该基因命名为 Foxp3。进一步研究表明,人类中同源基因的突变会导致一种罕见但致命的遗传性自身免疫病——IPEX综合征(免疫失调、多内分泌病、肠病、X连锁),这证实了Foxp3在免疫调控中的核心作用。
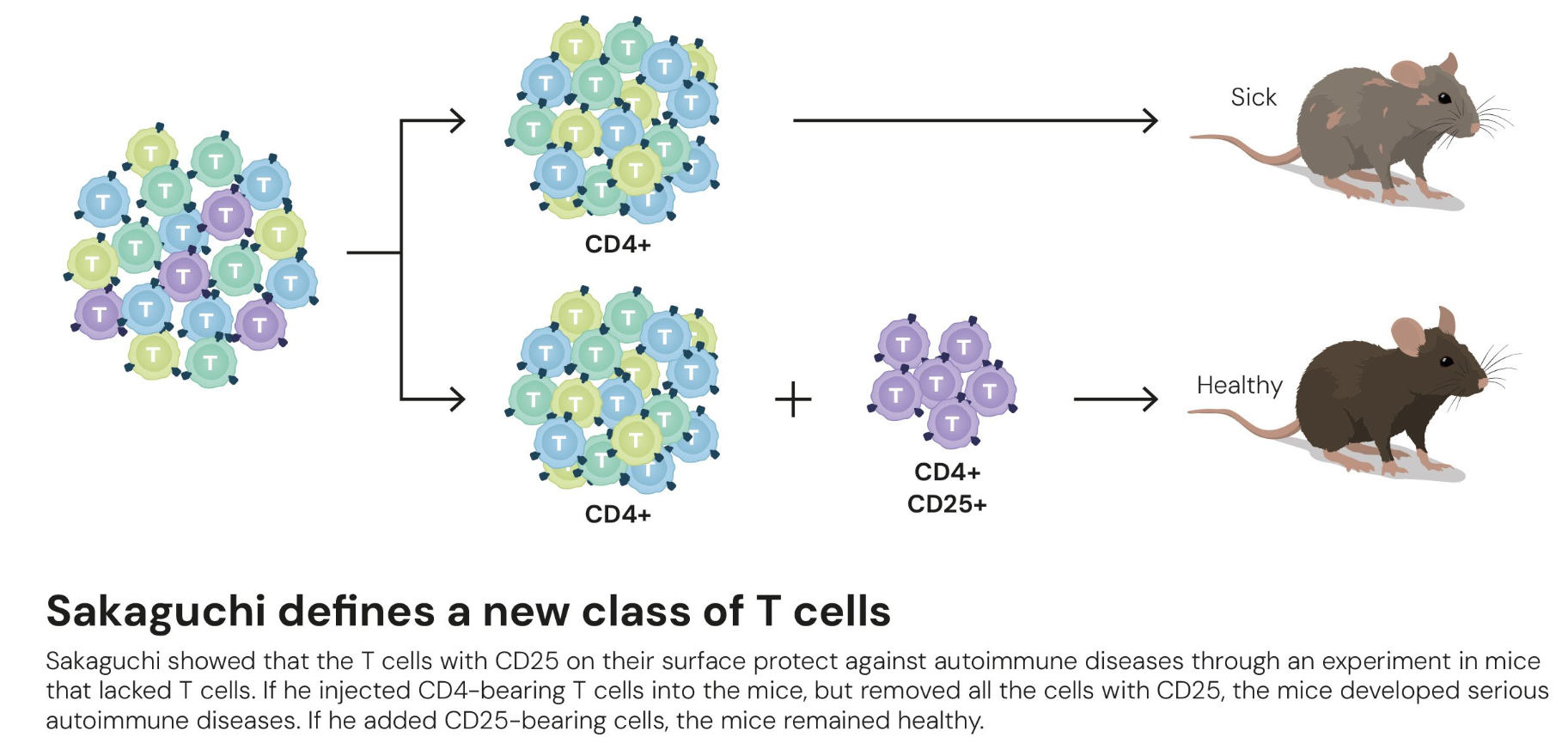
两年后,Shimon Sakaguchi团队将这两项发现成功整合:他们证明,Foxp3 是调节性T细胞发育与功能的“主控开关”。缺乏Foxp3的小鼠无法生成功能性Tregs,从而迅速发展为全身性自身免疫反应。这一关联性研究不仅确立了Tregs的分子基础,也标志着调节性T细胞从表型识别走向功能与机制的全面解析。
如今,调节性T细胞已被公认为免疫稳态的核心调控者。它们在全身巡逻,持续监控其他免疫细胞的活性,确保免疫反应精准、适度,避免“友军误伤”。
三位科学家的奠基性工作,不仅开创了“外周免疫耐受”这一重要研究领域,更深刻影响了现代医学的发展方向。基于Tregs的疗法正在被积极探索,用于治疗自身免疫病(如1型糖尿病、类风湿关节炎)、预防器官移植排斥反应,甚至调控肿瘤微环境以增强抗癌免疫。目前,多项以扩增或回输调节性T细胞为核心的临床试验已取得积极进展。
从基础发现到临床转化,Mary E. Brunkow、Fred Ramsdell 与 Shimon Sakaguchi的研究,展现了科学探索如何一步步揭开生命最精妙的平衡机制——在防御与自稳之间,守护人类健康。
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)