首页 > 医疗资讯/ 正文
溃疡性结肠炎(UC)是一种慢性炎症性肠病,患者常表现为腹痛、腹泻、甚至大出血,严重影响生活质量。尽管现代医学在UC的诊断和治疗上取得了进展,但目前仍缺乏完美疗法,部分患者对现有药物响应不佳,且副作用明显。因此,寻找更加安全有效的治疗手段成为当前研究的热点。
沉香(Lindera aggregata)作为传统中药材,历史悠久,广泛用于消化系统疾病的治疗。其复方及提取物曾显示出抗炎和保护肠道的潜力,但具体的活性成分及机制尚不明朗。异靛内酯(Isolinderalactone, ILDL)是沉香中一种特征性的倍半萜内酯类化合物,既往研究多聚焦于其抗癌作用。近来,研究团队将视角转向其在炎症性疾病中的潜力,尤其是溃疡性结肠炎。

为了系统评估ILDL的抗炎效应,研究首先采用LPS诱导的RAW264.7巨噬细胞炎症模型,筛选沉香中活性组分的抗炎效果。随后,选用经典的DSS诱导急性溃疡性结肠炎小鼠模型,深入观察ILDL在体内的保护作用和改善肠道病理表现的能力。
ILDL对巨噬细胞的多重调控作用
实验结果表明,ILDL能够显著抑制巨噬细胞的M1极化,即减少促炎细胞因子的释放,如TNF-α,IL-6等,同时不影响M2极化的抗炎表型,展现出良好的免疫调节能力。此外,ILDL促使巨噬细胞增强对凋亡肠上皮细胞的清除能力,这一效应有助于维持肠道屏障的完整性,防止炎症扩散。
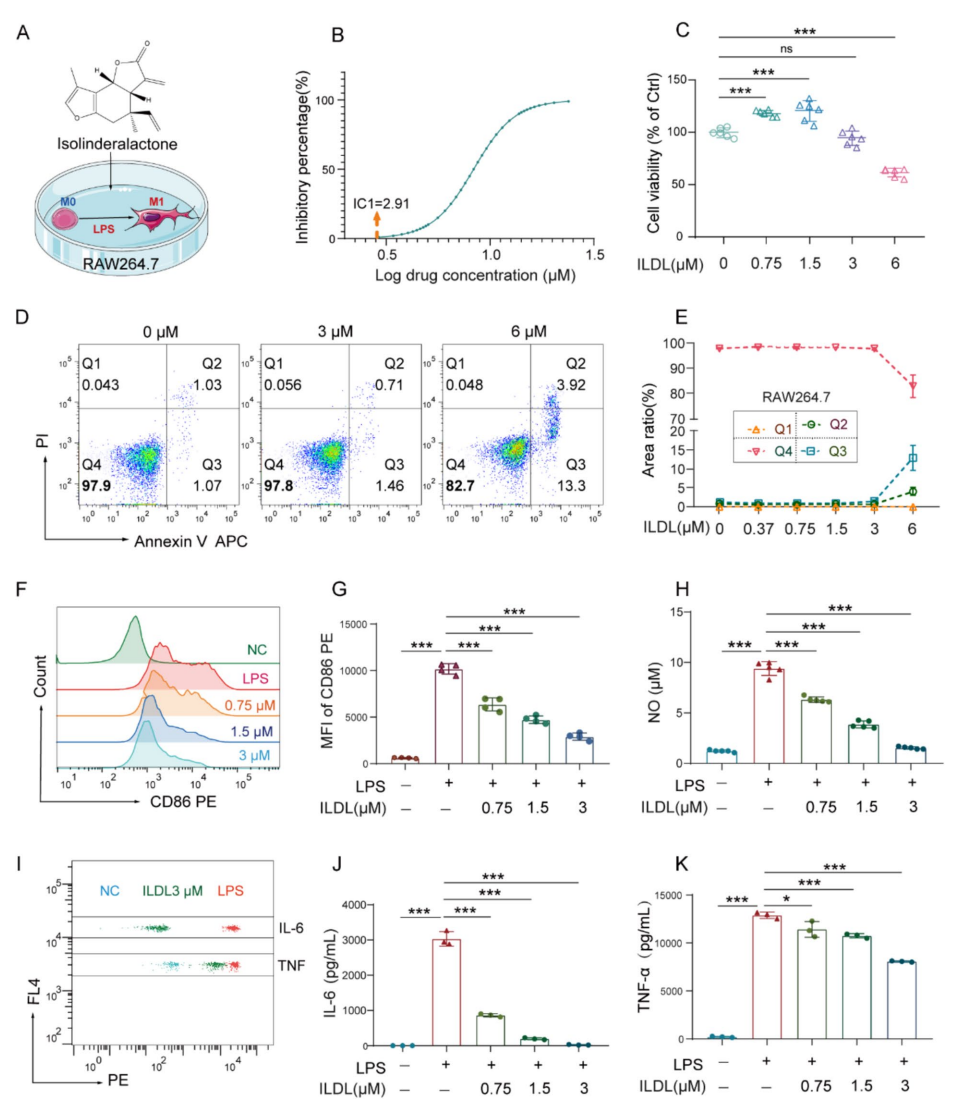
图:ILDL有效抑制巨噬细胞M1极化及炎症介质的产生
LXRα信号通路的关键角色
通过转录组学分析,研究发现ILDL的抗炎效应高度依赖于核受体LXRα(Liver X receptor alpha)通路的激活。ILDL直接结合LXRα,增强其靶基因ABCA1等的表达。进一步的遗传和药理学抑制实验确认,失去LXRα功能后,ILDL的抗炎作用几乎完全丧失,证明ILDL通过激活LXRα通路发挥核心治疗作用。
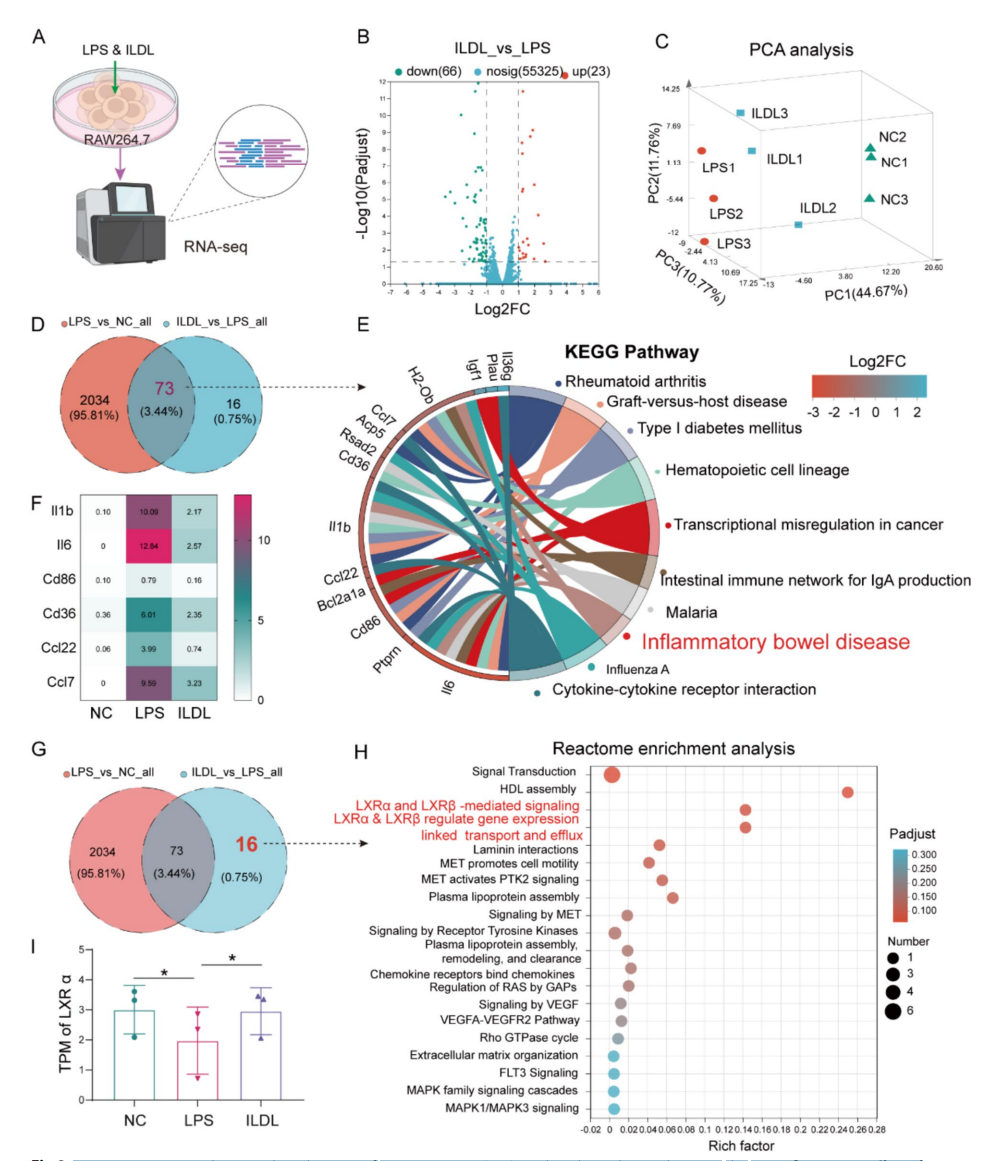
图:转录组学揭示LXRα介导的信号通路在ILDL抗炎作用中的潜在机制
LXRα在免疫调节中的作用
LXRα作为脂质代谢与免疫反应的交汇点,近年来被广泛关注。其激活不仅调节脂质稳态,还能抑制炎症因子合成,促进巨噬细胞的清除功能。ILDL通过这一通路,精准调控免疫与代谢,带来了理想的抗炎效果。
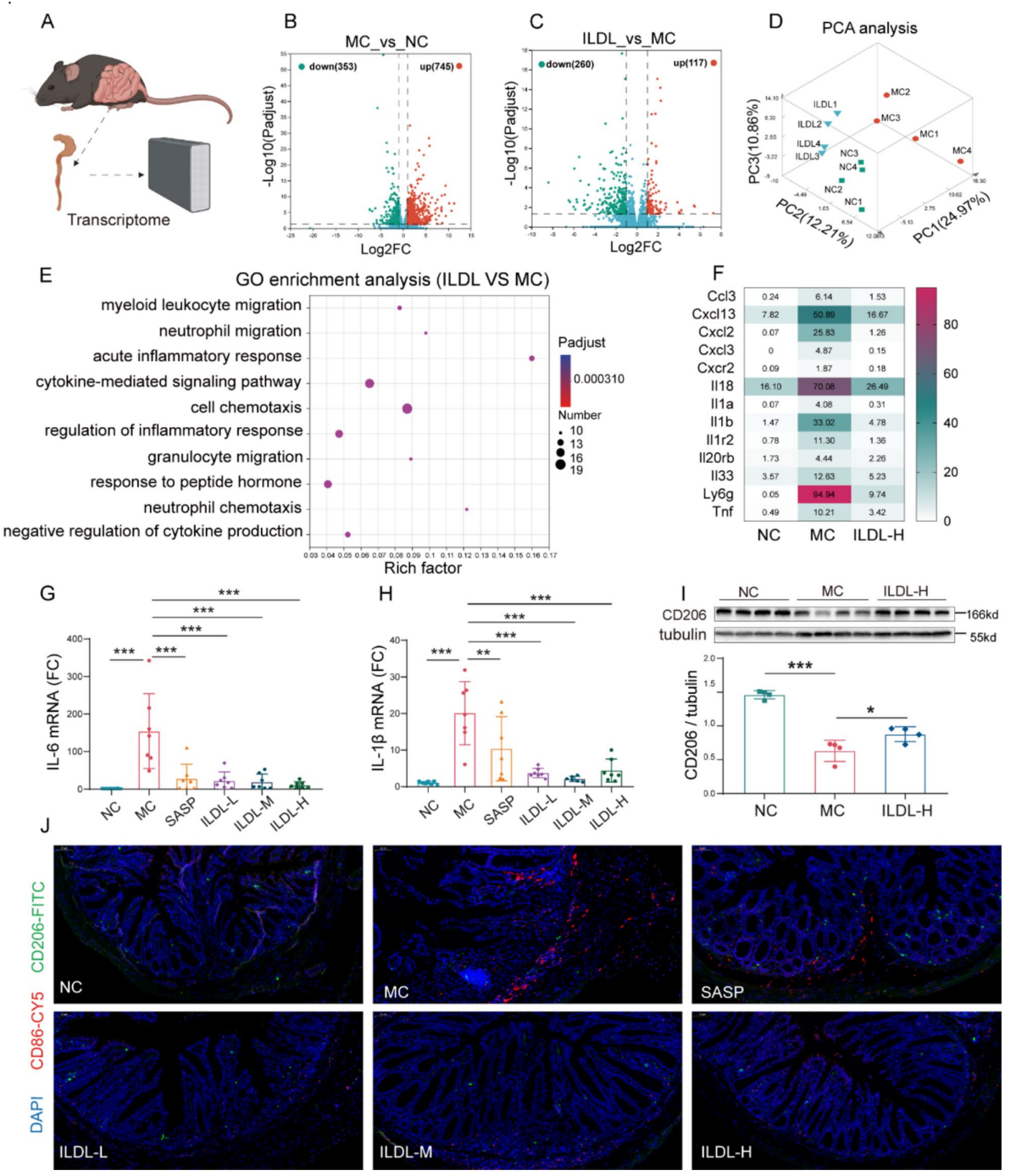
图:ILDL的抗溃疡性结肠炎作用与其抗炎活性相关
ILDL在溃疡性结肠炎模型中的疗效表现
在DSS诱导的UC小鼠模型中,ILDL显著缓解了体重下降,减少肠道炎症损伤,改善肠黏膜结构。病理学切片显示,ILDL处理组炎症细胞浸润减少,黏膜修复加快,提示其具有良好的体内抗炎和修复作用。
天然药物开发的挑战与机遇
ILDL作为天然产物,展现出独特的多靶点调控优势。相比传统单靶向小分子,天然活性成分往往安全性更高,副作用更小。该研究不仅为沉香的现代药理价值提供了科学依据,也为UC等炎症性疾病的治疗开辟新途径。 然而,天然药物开发面临诸多挑战,包括成分复杂、活性成分含量波动大、药代动力学不明等问题。未来研究需加强ILDL的药物化学优化,提高生物利用度和靶向性,推动其临床转化。
综上,本研究揭示了ILDL通过激活LXRα通路调控巨噬细胞功能,有效抑制溃疡性结肠炎的炎症反应,提供了天然药物治疗UC的新思路。未来,可结合纳米载体等先进技术,提升ILDL的递送效率和靶向精准度,推动其向临床应用迈进。 此外,探讨ILDL与现有UC药物的联合用药潜力,评估其长期安全性和疗效,将进一步丰富UC的治疗策略。
原始出处
Huang, M., Lan, M., Liu, X. et al. Isolinderalactone regulates macrophage polarization and efferocytosis by activating the LXRα pathway against ulcerative colitis. Chin Med 20, 152 (2025). https://doi.org/10.1186/s13020-025-01216-9
本文相关学术信息由梅斯医学提供,基于自主研发的人工智能学术机器人完成翻译后邀请临床医师进行再次校对。如有内容上的不准确请留言给我们。
猜你喜欢
- J Clin Oncol:挽救性放疗+恩杂鲁胺治疗根治性手术后PSA复发的高危性前列腺癌
- Crit Care:血压对院外心脏骤停患者死亡率的影响
- 七单位协同举办主题活动提高餐饮品质制止餐饮浪费
- World J Urol:中国科学家研究了前列腺钬激光剜除术对性前列腺梗阻继发的逼尿肌无力和肾功能障碍患者的疗效
- Lancet 子刊:维生素D补充对急性呼吸道感染的潜在效益和局限性
- 2019年09月12日每日养生健康简报,星期四!健康是一种生活态度!
- 贴三伏贴多久能洗澡
- 病例分享:江苏结友肺结节手术不选上海两大医院,却来杭州市一!为了明明白白的诊断,明明白白的治疗
- 私处散发什么味道才算正常?
- 女人为什么会有性渴望 9个因素让她欲望勃发
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)