首页 > 医疗资讯/ 正文
近年来,肝硬化作为多种慢性肝病的终末阶段,其复杂的发病机制和多样的临床表现,使得治疗难度较大。基于传统中药的复方制剂肉苁蓉颗粒(Rgkl)在临床上应用逾二十年,展现了显著的疗效,但其具体分子机制尚未明确。本研究通过CCl4造模肝硬化小鼠模型,结合现代组学技术与分子生物学手段,系统揭示了Rgkl在调控肝窦内皮细胞(LSEC)脂质代谢、抑制肝星状细胞(HSC)激活以及改善肝脏血流动力学中的多重作用机制。

本研究采用CCl4诱导小鼠肝硬化模型,实施肉苁蓉颗粒干预。通过影像技术评估肝脏弹性与血流速度,检测血清肝功能指标ALT、AST及透明质酸(HA)水平。肝组织病理学分析结合免疫组化染色,观察HSC激活标志物α-SMA及血管生成指标VEGF、CD34表达变化。扫描电镜用于评估LSEC滤孔结构。结合UPLC-Q-TOF-MS/MS鉴定活性成分,配合网络药理学分析,确定潜在靶点。转录组与单细胞测序揭示关键通路,利用西方印迹(WB)、免疫荧光以及分子对接技术验证机制。
实验数据显示,Rgkl显著降低了肝脏硬度和胶原沉积,同时提升了肝内血流速度,提示其对肝脏微循环有积极调节作用。血清ALT、AST与HA水平均明显下降,表明肝细胞损伤和纤维化程度减轻。免疫组化结果显示,Rgkl抑制了HSC的α-SMA表达,有效抑制星状细胞激活;血管生成相关因子VEGF及内皮标志CD34表达亦被下调,表明Rgkl具备抗病理性血管生成的能力。
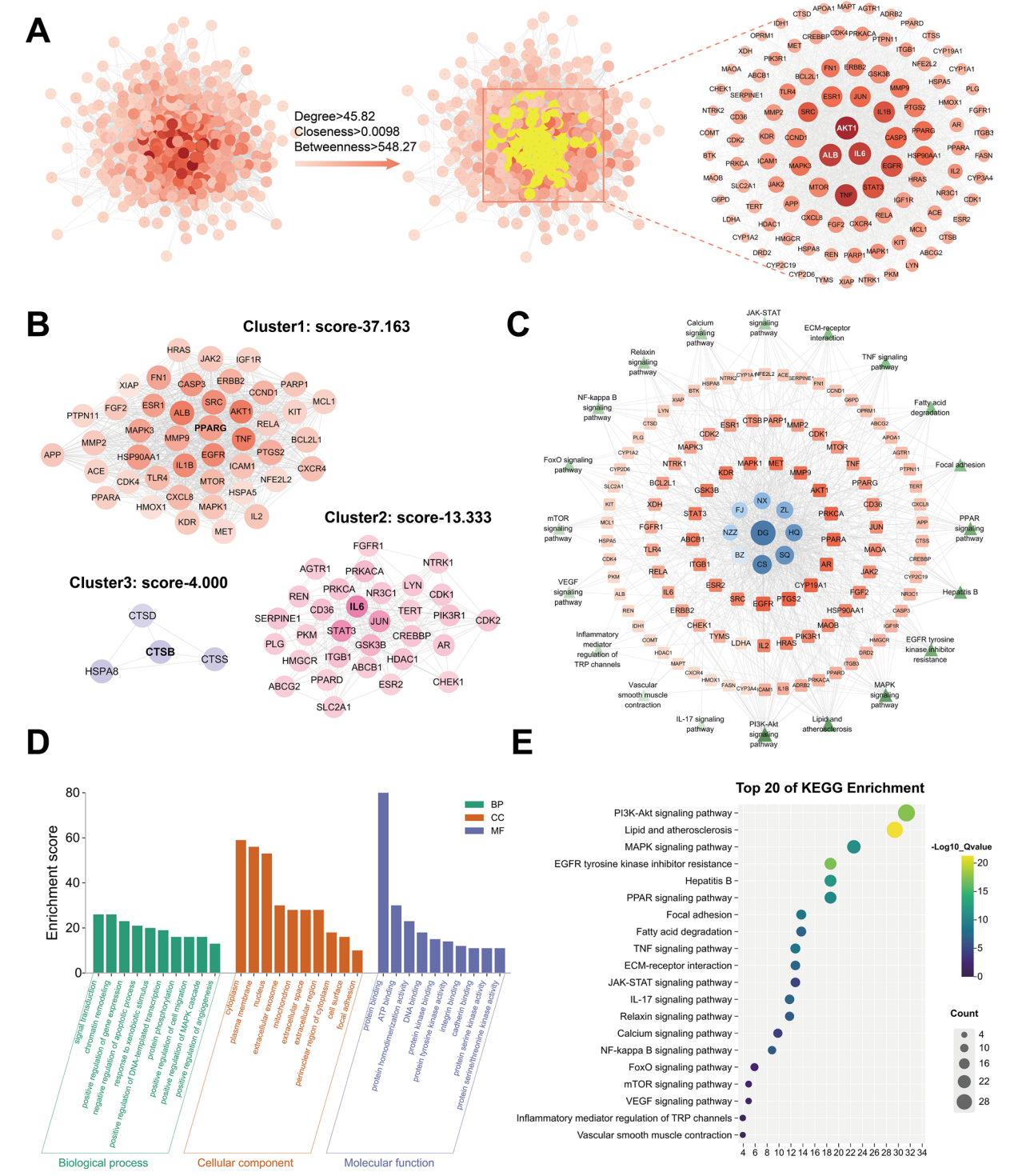
图:Rgkl治疗肝纤维化(或肝硬化)的关键作用靶点
扫描电镜分析发现,Rgkl处理组LSEC滤孔结构得以保留,伴随eNOS表达上调,提示其有助于维持肝窦内皮功能。 分子机制方面,Rgkl主要通过调节LSEC的脂质代谢途径CD36/PPAR/CPT-1,恢复内皮细胞功能;同时抑制HSC的RhoA/ROCK/YAP及PI3K/AKT/NF-κB信号通路,减少细胞收缩及炎症反应。UPLC-MS鉴定出含有帕藜内酯C、蒿甲醚A、槲皮素等18种活性成分,这些成分与肝硬化改善高度相关,发挥协同效应。
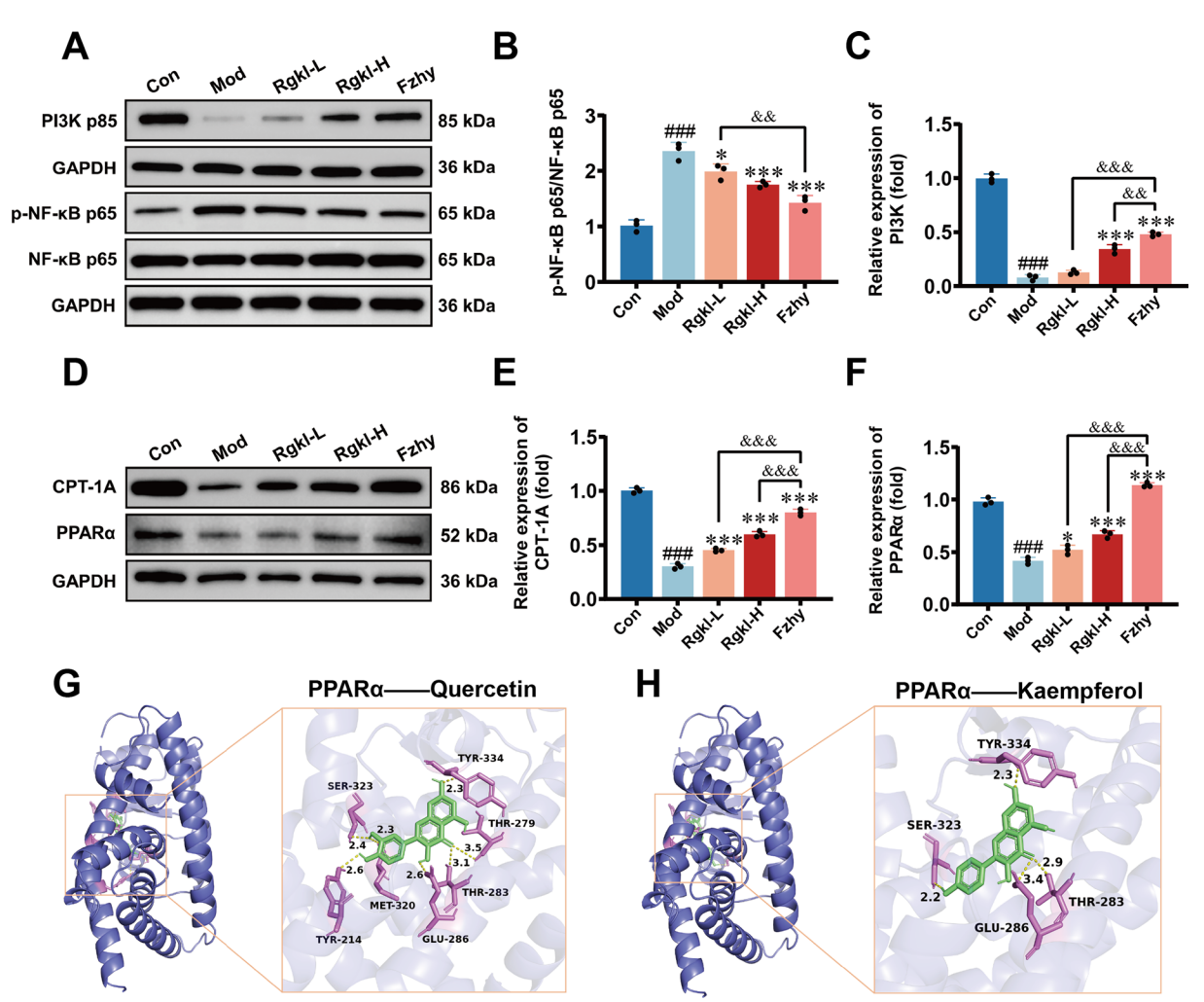
图:Rgkl调控肝星状细胞炎症活化与肝窦内皮细胞脂代谢治疗肝硬化的验证实验
综上,本研究系统阐明了肉苁蓉颗粒通过多靶点、多通路作用,显著减轻肝硬化的病理变化。特别是在调节肝窦内皮细胞脂质代谢和抑制星状细胞激活方面,揭示了其独特的分子机制,丰富了中药治疗肝纤维化的科学内涵。未来,需进一步临床验证其疗效及安全性,探索活性成分的精准靶向应用,以期推动新型肝硬化药物的开发。
原始出处
Jin, C., Ma, T., Zhang, Y. et al. Integration of network pharmacology, transcriptomics and single-cell sequencing to explore the effect of Rougan Keli in alleviating liver cirrhosis. Chin Med 20, 153 (2025). https://doi.org/10.1186/s13020-025-01220-z
本文相关学术信息由梅斯医学提供,基于自主研发的人工智能学术机器人完成翻译后邀请临床医师进行再次校对。如有内容上的不准确请留言给我们。
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)