首页 > 医疗资讯/ 正文
编者按:肺癌作为全球癌症相关死亡的首要原因,其治疗一直是医学界的重点和难点。近年来,随着医学技术的不断进步,肺癌的治疗手段也在不断更新和完善。然而,EGFR-TKI耐药问题以及部分患者对传统PD-1/PD-L1抑制剂治疗效果不佳的情况,仍是临床亟待解决的难题。在此背景下,全球首个PD-1/VEGF双特异性抗体依沃西单抗的出现,无疑为肺癌治疗带来了新的曙光。曲靖市第二人民医院罗详冲医生在本文中全面总结依沃西单抗在肺癌中的应用,以期为临床提供参考与指导。
肺癌是全球癌症相关死亡的首位原因,其中非小细胞肺癌(NSCLC)占比达85%,大部分确诊时即为晚期。尽管以表皮生长因子受体酪氨酸激酶抑制剂(EFGR-TKI)为代表的靶向治疗和以程序性死亡受体-1/配体-L1(PD-1/PD-L1)抑制剂为首的免疫治疗革新了肺癌格局,显著延长了肺癌患者的总生存期(OS)和提高了生活质量。但EGFR-TKI耐药是目前临床面临的困境,耐药进展后的药物选择性差,疗效有效,亟需改变EGFR-TKI耐药后线选择的格局,与此同时,部分PD-L1低表达的患者一线选择传统PD-1/PD-L1抑制剂的治疗效果也不佳。
全球首个PD-1/VEGF双特异性抗体依沃西单抗(Ivonescimab/AK112)能通过同时靶向PD-1和VEGF-A,实现解除免疫抑制和血管正常化的双重调控,成为首个在Ⅲ期临床研究中头对头击败帕博利珠单抗的药物。目前,依沃西单抗已经正式获批用于联合培美曲塞和卡铂治疗经EGFR-TKI治疗后进展的EGFR突变阳性局部晚期或转移性非鳞状非小细胞肺癌患者和用于PD-L1肿瘤比例分数(TPS)≥1%的EGFR/ALK突变阴性的局部晚期或转移性非小细胞肺癌一线单药治疗。基于依沃西单抗的惊艳结果,重塑了肺癌治疗新格局,全面开启肺癌治疗的新时代。
依沃西单抗的结构及作用机制
依沃西单抗是一种人源化IgG1-ScFv结构,采用Tetrabody技术通过基因工程将抗PD-1单链抗体(ScFv)与抗VEGF-A的Fab片段融合形成稳定的Y型四聚体(四价)(图1),其Fab端负责结合VEGF-A,抑制肿瘤血管生成,Fc端通过单链抗体片段(ScFv)结合PD-1,解除免疫抑制,同时行Fc段工程化改造,引入L234A/L235A两个氨基酸突变,消除FcγR结合能力,消除了抗体依赖性细胞介导的细胞毒性(ADCC)、补体依赖性细胞毒性(CDC)、抗体依赖性细胞吞噬作用(ADCP)、抗体依赖性细胞因子释放(ADCR)和细胞因子释放综合征(CRS),降低了免疫原性及毒副作用的发生。
研究表明[1],依沃西单抗对PD-1的半抑制浓度(IC50)为0.8nM,对VEGF的IC50为0.5nM。依沃西单抗的作用机制是通过同时靶向PD-1和VEGF-A两条关键通路实现的,可结合T细胞表面的PD-1受体,阻断其与肿瘤细胞PD-L1/L2的相互作用,解除肿瘤对T细胞的免疫抑制,恢复T细胞对肿瘤的杀伤能力,同时结合肿瘤微环境中的VEGF-A,抑制其与血管内皮细胞受体(VEGFR)结合,阻断异常血管生成,减少肿瘤营养供应并改善肿瘤免疫微环境,VEGF-A的存在使依沃西单抗对PD-1的结合力提升>18倍,而PD-1的存在使依沃西单抗对VEGF-A的结合力提升>4倍,形成双通路相互强化的阻断效果(图1)[1]。
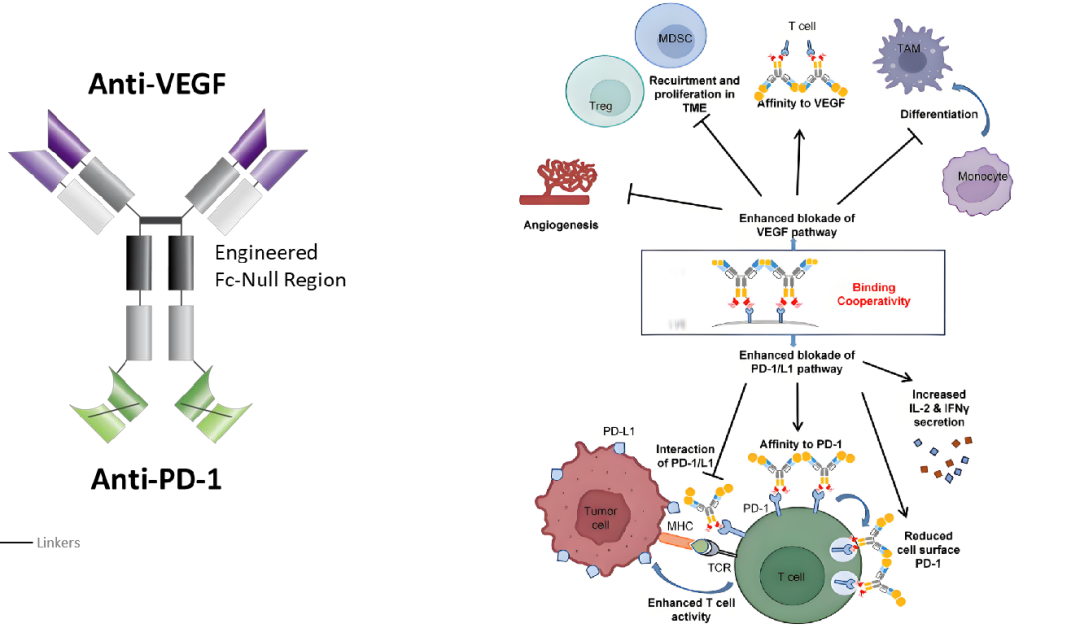
图1 依沃西单抗结构及作用机制
依沃西单抗在EGFR-TKI耐药后中的应用
近年来,随着肺癌精准治疗的迅猛发展,EGFR-TKI已成为EGFR突变阳性NSCLC患者的治疗新标准,但EGFR-TKI的耐药情况是难以避免的临床和科学难点。EGFR-TKI耐药机制呈现多样化,如何根据不同的耐药机制选择个体化的治疗方案和策略是临床研究热点。
EGFR-TKI耐药后的治疗需以分子机制为导向精准分层:对于依赖型耐药如C797S突变患者可根据突变模式选择三代联合一代EGFR-TKI(C797S反式突变)或布加替尼联合西妥昔单抗(C797S顺式突变);对于非依赖型耐药,MET扩增患者可联用三代EGFR-TKI与MET抑制剂如赛沃替尼,而HER2/BRAF突变患者也可尝试双靶向治疗,获益人群需再次行基因检测明确突变类型且能耐受联合治疗带来的不良反应。但目前的真实临床实践中,药物的可及性、经济性或者EGFR耐药的复杂化使整体的治疗策略选择有限,整体的后线治疗效果仍不理想。
HARMONi-A是一项双盲Ⅲ期随机对照研究,首次评估了依沃西单抗联合化疗对比化疗在EGFR-TKI治疗后进展的EGFR突变转移性NSCLC患者的疗效和安全性[2]。依沃西单抗联合化疗组对比化疗组取得了PFS的优势分别为7.1个月和4.8个月,HR值为0.46(图2),疾病进展或死亡风险显著降低了54%。亚组分析中,对于存在脑转移的患者疾病进展或死亡风险降低了60%;对于既往接受过1种EGFR-TKI治疗后进展的患者疾病进展或死亡风险降低了53%;对于既往接受过≥2种EGFR-TKI治疗后进展的患者疾病进展或死亡风险降低了54%;对于19外显子缺失突变的患者疾病进展或死亡风险降低了52%;对于T790M突变阳性的患者降低78%的疾病进展或死亡风险,获益更显著。
与同类研究如ORIENT-31相比,PFS提升幅度更为显著,提示双抗双靶点协同作用可能优于传统单靶点联合策略,联合组与化疗组的ORR分别为50.6%和35.4%,ORR的改善也较为显著,OS有获益的趋势。安全性方面主要为化疗相关的不良反应,免疫相关不良事件和血管内皮生长因子受体相关事件发生率较低,且未出现新的安全性信号,与PD-1/PD-L1抑制剂联合抗VEGF单抗如阿替利珠单抗+贝伐珠单抗相比,依沃西单抗的免疫相关毒性显著减少,可能得益于其结构的优化设计。基于HARMONi-A研究,依沃西单抗为EGFR-TKI耐药NSCLC的后线治疗提供了新的选择,成功改写了指南,正式获批用于联合培美曲塞和卡铂治疗经EGFR-TKI治疗后进展的EGFR突变阳性局部晚期或转移性非鳞状非小细胞肺癌患者。
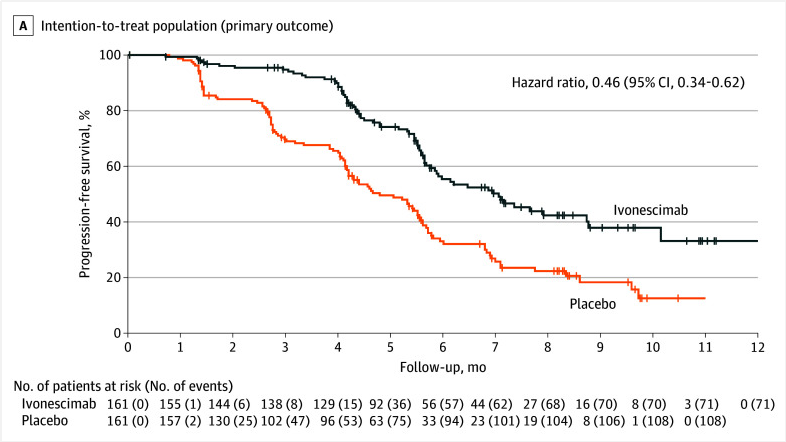
图2 HARMONi-A研究联合组与对照组的PFS和HR值
依沃西单抗在EFGR突变阴性肺癌中的应用
免疫治疗是目前肺癌的研究热点之一,PD-1/PD-L1抑制剂单药或联合化疗已成为EGFR突变阴性晚期NSCLC的一线治疗标准,尽管免疫治疗已取得了令人鼓舞的疗效,但单药治疗提供的临床获益有限且当前的疗效距离实现患者治愈的目标仍存在巨大差距。
HARMONi-2研究是一项随机、双盲、III期临床试验,旨在评估依沃西单抗与帕博利珠单抗一线治疗PD-L1阳性晚期NSCLC患者的疗效和安全性[3]。
结果显示,依沃西单抗组和帕博利珠单抗组的中位PFS分别为11.14和5.82个月(HR=0.51),依沃西单抗较帕博利珠单抗降低了49%疾病进展或死亡风险。依沃西单抗和帕博利珠单抗客观缓解率(ORR)分别为50.0%和38.5%,疾病控制率(DCR)分别为89.9%和70.5%,得到了明显改善。亚组分析中,在PD-L1表达水平为1%-49%的人群中,依沃西单抗相比帕博利珠单抗的PFSHR为0.54;在PD-L1表达水平≥50%人群中,依沃西单抗相比帕博利珠单抗的PFS HR为0.46;在鳞状非小细胞肺癌人群中,依沃西单抗相比帕博利珠单抗的PFS HR为0.48;在非鳞状非小细胞肺癌人群中,依沃西单抗相比帕博利珠单抗的PFS HR为0.54,均提示依沃西单抗疗效优于帕博利珠单抗。
基于上述研究结果,依沃西单抗获批用于PD-L1肿瘤比例分数(TPS)≥1%的EGFR/ALK突变阴性的局部晚期或转移性非小细胞肺癌一线单药治疗,为PD-L1阳性晚期NSCLC患者提供了一种全新的治疗选择。
依沃西单抗在晚期肺鳞癌中的应用
目前免疫治疗的出现使晚期肺鳞癌的治疗进入一个崭新的时代,已经彻底改写了晚期肺鳞癌的临床实践指南。既往抗血管生成药物贝伐珠单抗因出血风险无法用于肺鳞癌,极大地限制了晚期肺鳞癌的药物选择及治疗效果。
HARMONi-6研究(AK112-306)是一项Ⅲ期头对头临床试验,旨在评估依沃西单抗联合化疗对比替雷利珠单抗联合化疗一线治疗晚期鳞状非小细胞肺癌的疗效与安全性。共入组532例晚期肺鳞癌患者,其中中央型鳞癌占比约63%。中期研究结果显示,在意向治疗人群(ITT)中,依沃西联合化疗组较替雷利珠单抗联合化疗的患者PFS取得阳性结果,同时在PD-L1阳性和阴性人群中,依沃西联合化疗均显示出明显的PFS获益,在安全性方面,依沃西组总体表现良好,未发现新的安全性信号,与治疗相关的严重不良反应发生率以及三级及以上出血事件发生率与对照组相似,期待最终的研究结果。
HARMONi-6研究填补了抗血管生成药物在晚期肺鳞癌中的临床空白,突破了贝伐珠单抗无法应用于肺鳞癌的瓶颈,为晚期鳞癌患者带来了全新更优选择。
依沃西单抗在脑转移患者中的应用
NSCLC脑转移发生率高、预后差、总的生存时间缩短。由于血脑屏障等的限制,目前仅小分子靶向药物如阿美替尼、奥希替尼、伏美替尼以及阿来替尼等对EGFR/ALK突变阳性的NSCLC脑转移患者显示良好的疗效,但对于分子靶向药物耐药以及驱动基因突变阴性的脑转移患者来说,大分子的PD-1/PD-L1抑制剂和化疗药物则很难透过血脑屏障而发挥治疗作用,因此,NSCLC脑转移患者的药物探索任重道远。
HARMONi-A研究中针对EGFR-TKI耐药的脑转移患者依沃西联合化疗组颅内的中位PFS达8.4个月,较单纯化疗组的5.4个月显著延长,疾病进展风险降低了60%(图3)[2];HARMONi-2研究中,PD-L1阳性的脑转移患者接受依沃西单抗单药治疗较帕博利珠单抗显著降低了45%疾病进展风险[3]。早期的AK112-201/202临床试验显示,35例脑转移患者接受依沃西单抗单药或联合化疗后,颅内完全缓解率为23%,整体中位颅内PFS高达19.3个月,且安全性良好,未观察到接受依沃西单抗治疗的脑转移患者发生颅内出血事件。
基于以上研究结果,提示依沃西单抗对NSCLC脑转移的患者颅内肿瘤的控制效果显著,有望成为NSCLC脑转移患者的全新治疗选择。
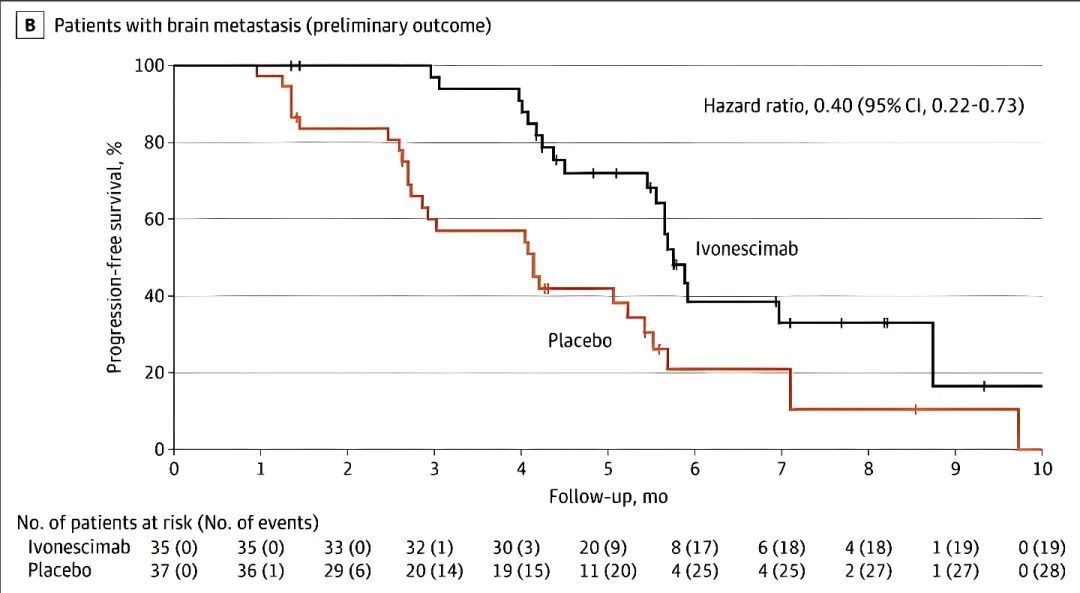
图3 依沃西单抗治疗脑转移患者的PFS和HR
依沃西单抗在肺癌围手术期中的应用
近年来免疫治疗在肺癌领域中不断从晚期到中期和早期前移,早期肺癌的围手术期治疗已经全面步入免疫时代。KEYNOTE-671、CheckMate-77T、AEGEAN、CheckMate-77T、RATIONALE-315、Neotorch等研究相继取得阳性结果,三种新辅助、辅助、以及新辅助+辅助的围手术期治疗模式已被证实可以显著降低可切除NSCLC术后复发风险,成为Ⅱ~Ⅲ期NSCLC围手术期治疗新标准,但目前围术期免疫治疗领域仍存在诸多未被解决的问题,如整体的病理完全缓解(pCR)率和主要病理缓解(MPR)率还需提高、如何选择不同围术期免疫治疗模式、围术期免疫治疗最佳获益人群的筛选等。
AK112-205研究是一项单中心、开放标签的Ⅱ期临床研究,旨在评估依沃西单抗单药或联合化疗新辅助/辅助治疗NSCLC的安全性和有效性[4],结果显示,依沃西联合化疗治疗组的pCR和MPR率分别是43.6%和71.8%,其中对于鳞癌患者,pCR率高达63.6%,MPR率高达84.1%;依沃西单药治疗组的pCR和MPR率分别为30.0%和60.0%(图4),安全性方面,尚未出现意外出血情况,未发生导致手术延迟或取消的治疗相关不良事件,整体安全性可控。因此,无论是依沃西单抗单药还是依沃西单抗联合化疗,均能使患者在pCR和MPR率上获得显著的结果,相较于传统的单靶点PD-1/PD-L1抑制剂的pCR和MPR率,依沃西单抗再创新高,充分证实了依沃西单抗在围术期肺癌治疗中的显著效果,为可切除NSCLC患者提供了更强有力的保证。
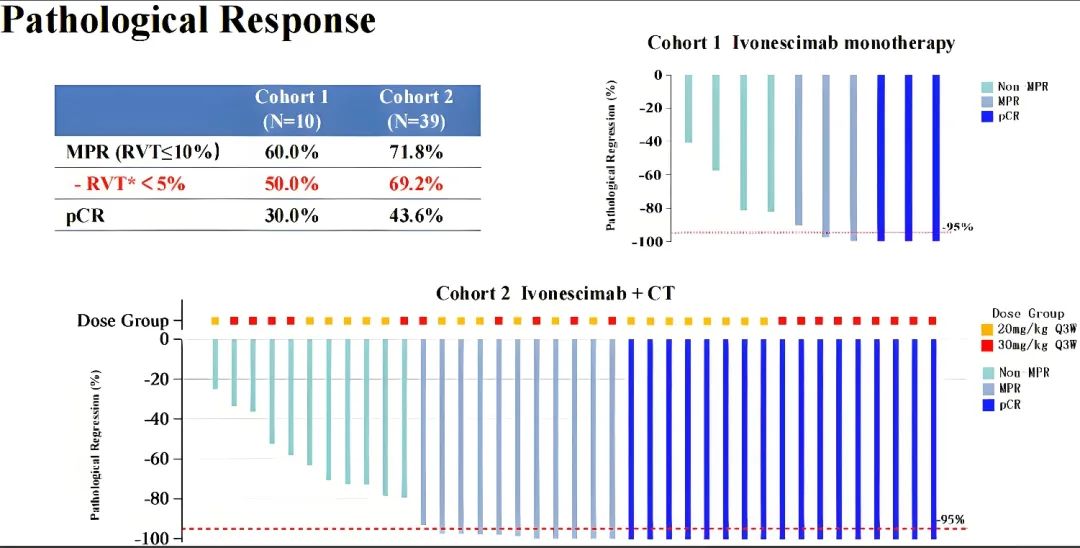
图5 AK112-205研究中实验组和对照组的pCR和MPR率
依沃西单抗在小细胞肺癌中的应用
小细胞肺癌(SCLC)是一种恶性程度高、侵袭性强和预后差的恶性肿瘤。既往传统的化疗方案虽能在一定程度上缓解病情,但药物耐药性快使得长期生存率差。近年来,免疫治疗改变了SCLC的治疗格局,免疫治疗联合化疗已成为广泛期小细胞肺癌一线治疗的标准方案。然而,由于免疫治疗联合化疗如阿替利珠单抗或度伐利尤单抗联合依托泊苷和铂类的生存获益仍然有限,如何进一步提高疗效是亟待解决的问题。
NCT05116007研究是一项开放标签、多中心的Ib期临床试验包括剂量递增和剂量扩展阶段,旨在评估依沃西单抗联合依托泊苷和卡铂一线治疗ES-SCLC患者的疗效和安全性[5]。结果显示,所有患者中的联合治疗组的ORR和DCR分别为80%和91.4%,在依沃西单抗3mg/kg、10mg/kg和20mg/kg剂量组中,患者的ORR分别为66.7%、90.9%和76.2%。在3mg/kg剂量组中,中位PFS和中位OS尚未达到,10mg/kg和20mg/kg剂量组的中位PFS分别为7.0个月和6.9个月,中位OS分别为17.1个月和14.5个月。安全性方面,最常见的不良反应为中性粒细胞计数减少、白细胞计数减少和贫血。该研究表明,依沃西单抗联合依托泊苷和铂类作为ES-SCLC的一线治疗具有良好的抗肿瘤活性,有望为ES-SCLC患者的治疗新选择。
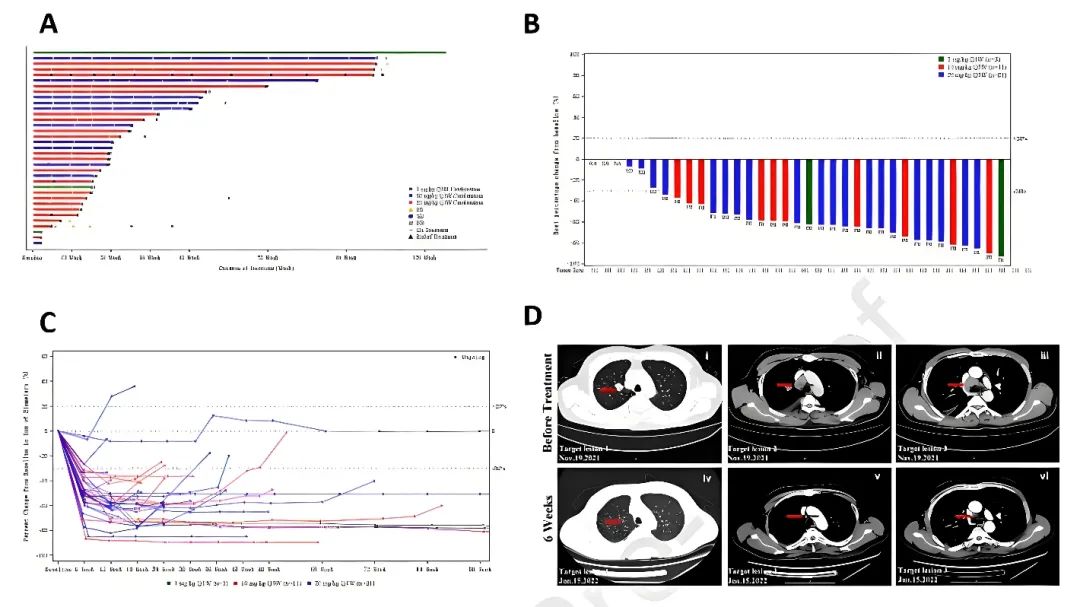
图6 依沃西单抗在广泛期小细胞肺癌中的疗效
总结
综上所述,依沃西单抗在EGFR耐药后、驱动基因阴性PD-L1阳性、无论是肺腺癌还是肺鳞癌、肺癌伴脑转移、围手术期以及小细胞肺癌中都显示出良好的疗效[6-10],实现了肺癌的全面布局,推动了肺癌免疫治疗从传统单靶点PD-1/PD-L1抑制剂迈向全新的PD-1/VEGF的双靶点双抗治疗新时代,全面开启了肺癌治疗的新篇章,但目前仍需不断进行深入研究如克服或延缓耐药情况,优化生物标志物筛选,探索更优的联合疗法,横向及纵向前瞻性对比探索以及如何降低药物毒性等,相信随着不断地探索,依沃西单抗讲成为更多肺癌患者的又一利器,也将成为特异性双抗药物的开荒者。
参考文献:
[1] Dhillon S. Ivonescimab: First Approval[J]. Drugs. 2024, 84(9):1135-1142.doi: 10.1007/s40265-024-02073-w. Epub 2024 Jul 29. PMID: 39073550.
[2] Fang W, Zhao Y, Luo Y, et al.Ivonescimab Plus Chemotherapy in Non-Small Cell Lung Cancer With EGFR Variant: A Randomized Clinical Trial[J], JAMA. 2024, 332(7): 561-570. doi: 10.1001/jama.2024.10613.PMID: 3882054.
[3] Xiong A, Wang L, Chen J, et al. Ivonescimab versus pembrolizumab for PD-L1-positive non-small cell lung cancer (HARMONi-2): a randomised, double-blind, phase 3 study in China[J]. Lancet, 2025, 405(10481): 839-849. doi: 10.1016/S0140-6736(24)02722-3. PMID: 40057343.
[4] Frentzas S, Austria Mislang AR, Lemech C, et al. Phase 1a dose escalation study of ivonescimab (AK112/SMT112), an anti-PD-1/VEGF-A bispecific antibody, in patients with advanced solid tumors[J]. J Immunother Cancer. 2024,12(4):e008037. doi: 10.1136/jitc-2023-008037. PMID: 38642937; PMCID: PMC11033648.
[5] Chen Z, Wu L, Wang Q, et al. Brief Report: Ivonescimab Combined With Etoposide Plus Carboplatin as First-Line Treatment for Extensive-Stage SCLC: Results of a Phase 1b Clinical Trial[J]. J Thorac Oncol. 2025, 20(2):233-239. doi: 10.1016/j.jtho.2024.10.013. Epub 2024 Oct 28. PMID: 39490738.
[6] Wang F, Wei X, Zheng Y, et al. Safety, Pharmacokinetics, and Pharmacodynamics Evaluation of Ivonescimab, a Novel Bispecific Antibody Targeting PD-1 and VEGF, in Chinese Patients With Advanced Solid Tumors[J]. Cancer Med. 2025,14(6):e70653. doi: 10.1002/cam4.70653. PMID: 40114411; PMCID: PMC11925807.
[7] Zhang Y, Liu X, Ren S. Ivonescimab in non-small cell lung cancer: harmonizing immunotherapy and anti-angiogenesis[J]. Expert Opin Biol Ther. 2025, 25(5):1-7. doi: 10.1080/14712598.2025.2487512. Epub 2025 Apr 2. PMID: 40162997.
[8] Al Matairi A, Hammadeh BM, Aldalati AY, et al. Efficacy and Safety of Ivonescimab in the Treatment of Advanced Non-small Cell Lung Cancer (NSCLC): A Systematic Review[J]. Cureus. 2025,17(1):e77381. doi: 10.7759/cureus.77381. PMID: 39944427; PMCID: PMC11818946.
[9] Sankar K. Ivonescimab in advanced NSCLC: is progression-free survival enough, or are overall survival data also needed[J], Lancet. 2025,405(10481):757-759. doi: 10.1016/S0140-6736(25)00369-1. PMID: 40057331.
[10] Long R, Kuang W, Zhou Q. Ivonescimab plus chemotherapy in advanced or metastatic non‑squamous non‑small cell lung cancer with EGFR variant in China: a cost-effectiveness analysis[J]. Transl Lung Cancer Res. 2025,14(5):1622-1634. doi: 10.21037/tlcr-2024-1053. Epub 2025 May 22. PMID: 40535084; PMCID: PMC12170261.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)