首页 > 医疗资讯/ 正文
产时母体发热会直接影响胎心率,并与母婴不良结局相关。硬膜外相关母体发热(ERMF)是产时发热的诱因之一,约20%接受硬膜外分娩镇痛的孕妇会出现此症状。接受硬膜外布比卡因麻醉的孕妇血浆中IL-1Ra/IL-1b比值下降,表明IL-1Ra或IL-1b可能在ERMF中发挥作用。白细胞介素-1(IL-1)其促炎效应通过IL-1与IL-1Ra的结合受到严格调控,遗传变异位点rs6743376和rs1542176的变异是目前已知对循环IL-1Ra蛋白浓度影响最强的遗传决定因素。通过对英国Biobank数据库的产时数据采用孟德尔随机化方法,该研究团队发现基因预测的较高IL-1Ra水平与硬膜外镇痛术后剖宫产风险增加相关,并提出假说:在接受硬膜外分娩镇痛的产妇中,具有基因预测较高IL-1Ra水平的女性发生产时发热的频率会更低。研究的结果发表在2025年7月的British Journal of Anaesthesia期刊上。

方法
研究设计
EPIFEVER-2研究是一项采用孟德尔随机化方法的前瞻性观察性队列研究,于2021年1月25日获得伦敦(布鲁姆斯伯里)研究伦理委员会(20/LO/1213)的伦理批准后,在英国六个中心开展。该研究在获得伦理批准后进行了前瞻性注册(ISRCTN99641204)。此前已发表过详细说明数据收集、设计和分析方案的协议论文。所有参与者均签署了书面知情同意书。本研究遵循STROBE-MR指南要求,以加强采用孟德尔随机化方法的流行病学观察性研究报告质量。
纳入标准
这项前瞻性研究采用严格的纳入与排除标准进行设计,旨在最大限度降低潜在混杂因素对解读产妇产时发热、临床结局与等位基因评分之间关系的干扰风险。纳入标准:≥18岁女性;单胎或双胎妊娠;分娩镇痛使用硬膜外导管。排除标准:不愿意或没有能力签署同意书;无法理解书面或口头英语;已知免疫或遗传综合征或突变(以免疫缺陷为特征);硬膜外置管前经微生物学证实的感染(包括新冠病毒快速抗原检测阳性);已确认的产时发热(母体体温≥38℃);宫内死亡;或无论是否经微生物学证实感染而开具或使用抗生素的情况。
临床数据收集
记录硬膜外置管时间与分娩时间,同时按照接受硬膜外镇痛产妇的常规护理指南进行体温监测(图1)。分娩方式、产前抗生素使用情况及产妇住院时长均从电子健康档案中提取。
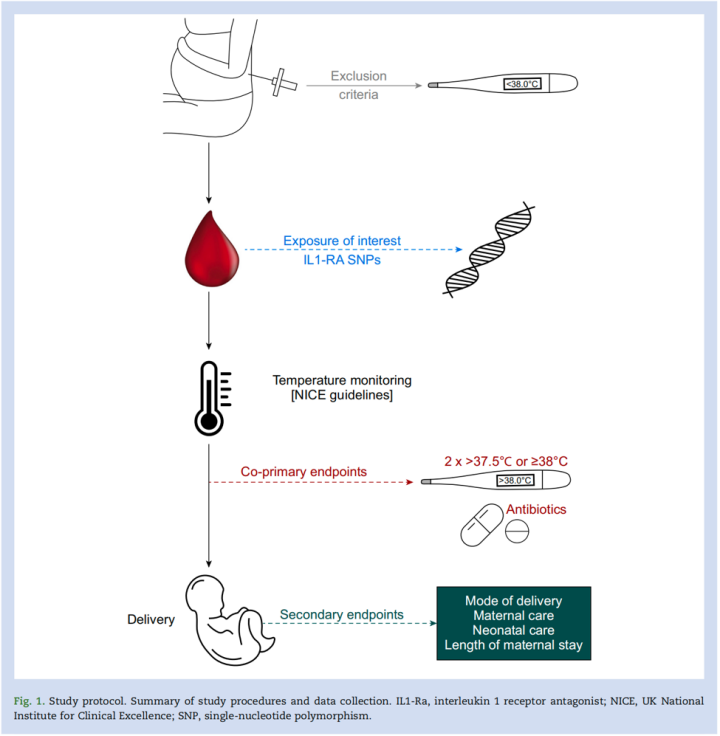
单核苷酸多态性基因分型
在硬膜外导管置入后4小时内采集血液样本至PAXgene Blood DNA管(Qiagen公司,英国曼彻斯特),这是保存基因组DNA的最佳方法。Paxgene管在分析前储存于零下80℃环境。QMUL基因组中心进行了靶向DNA分析。研究结束后由对研究细节不知情的人员进行批量分析。由于本项目涉及少量单核苷酸多态性(SNPs)和大规模人群,所以采用Taqman SNP基因分型技术检测IL-1Ra基因的rs6743376和rs1542176等位基因存在与否以建立遗传评分。研究还探讨了NLRP3炎症小体的多态性是否与ERMF相关,鉴于NLRP3是IL-1家族细胞因子产生的关键介质。研究对NLRP3内含子变异体rs10754555进行了基因分型,该变异体通过激活炎症小体和IL-1β产生,与临床相关的全身炎症增加存在关联。
白细胞介素-1受体拮抗剂等位基因评分的构建
研究未直接测量循环IL-1Ra水平,而是采用了国际白细胞介素1遗传学联盟描述的方法——该联盟通过孟德尔随机化分析研究了IL-1Ra基因上调对心脏代谢的影响。该遗传评分完全符合此方法的要求标准,主要因为这两个SNPs互不相关,且对基因预测的IL-1Ra浓度具有统计学上独立的影响效应。此外,这两个SNPs对IL-1Ra浓度的影响幅度相似,遗传评分与IL-1Ra浓度呈线性关联。每遗传一个IL1RN C等位基因,基因预测的IL-1Ra浓度就会增加0.22个标准差。这意味着通过构建遗传评分将两个SNPs联合分析,既能增强研究效力又具有生物学相关性。作为探索性分析,丐研究还检测了NLRP3内含子变异体rs10754555与主要结局的关联性。
关注暴露因素
研究关注的暴露因素是基因预测的IL-1Ra水平,对0(最低基因IL-1Ra水平)与≥1等位基因评分进行对比。
主要终点
复合主要终点指标为产妇产时发热,产时发热定义为母体体温>38℃或分娩期间开始硬膜外镇痛后(依据英国皇家妇产科学院指南建议:当产妇体温>38℃或两次间隔至少1小时的测量结果>37.5℃时需进行抗菌治疗)使用抗生素的处方情况。因此,在未使用抗生素的情况下,若产妇体温超过38℃,即达到主要观察终点。
次要终点
次要终点指标包括共同主要结局的各个组成部分、分娩方式,以及对母亲(产程时长、住院时间和重症监护使用情况)和婴儿(出生5分钟时的Apgar评分及新生儿重症监护使用情况)所需的临床护理。
统计分析
针对预先设定的主要临床终点,研究比较了等位基因评分为0和1时主要复合终点的相对发生率。对于主要和次要终点,研究采用卡方检验来验证等位基因评分之间(及跨评分)是否存在独立性。在分娩方式分析中,研究探讨了产妇产时发热/抗生素使用情况与等位基因评分对剖宫产率和阴道分娩率的交互影响。事后检验采用Fisher精确检验,因统计模拟研究表明该方法可作为卡方检验有价值的补充分析技术。所有分析均基于意向治疗原则,使用NCSS 2023统计软件完成。各组终点的汇总统计量均呈现估计治疗效果及相应95%置信区间(双侧P值)。对于事件发生率较低的次要结局(<20例),未进行统计分析。连续变量数据采用单因素方差分析,辅以Tukey-Kramer事后检验分析组间交互作用。显著性差异设定为P<0.05。
样本量估算
根据IL-1Ra联盟评分及对英国生物样本库的分析,等位基因评分为0的女性约占人口12%。首期EPIFEVER研究中产妇产时发热总体发生率为13.4%,考虑到英国产科护理指南当前采用更低的体温阈值(37.5℃)作为产时早期抗生素使用标准,该研究评估该数据可能非常保守。在英国生物样本库研究分析前,研究推测等位基因评分为0的产妇发生产时发热的概率更高(约22%)。因此估算至少需要637名受试者才能检测出约13%的共同主要终点绝对差异,前提设定为:等位基因评分≥1的产妇产时发热发生率为9%(α=0.05;1-β=0.2)、分配比例7.5:1,并考虑分娩入组后1%的脱落率(双侧检验)。据此估算,75名等位基因评分为0的产妇将与558名评分≥1的产妇进行对照。
结果
研究受试者
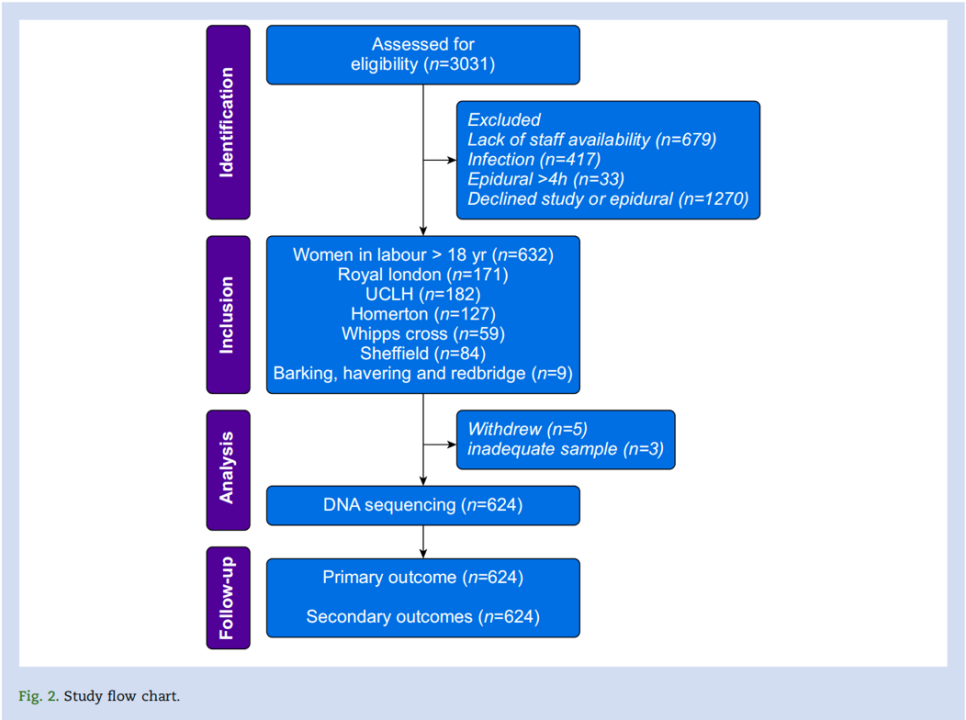
研究受试者招募工作于2021年4月27日开始,2023年4月25日在英国六个中心完成。期间研究筛查了2399名女性,最终有632人参与研究(图2)。624名产妇中有66人(10.6%)出现产时发热,其中52人(78.8%)进行了血培养检测,有5人报告存在微生物生长。
白细胞介素-1受体拮抗剂(IL-1Ra)等位基因评分分布
在EPIFEVER-2研究人群中,等位基因评分为0的女性占11.8%(n=74)。不同等位基因评分组在种族或其他特征方面均无显著差异。
主要复合终点:产妇产时发热或分娩前抗生素给药
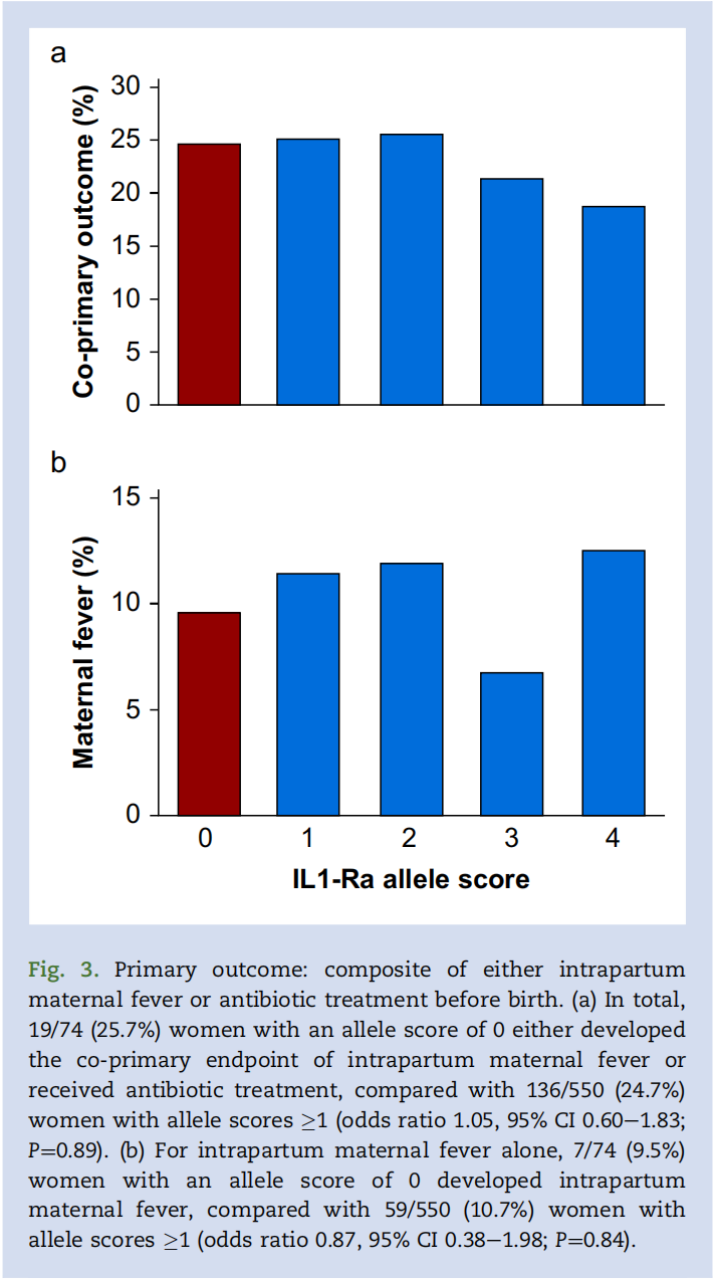
在等位基因评分为0的产妇中,19/74例(25.7%)出现产时发热或接受抗生素治疗(或两者兼有),而等位基因评分≥1的产妇中这一比例为136/550例(24.7%)(比值比1.05,95%置信区间0.60-1.83;P=0.89)(图3a)。
产妇产时发热的情况
在等位基因评分为0的74名产妇中,有7人(9.5%)出现发热症状;相比之下,550名等位基因评分≥1的产妇中有59人(10.7%)出现发热(比值比0.87,95%置信区间0.38-1.98;P=0.84)(图3b)。
抗生素治疗
在等位基因评分为0的20/74名(27.0%)产妇中,硬膜外镇痛后开始产时抗生素治疗;而等位基因评分≥1的133/550名(24.2%)产妇接受该治疗(比值比0.87,95%置信区间0.38-1.98;P=0.59)。
产程时限
等位基因评分为0的产妇组,硬膜外导管置入后的平均产程时长为644分钟(95%置信区间565-724分钟);等位基因评分为1-4的产妇组为601分钟(95%置信区间578-631分钟)(P=0.31,单因素方差分析)。
分娩方式
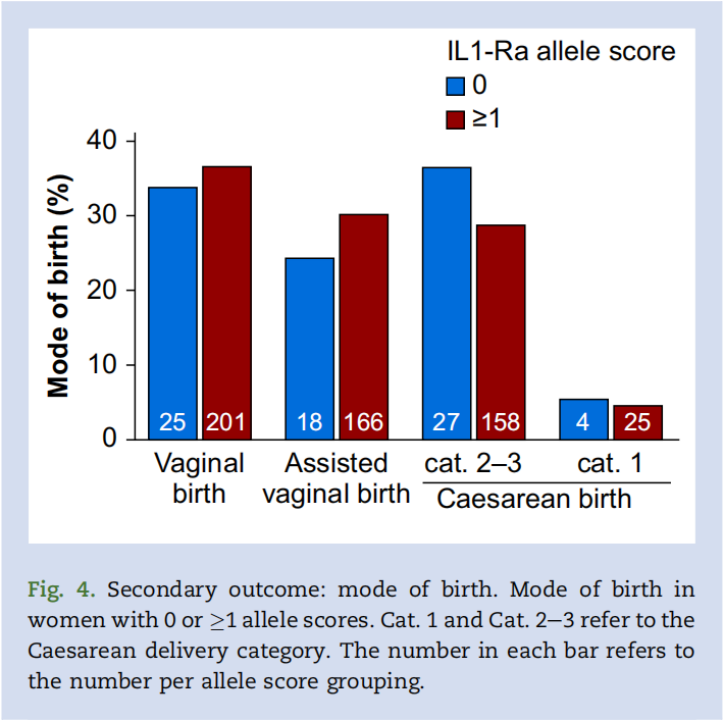
在等位基因评分为0的74名孕妇中,31人(41.9%)选择了剖宫产分娩;而在等位基因评分为1-4的550名孕妇中,183人(33.3%)选择了该分娩方式(卡方值=2.15;P=0.143)(见图4)。
新生儿与产妇结局
新生儿与产妇结局(包括产妇住院时长)在等位基因评分为0与≥1分的产妇间未呈现差异。探索性分析显示,NLRP3基因内含子变异体rs10754555与主要结局无显著关联(卡方值=2.66;P=0.265)。
讨论
EPIFEVER-2研究建立了规模最大的前瞻性数据集,详细记录了产时发热的发生率及其后果,该研究采用严格定义的入组标准并排除了潜在混杂因素。该研究的主要发现是:在接受椎管内分娩镇痛的产妇中,发热风险与IL-1Ra基因决定水平无关。数据还表明,相当比例产妇的产时发热会直接影响产科处理决策。
研究团队设计这项前瞻性研究时制定了严格的纳入与排除标准,以最大限度降低潜在混杂因素对解读产母发热与等位基因评分关系的干扰。通过孟德尔随机化分析获得的遗传学数据表明,较低的白细胞介素-1受体拮抗剂(IL-1Ra)水平与产母发热或产前抗生素治疗风险之间不存在潜在因果关系。构建IL-1Ra遗传评分为研究关键IL-1Ra单核苷酸多态性(SNP)与临床结局的因果关系提供了孟德尔随机化研究手段。在满足一系列明确假设条件的前提下,这种通过等位基因评分映射蛋白质水平的孟德尔随机化方法,能为暴露变量与结局间的因果关系提供证据支持。由于孟德尔随机化比传统观察性研究更不易受混杂因素或反向因果关系影响,该方法可深入揭示IL-1Ra对活跃分娩结局的生物学作用机制。与英国Biobank数据库的数据一致,该研究发现携带特定等位基因评分的女性比例与既往报告相似。EPIFEVER-2研究进一步扩展了这些发现——超过45%的参与者为非白人女性(英国Biobank数据库中93%为英国白人女性)。
尽管孟德尔随机化研究具有天然随机分配个体的优势,但其结果与药物随机对照试验之间仍存在显著差异。要使孟德尔随机化研究得出可靠结论,必须满足三个关键假设:首先,遗传变异必须与目标生物学参数相关。改研究团队的实验室研究显示,局部麻醉剂(布比卡因)与IL-1Ra释放之间存在直接关联。第二项假设中,均未发现IL-1Ra与暴露-结局关系混杂因素存在相关性证据,这一点通过不同等位基因评分组间相似的药物剂量得到印证。第三项假设基于"无多效性"原则,即遗传变异仅通过风险因素影响结局。
该研究的一个普遍优势在于,这个种族混合研究人群的等位基因评分分布与英国生物样本库报告的比例以及IL-1Ra联盟评分报告的结果相似。单核苷酸多态性通过批量分析处理,并由对临床结果不知情的人员报告。这个前瞻性数据集具有高度细化程度,得益于严格控制的纳入/排除标准。然而,缺乏相关蛋白质数据(即循环IL1b/IL-1Ra)是一个局限。若能获得更精确的首次检测到发热或使用抗生素的时间数据,可能会提供更多理解。研究团队承认次要结局的统计效力不足。考虑到要求分娩硬膜外镇痛术的孕妇通常具有不同患者特征(如种族和社会经济地位),以及其他医疗行为、合并症和产科病史,该研究可能存在选择偏倚。另一个局限是未记录剖宫产的时机和指征。测量IL-6和CRP的血浆水平可能有助于进一步了解产妇发热机制。近期使用脂质体RNA新冠疫苗(尤其是这个高风险孕妇群体)可能改变了白细胞介素1-白细胞介素1受体拮抗剂轴,但研究未记录近期新冠疫苗接种状态。虽然产时同意后约2%的脱落率高于预期,但并未实质影响研究主要终点。
总之,对于分娩期间要求硬膜外镇痛术的产妇,遗传决定的较高IL1-Ra水平并未显著增加产时发热、产时抗生素使用或剖宫产的发生概率。
参考文献
EPIFEVER-2 investigators. Interleukin-1 receptor antagonist polymorphisms in women receiving epidural analgesia who develop maternal intrapartum fever: a prospective, multicentre Mendelian randomised study. Br J Anaesth. 2025 Jul;135(1):134-140. doi: 10.1016/j.bja.2025.03.037.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)