首页 > 医疗资讯/ 正文
中心静脉压(Central venous pressure,CVP)的测量从动物模型的初步研究,到作为容量状态标志物和复苏目标的推广,进而指导危重患者治疗的选择,已纳入临床实践70余年,然而CVP监测的效用仍存在争议。现有证据表明因CVP无法预测不同患者群体的容量反应性导致该参数监测被弃用。此外,在不同的手术和非手术人群中,针对特定CVP值进行设定的临床效用仍不确定,这些目标值影响临床结果的机制也不明确。
2025年6月,Anaesthesia在线刊发一篇关于中心静脉压测量与解读的叙述性综述,该综述对72篇关于CVP的文献进行了全文提取和数据综合,探讨了CVP监测的历史发展、生理基础、测量技术及在各种临床场景中的应用证据,并指出CVP单独作为容量反应性预测指标不可靠,但结合趋势分析、波形解读及与其他参数,对评估右心功能、静脉淤血和器官灌注有重要价值。

CVP测量的早期概念与技术发展
首次报道的CVP测量发生于1733年,进一步的犬类动物实验推动了Frank-Starling“心脏定律”的形成,经典的Frank-Starling曲线的解读推断CVP等同于心室前负荷,并暗示CVP可作为血管内充盈度和容量反应性的标志物。1905年,Bliechroder经肘窝进行了人类的首次中心静脉置管,但直到1929年Forssmann实施自我置管后,该技术才被正式报道。
20实际50年代因颈内静脉置管和水柱压力计测量技术的进步,CVP的监测成为医学领域的研究热点。早期志愿者研究显示CVP在补液时暂时性升高而失血则使其下降,这导致CVP监测作为容量反应性标志物的兴起。然而,1973年ArthurGuyton开创性工作推进了对血流动力学、充盈压和CVP的临床理解,但他也警示不应依赖中心静脉压作为容量反应性的标志物,主张采用Guyton模型来解释循环的变化。Guyton模型:CVP受上游和下游压力的共同影响,心输出量由心功能曲线与静脉回流曲线交点决定,心功能曲线与Starling曲线相似,即右心房压力升高会导致心输出量增加,而静脉回流=(平均体循环充盈压-右房压)/静脉回流阻力。因此,右房压升高会降低静脉回流和心输出量。此外,只有当输液促使平均体循环充盈压升高幅度超过右心房压力,或通过恢复塌陷的腹部静脉降低静脉回流阻力时,输液才会增加静脉回流【图1】。
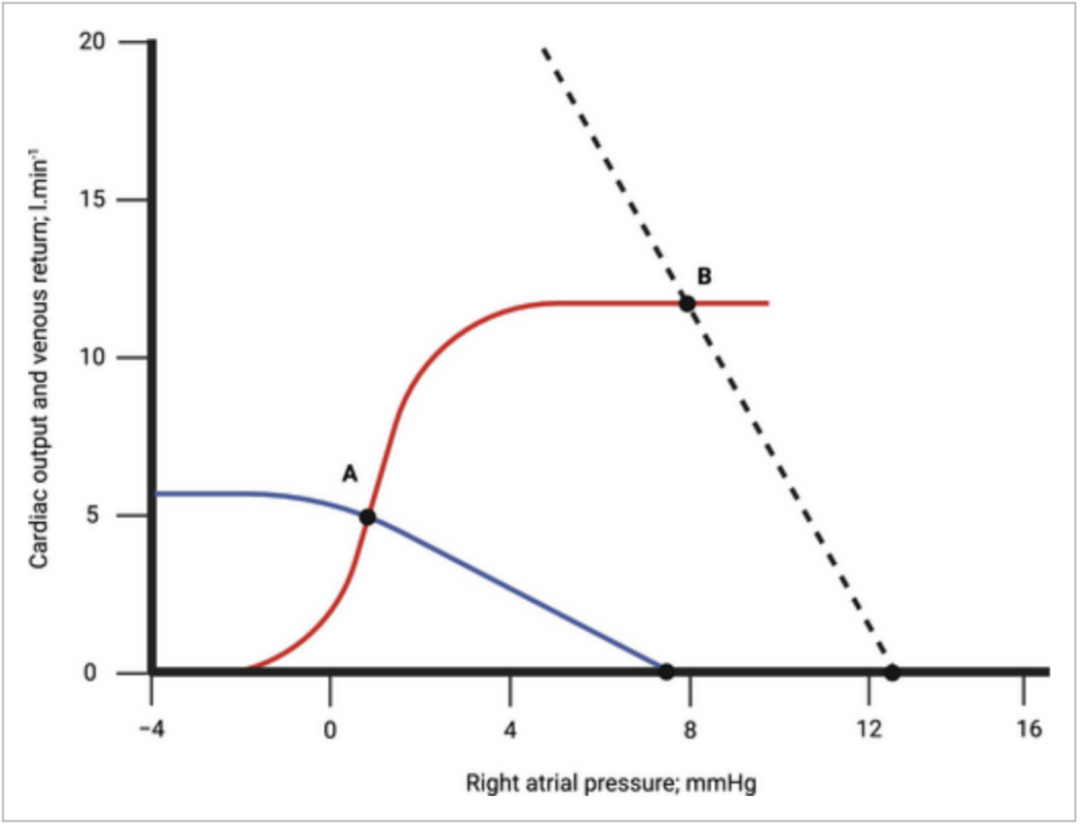
图1. Guyton 的两条曲线结合以模拟循环血流。红线,心功能曲线;蓝线,静脉回流曲线。两者的交集(A)决定了心输出量。当静脉回流较高(黑色虚线)时,心输出量同样增加(B)
CVP的测量技术
测量CVP的金标准是通过中心静脉导管或肺动脉导管,在其穿过右心房测量获得。中心静脉导管的常见置管部位是颈内静脉或锁骨下静脉,导管尖端位于或靠近上腔静脉-右心房交界处。当从膈肌以下部位(如经股静脉)测量CVP时,下腔静脉的导管尖端与右心房无阻塞和压迫的情况下,下腔静脉测量值与上腔静脉测量值的差异在0.23mmHg以内。然而,若存在腹压改变或下腔静脉阻塞、血栓、破裂等情况时,经膈肌以下部位测量CVP的准确性低,难以反映真实值。
压力传感器位置的正确放置并归零至大气压是保证CVP测量值准确的关键。传感器需对齐三尖瓣水平,相当于胸骨角下方5cm水平或胸部前后径的1/3处。这个位置测量的数值比胸部中点位置测量更准确。压力传感器通过三通阀归零至大气压,并需定期重复归零以应对电缆故障或基线漂移。考虑到固有频率和阻尼系数的问题,可通过快冲试验引发方形波形,以评估存在阻尼过低或过度的情况。
在右心室舒张末压或三尖瓣关闭时进行CVP测量,可最准确反映心脏前负荷。获取CVP数值最准确的方法包括:①直接读取波形;②在三次呼吸周期的呼气末期(此时无论是自主呼吸还是机械通气患者,胸膜压力最接近大气压),将床旁监护仪数值冻结在c波起始处。若因气道阻塞或支气管痉挛导致呼气末压力升高,使用该方法会造成CVP假性升高。
CVP的生理学基础
CVP是一项基本的生理变量,由几个关键因素相互作用产生: ①上游压力:取决于血容量和血管容量;②下游压力:特指右心房流出的阻力;③侧向压力:特指胸腔内压力和心包内压力(受机械通气影响最大)。总血容量与平均体循环充盈压呈非线性关系,70%静脉系统中有25%的血液储存于跨壁压高于0 mmHg的静脉中的血容量称为“张力性”血容量,张力性血容量构成平均体循环充盈压,进而驱动静脉回流。CVP仅反映血管内压力,而真实右心房舒张压为血管内压力减去胸腔内压力的综合值,因此除影响右心室顺应性、心律和血容量的因素外,任何改变胸腔内压力的因素也会影响CVP测量值【图2】。
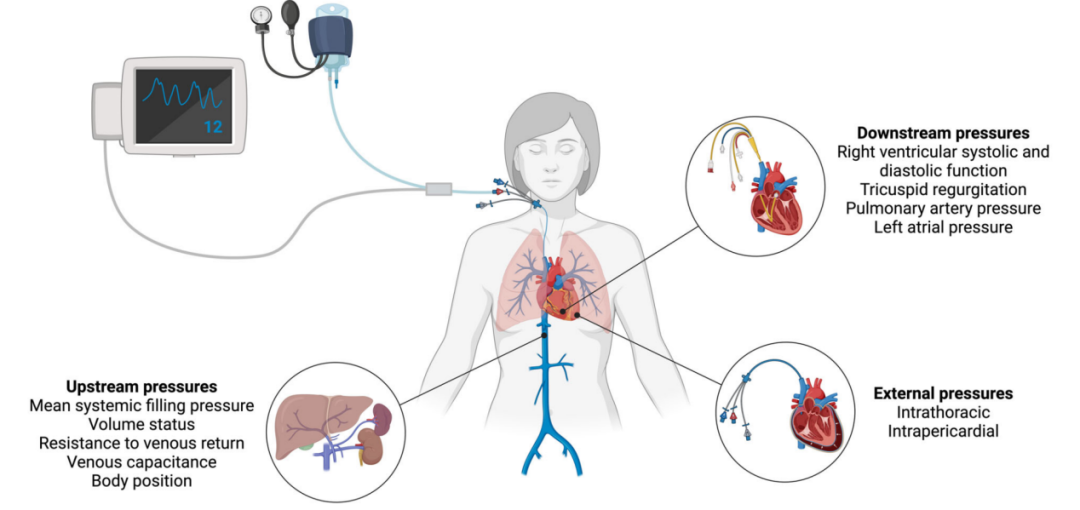
图2. 影响中心静脉压因素的相互作用
典型CVP波形分为a波、c波、v波,其间穿插着x降支和y降支,并随心动周期和呼吸运动波动:a波(心房收缩);c波(右心室等容收缩期三尖瓣向心房膨出);x降(右心室排空期);v波(三尖瓣关闭时心房充盈);y降支(舒张期初始三尖瓣开放)【图3】。
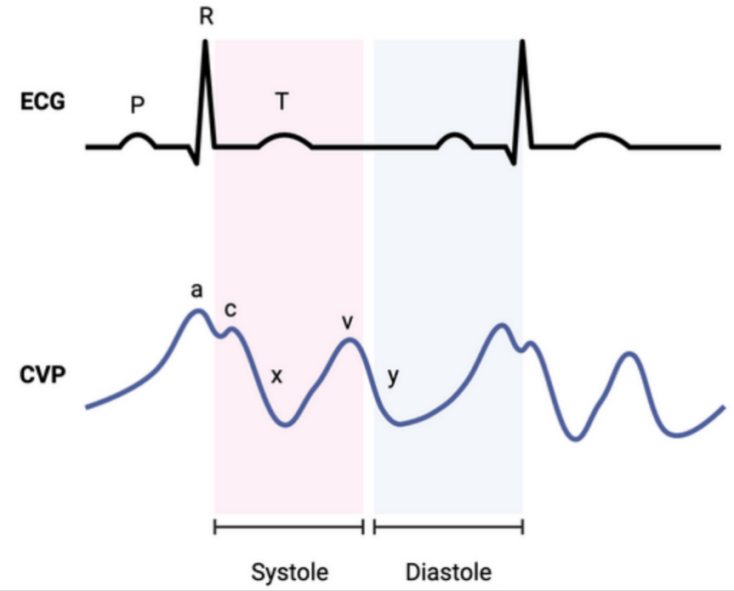
图3. 中心静脉压波形的力学成分与 ECG 的电事件相对应。收缩期(红色区域)包括 c波、x 下降波和 v波;舒张期(蓝色区域)包括a波和y下降波
病理状态下的中心静脉压
CVP波形分析可动态观察右心血流动力学,其波形形态的病理性变化比单一的CVP值能提供更详细、更精细的信息。在严重三尖瓣反流中,v波显著增大并与c波融合,形成巨大“c-v波”,称为“Lancisi征”。若c波缺失,应采用a波峰值压力或与QRS波群终点对应的压力值,以确保测量的准确性。
早期右心室舒张功能不全时,x降支减弱或消失;同时,舒张早期右心房压力升高,继发y降支显著加深。y降支加深本身并非右心室松弛功能受损的特异性表现,而是右心室顺应性下降(无论病因如何)导致右房压升高的通用指标,也可见于缩窄性心包炎等其他疾病【图4】。
现代证据表明,CVP难以准确反映心脏前负荷是否充足,且在危重症患者中无法有效预测容量反应性。研究推测,CVP预测容量反应性能力差的原因,在于静脉回流、右心室收缩与舒张功能、肺血管张力及胸腔内压力之间存在复杂相互作用。目前已不建议依赖CVP评估容量反应性,单一CVP值无法准确反映总血容量状态,不应将其作为唯一的复苏目标。
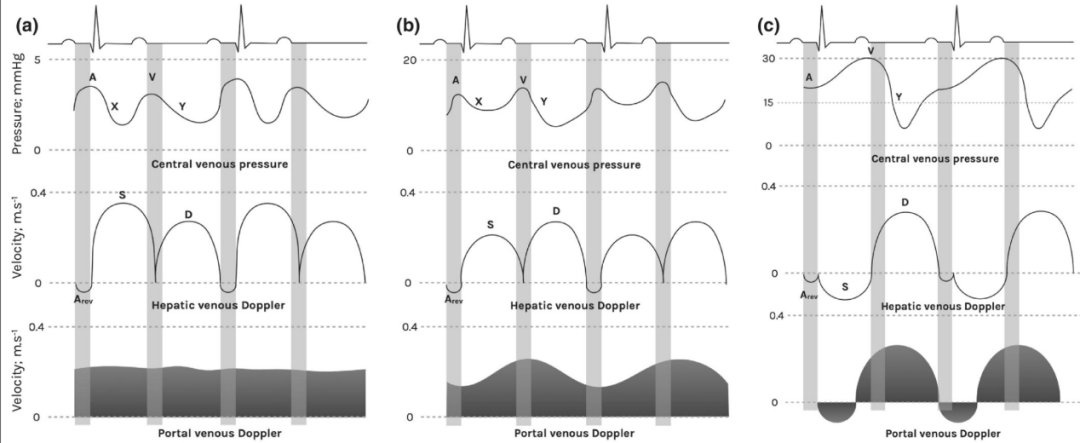
图4. 右心室舒张功能障碍、病理性CVP波形变异和肝静脉及门静脉多普勒超声的相关性(a)正常生理状态;(b)早期右心室舒张功能障碍;(c)晚期右心室舒张功能障碍
CVP与右室舒张功能障碍
CVP升高可能反映了因心室顺应性下降继发的右心室充盈障碍,却无法诊断右心室功能障碍的病因。右心室舒张末期容积由跨壁压和心肌顺应性决定,心包内压和胸腔内压升高会降低右心室跨壁压,而右心室舒张功能受损则需要更高的CVP以促进充盈。
CVP对右心室功能障碍或容量状态缺乏特异性,但其趋势监测在肺动脉高压或左心衰竭等疾病中仍具价值。CVP压力升高可触发后负荷代偿性增加,进而加重右心室充盈障碍,CVP有助于监测右心室舒张功能障碍随时间的进展【图4】。
麻醉医师和重症医师正越来越多地参与肺动脉高压继发右心衰竭风险患者的诊疗。此类患者接受急诊手术时,围手术期死亡率高达15%-50%。中心静脉导管(CVC)置入与监测属于所有麻醉医师的核心技能,在此类情况下,CVP的绝对值、趋势和波形均具重要意义:CVP进行性升高伴平均动脉压下降,可能提示右心室衰竭,需考虑给予正性肌力和/或血管活性药物支持、谨慎的容量管理及
吸入性肺血管扩张剂;CVP波形变化:也可警示麻醉医师右心室功能恶化。
多普勒超声检查(尤其是肝静脉、门静脉和股静脉)已被用于评估其与CVP及右心室功能障碍的关系。腹腔内主要静脉(尤其是肝静脉和门静脉)的多普勒静脉分析与右心室功能障碍及患者预后相关。肝静脉和门静脉的多普勒变化与病理性CVP波形变异高度吻合。这些变化可通过体表超声或经食道超声心动图检测,包括CVP波形分析中x降支消失和y降支加深,可作为右心室舒张功能障碍的补充标志物。将多普勒波形分析与CVP波形分析、CVP趋势及绝对值相结合,可能为整体血流动力学状态和右心室功能提供更全面的信息。
大量证据表明中心静脉压CVP会影响组织灌注,进而可能导致内脏器官损伤。在健康状态下,低CVP对驱动体循环灌注的压力梯度影响极小,然而全身麻醉期间,若平均动脉压为60 mmHg,CVP从5 mmHg升至10 mmHg会使平均动静脉压力(即驱动器官灌注的梯度)降低10%。此外,CVP升高会增加毛细血管压力,改变血管内与组织间隙的流体静压梯度,导致液体进入组织间隙,且无法通过升高平均动脉压抵消这一效应。
有证据表明,CVP升高是接受心脏手术的患者急性肾损伤和死亡率的预测因子,且独立于心输出量。此外,新证据表明,在重症监护患者中,平均动静脉压力对肾损伤的预测独立于CVP,这为CVP升高的患者设定更高平均动脉压目标提供了理论依据;然而,目前还缺乏支持这种做法的前瞻性证据。
在平均动脉压未相应增加的情况下,CVP升高会降低平均动静脉压力,从而减少器官灌注。在消化系统中,平均动静脉压力降低与心-肠综合征(即内脏灌注不足导致缺血、肠道动力改变和细菌移位)的发病机制相关。此类患者的CVP升高可能进一步减少静脉回流,进而降低内脏循环的前向血流量,加重疾病状态。CVP监测可为临床医生提供静脉回流受损的早期指标,若结合平均动脉压和平均动静脉压力进行解读,可预警微循环灌注减少和即将发生的器官灌注紊乱和/或全身淤血【图5】。
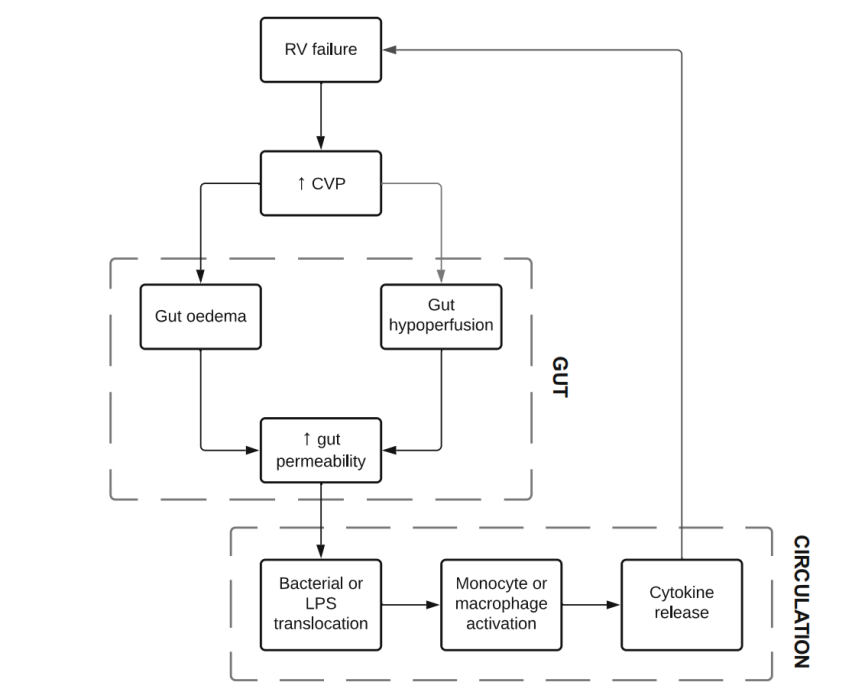
图5. 心-肠综合征的发病机制 RV,右心室;CVP,中心静脉压;LPS,脂多糖
结论
尽管有证据表明,单一CVP绝对值对容量反应性的预测价值有限,但将CVP与波形分析及趋势监测相结合,可以为右心功能、静脉淤血和器官灌注提供有价值的认识。新证据显示,CVP与右心室舒张功能障碍、微循环灌注及多普勒静脉波形等关键生理变量之间存在重要关联,这进一步凸显了CVP监测在围手术期和重症监护环境中的意义。
理解CVP趋势、波形形态及其与其他血流动力学指标的相互作用,对于优化围手术期和重症监护环境中的管理策略至关重要。未来研究方向可能包括优化CVP与先进的监测模式监测方式相结合,同时减少对过时容量评估模式的依赖,以优化患者预后。
原始文献:
Lloyd-Donald P, Fujino M, Waldman B, Miles LF. Measurement and interpretation of central venous pressure: a narrative review. Anaesthesia. 2025. doi: 10.1111/anae.16633.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)