首页 > 医疗资讯/ 正文
γδT细胞在过继性细胞治疗中展现出巨大的潜力,但其肿瘤靶向效率较低。
2025年6月27日,北京大学林坚、陈兴、郭红燕、Chen Long共同通讯在National Science Review在线发表题为“Chemical engineering of γδ T cells with cancer cell-targeting antibodies for enhanced tumor immunotherapy”的研究论文,该研究报告了用于增强肿瘤治疗的抗体-γδT细胞偶联物的开发。
该研究通过评估细胞表面的不同生物分子,唾液酸(各种细胞表面聚糖的末端糖)被确定为通过用含有生物正交官能团的非天然糖标记代谢聚糖将抗体锚定在γδT细胞上的最佳位点。程序性死亡配体1(PD-L1)特异性纳米体(αPD-L1)通过点击化学结合到γδT细胞上,产生的αPD-L1-γδT淋巴细胞对PD-L1阳性癌症细胞系、患者来源的原发性癌症细胞和活体小鼠中的异种移植肿瘤表现出增强的细胞毒性。从机制上讲,αPD-L1-γδT细胞通过与PD-L1结合靶向癌症细胞和肿瘤,并诱导癌症细胞焦亡。此外,αPD-L1-γδT细胞重塑肿瘤微环境,使其具有免疫活性,至少部分是通过CCR5-CCL5轴募集和激活CD8+T细胞。这项工作为γδT细胞的化学工程提供了一种通用的策略,以改善治疗应用。
与传统的αβT(αβT)细胞相比,γδT(γδT)细胞是T淋巴细胞的独特亚群,具有独特的T细胞受体(TCR),即γ链和δ链。不同于αβ TCRs对主要组织相容性复合体(MHC)依赖性抗原的识别,γδ T细胞的TCRs直接识别蛋白质抗原,即以磷抗原作为分子胶形成的BTN3A1/BTN2A1复合体。不依赖于MHC的抗原识别机制使γδ T细胞成为同种异体细胞治疗的理想选择,因为预计不会发生移植物抗宿主病。γδ T细胞在体外和体内都表现出抗肿瘤活性,这引起了人们对基于γδ T细胞的过继细胞治疗的广泛兴趣。然而,像大多数用于过继细胞转移的免疫细胞一样,体外扩增和未工程化的γδ T细胞通常导致有限的临床益处,这是由于低肿瘤靶向效率和转移细胞的有限活化。
为了克服这些限制,已经开发了几种工程方法来提高γδ T细胞的抗肿瘤功效。例如,嵌合抗原受体(CARs)已经被工程化到γδ T细胞,受到αβ CAR-T细胞巨大成功的启发。尽管前景看好,但基因工程和γδ CAR-T细胞的大规模生产仍然昂贵且耗时。或者,细胞表面的化学工程代表了一种调节免疫细胞(如自然杀伤细胞和αβ CAR-T细胞)功能的多用途和有前途的方法。因此,假设对γδ T细胞表面进行具有肿瘤靶向功能的化学工程改造,将为工程改造的γδ T细胞提供增强的抗肿瘤活性和易于生产。
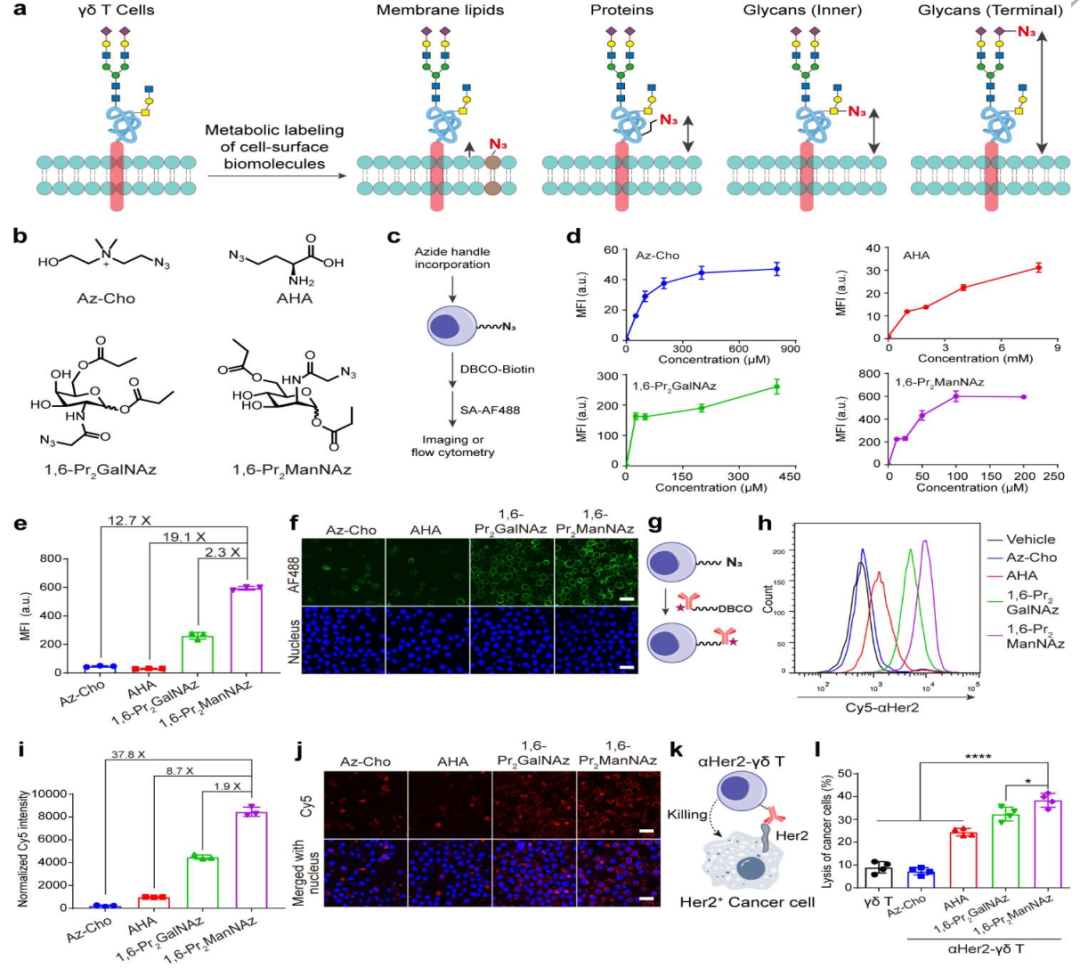
γδT细胞表面抗体的结合(图源自National Science Review)
基于这些考虑,研究人员报告了通过细胞表面聚糖的化学工程开发抗体-γδT细胞偶联物的进展,并证明了其在体外和体内的增强抗肿瘤功效。通过评估不同的细胞表面生物分子,选择细胞表面唾液酸(各种细胞表面聚糖的末端糖)作为肿瘤靶向抗体的锚定位点。通过利用最近基于1-O-乙酰基-N-叠氮基乙酰基-甘露糖胺-6-双(S-乙酰基-2-硫乙基)-磷酸盐(AMS-ManNAz-P)开发的快速代谢聚糖标记策略(fMGL),抗体被高效快速地结合到细胞表面唾液多糖上,而不会干扰γδT细胞的功能。
在异种移植小鼠模型中,与抗PD-L1抗体结合的γδT细胞(αPD-L1γΔT细胞)对PD-L1参与的癌症细胞系和患者来源的原发性癌症细胞表现出有效的杀伤作用,并抑制肿瘤生长。从机制上讲,αPD-L1与PD-L1的结合将αPD-L1-γδT细胞靶向癌症细胞和肿瘤,从而诱导癌症细胞的焦亡。此外,αPD-L1-γδT细胞的浸润塑造了免疫活性肿瘤微环境(TME),至少部分是通过CCR5-CCL5轴募集和激活CD8+T细胞。因此,该研究中开发的抗体-γδT细胞偶联物为工程化具有增强抗肿瘤活性的γδT淋巴细胞提供了一种有前景的策略。
参考信息:
https://academic.oup.com/nsr/advance-article/doi/10.1093/nsr/nwaf256/8176682?searchresult=1
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)