首页 > 医疗资讯/ 正文
关节周围肌肉萎缩是骨关节炎(OA)患者的常见问题,但其原因尚不清楚。
2025年6月27日,陆军军医大学倪振洪、周思儒、陈林、连继勤共同通讯在Nature Aging在线发表题为“Senescent macrophages induce ferroptosis in skeletal muscle and accelerate osteoarthritis-related muscle atrophy”的研究论文,该研究证明了小鼠股四头肌的慢性炎症与OA一致,其特征是巨噬细胞增加、炎症途径激活和组织血管化。
研究发现,在OA进展过程中,巨噬细胞逐渐表现出衰老表型的增加,并通过旁分泌诱导铁死亡来促进肌肉萎缩。从机制上讲,铁过载诱导的线粒体损伤导致天冬酰胺代谢物减少,通过抑制mTORC1–HMGCR信号传导来损害辅酶Q10(CoQ10)的合成。最终,这种级联反应增强了脂质过氧化,促进了骨骼肌细胞的铁死亡。心脏药物辅酶Q10可以通过抑制铁死亡来减轻肌肉萎缩,从而减少OA关节的病理损伤。该研究结果为OA患者肌肉萎缩的潜在管理提供了见解。

骨关节炎(OA)被认为是一种涉及病理变化的整体关节疾病,包括软骨损伤、软骨下骨重塑和滑膜炎症。关节周围的肌肉萎缩是OA患者的一种常见身体表现,是OA发病的指标,与膝关节症状和关节病理恶化密切相关。然而,OA相关肌肉萎缩的病理特征和分子机制在很大程度上仍然未知,这极大地限制了临床治疗的有效性。
细胞衰老是细胞周期停滞的永久状态,在不同的生理和病理过程中起着重要作用。高通量测序的最新数据确定了衰老骨骼肌细胞衰老的典型特征。清除衰老细胞已被证明可以增强多种肌肉疾病的肌肉再生并抑制肌肉萎缩。相反,衰老细胞在某些情况下也可能积极调节肌肉再生。例如,它们在蝾螈模型中可以通过促进肌肉去分化来增强肢体再生。然而,尚不清楚衰老细胞是否参与了OA相关的肌肉萎缩。
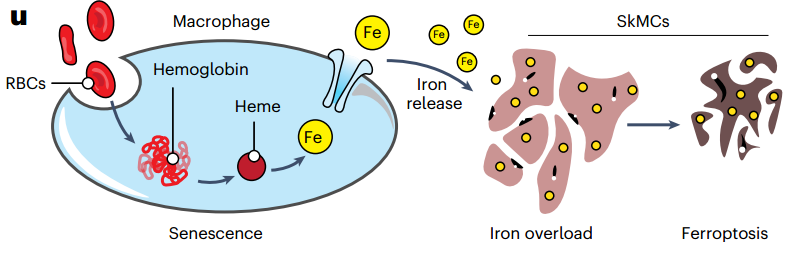
机理模式图(图源自Nature Aging)
铁死亡是一种程序性细胞死亡,其特征是铁依赖性膜脂质过氧化(LPO),这也与骨骼肌的再生或萎缩有关。在癌症恶病质实验模型中,组织过滤中性粒细胞可引发脱铁性贫血和肌肉萎缩。抑制铁死亡已被证明可以有效地保护脂肪毒性肥胖小鼠的骨骼肌完整性和质量。作为一种氧化还原活性代谢产物,辅酶Q10(CoQ10)可以通过调节其氧化还原状态在质膜和线粒体内膜中发挥抗氧化剂的作用,从而有效抑制LPO和铁死亡。线粒体肌病患者的骨骼肌中辅酶Q10减少。在OA患者中,CoQ10水平与抗氧化能力、肌肉质量、肌肉力量和肌肉耐力之间也观察到正相关。然而,铁死亡在OA相关肌肉萎缩发病机制中的作用和潜在机制仍然难以捉摸。
在该研究中,研究人员探究了OA受累关节周围股四头肌的组织病理学改变和分子特征。数据显示,慢性炎症是股四头肌的主要病理特征,伴随着大量巨噬细胞的浸润,表现出衰老样表型。研究发现,衰老的巨噬细胞通过诱导骨骼肌铁死亡加剧了股四头肌萎缩。从机制上讲,雷帕霉素复合物1(mTORC1)-HMG-CoA还原酶(HMGCR)途径的天冬酰胺机制靶标的抑制导致内源性辅酶Q10的减少,从而损害了骨骼肌细胞(SkMCs)对铁死亡的防御系统。此外,外源性补充辅酶Q10显著增强了股四头肌质量,改善了OA关节的病理损伤。总之,该研究阐明了股四头肌萎缩的主要细胞事件和潜在机制,从而为OA治疗提供了一种有前景的药物(辅酶Q10)。
参考信息:
https://www.nature.com/articles/s43587-025-00907-0#Sec49
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)