首页 > 医疗资讯/ 正文
【亮点提要】
- 血液嗜酸细胞计数和呼气一氧化氮(FeNO)均与哮喘严重发作风险呈显著正相关,且两者联合预测具有协同增强效应。
- 哮喘既往严重发作史、疾病严重度、肺功能下降及症状控制不佳等临床因素均为哮喘发作的独立风险因子。
- 有趣的是,适度的支气管扩张剂反应性与严重哮喘发作风险降低相关,提示诊断性指标与风险预测的复杂关系。
研究概览
2025年4月8日,《柳叶刀·呼吸医学》(The Lancet Respiratory Medicine)在线发表了一项题为“Inflammatory and clinical risk factors for asthma attacks(ORACLE2): a patient-level meta-analysis of control groups of 22 randomised trials”研究。该研究由荷兰莱顿大学医学中心和加拿大舍布鲁克大学等国际多中心合作完成,收集整合了22项随机对照试验(RCT)对照组共6513例哮喘患者的个体患者数据(IPD),通过负二项回归模型系统评估了血液嗜酸细胞计数、呼气一氧化氮(FeNO)以及传统临床指标对哮喘发作风险的独立及联合预测价值。研究发现,炎症生物标志物作为可调节的风险因素,具有显著的增量预测作用,支持将其纳入临床风险分层体系,助力实现个体化风险管理及精准干预。

研究背景
哮喘作为一种慢性气道炎症性疾病,全球患者约4亿,且高收入国家中发病率高达10%。哮喘发作不仅造成患者症状反复加重,还严重影响生活质量,增加医疗负担并升高死亡风险。传统的风险评估主要依赖既往发作史、肺功能、症状评分等临床指标,但这些大多反映既成的疾病损伤或不易直接调控的个体特征,难以为预防提供精准靶向。
近年来,越来越多证据表明2型气道炎症(type 2 inflammation)是哮喘发作的重要驱动机制,且可以通过血液嗜酸细胞计数和呼气一氧化氮(FeNO)两项简便、无创的生物标志物在临床中加以定量监测。2型炎症既是发病过程中的关键致病途径,也是现有及新兴抗炎疗法的靶点。然而,迄今为止,尚缺乏大规模、高质量的个体患者数据分析系统阐明这两种炎症指标在哮喘发作风险预测中的独立和联合增量价值,以及它们与其他临床风险因子的综合关系。
因此,本研究通过联合22项RCT对照组的个体患者数据,旨在量化血液嗜酸细胞计数和FeNO与严重哮喘发作风险的多变量预测关系,评估其在哮喘风险分层中的应用潜力,为临床个体化管理提供依据。
研究方法
本系统评价与荟萃分析(ORACLE2)纳入了1993年至2021年4月在MEDLINE数据库检索到的所有随机对照试验,筛选标准为:研究对象为≥12岁哮喘患者,设有固定治疗方案且对照组患者无治疗强度调整,且基线同时测量血液嗜酸细胞计数和FeNO,随访时间≥6个月。研究团队独立复核行政、风险偏倚情况,最终纳入22项RCT对照组患者个体数据共6513例。
采用多重插补法处理缺失值。基线变量包括临床指标(哮喘病史、肺功能、症状评分、治疗步骤等)与炎症生物标志物(血液嗜酸细胞计数、FeNO)。以负二项回归模型计算调整后年化哮喘严重发作率(≥3天系统性糖皮质激素治疗)与各预测因子之间的关联,综合考虑多种协变量及试验间异质性,证据等级采用GRADE体系评估。
研究结果
纳入的6513例患者中,92%为中重度哮喘(GINA步骤3-5),女性占64%。随访5482人·年期间共记录4615次严重哮喘发作,年化发作率约0.84次/人·年。患者基线中位血液嗜酸细胞计数为0.25×10⁹/L,FeNO中位数23 ppb。
主要多变量分析结果指出:
- 血液嗜酸细胞计数每10倍增加,哮喘发作风险增加48%(RR 1.48,95% CI 1.30–1.68)。
- FeNO每10倍增加,发作风险增加44%(RR 1.44,95% CI 1.26–1.65)。
- 既往12个月有哮喘严重发作史的患者风险是无发作患者的1.94倍(95% CI 1.61–2.32)。
- GINA治疗步骤5(严重哮喘)较步骤3(中度哮喘)风险增加57%(RR 1.57,95% CI 1.22–2.03)。
- 肺功能指标FEV1%每降低10%,风险增加11%(RR 1.11,95% CI 1.08–1.15)。
- 症状控制评分ACQ-5每增加0.5分,风险增加10%(RR 1.10,95% CI 1.07–1.13)。
此外,二者联合高水平(血嗜酸细胞≥0.30×10⁹/L且FeNO≥50 ppb)患者的发作风险显著高于两者低水平者(RR 1.47 vs 0.76)。这一协同增益具有高度统计学显著性(交互作用p=0.045)。
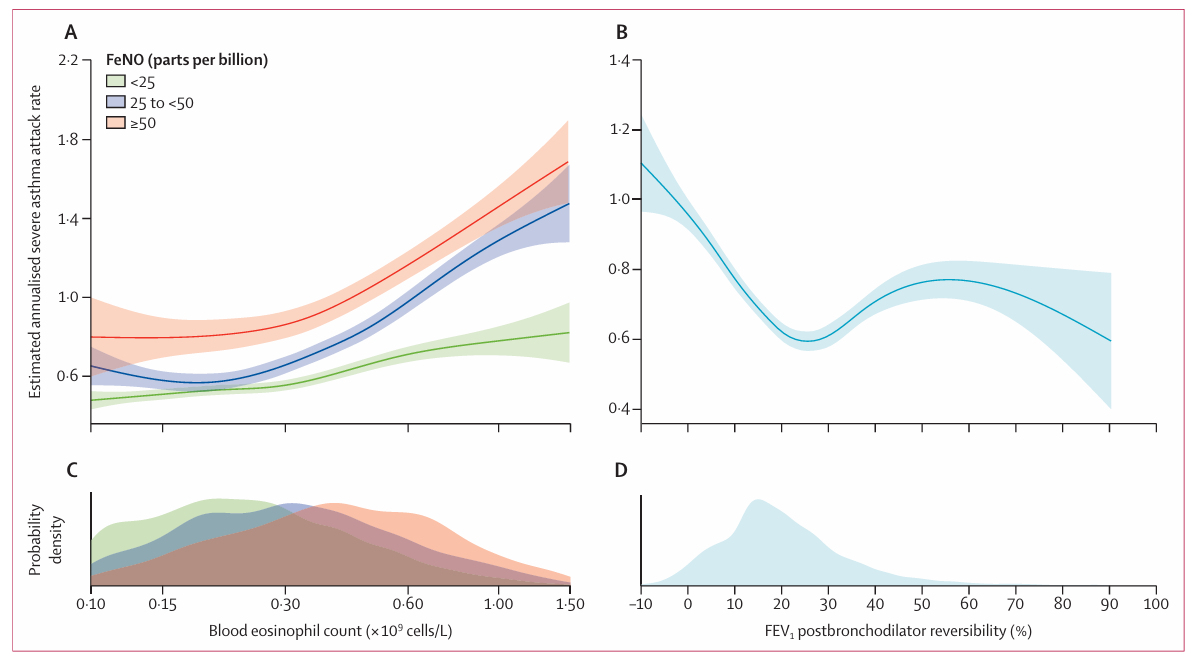
图:不同FeNO水平下血液嗜酸细胞计数与哮喘发作风险的关系曲线;血液嗜酸细胞计数与FeNO联合分布密度及肺功能反应性的非线性风险关联说明了复杂的生物学互作
有趣的是,支气管扩张剂反应性(FEV1 反应率)每增加10%,哮喘发作风险下降7%(RR 0.93,95% CI 0.90–0.96),呈非线性趋势,轻度反应(<25%)风险最低,而>25%反应者风险相对增高。
其他独立风险因素包括女性性别、较高BMI、既往住院次数、吸烟史(尤其前吸烟者)以及部分上气道合并症(过敏性鼻炎、鼻息肉性或非息肉性慢性鼻窦炎)。年龄、血清IgE及吸入激素依从性未表现为稳定的预后指标。
研究还指出各研究间患者基线异质性大(C统计量0.58–0.95),单因素分析异质性显著(I²达0.56–0.97),但多变量模型能够稳定端定这些风险关系。
研究价值与意义
该研究首次通过大规模、多中心的随机试验对照组患者级数据,系统量化证实了血液嗜酸细胞计数和FeNO这两类反映2型气道炎症的无创标志物在预测哮喘严重发作风险中发挥的关键而互补作用。与传统临床风险因子相比,这些炎症生物标志物不仅独立且显著增加了风险预测能力,尤以二者联合评估效果显著。
相较于既往以临床症状、肺功能为核心的风险分层方法,本研究揭示了以2型炎症生物标志物为中心的风险识别策略的优势,为精准预防提供了重要的入手点。2型炎症标志物的变动可以反映抗炎治疗(包括吸入皮质激素及生物制剂)效果,具有更大临床指导价值。此外,适度支气管反应性与较低风险的发现挑战了传统对反应性诊断意义的简单认知,提示临床风险预测需结合多维信息。
研究数据来源于设计严谨的RCT对照组,确保随访监测和数据质量,强化了预后因子评估的可靠性。多变量模型解释了23%的发作风险变异,提示未来整合更多潜在机制指标可进一步提升预测精度。
总体而言,ORACLE2研究为哮喘管理提供了科学依据,强调将血液嗜酸细胞计数和FeNO纳入临床风险评估标准,推动以炎症为导向的分层治疗,实现个体化精准防控。研究结果也为新疗法靶点筛选和治疗反应预测提供了重要参考,有助于提升哮喘患者预后和生活质量。
梅斯小编点评:
本研究通过创新整合22项国际哮喘临床试验对照组的大规模患者级数据,系统量化了生物标志物与传统临床指标的联合发作风险预测价值,具有里程碑意义。特别是确认了血液嗜酸细胞与FeNO联合作为哮喘发作风险的增量且协同预测指标,有助于突破单一指标局限,推动临床从症状管理向机制精准防治转型。
未来研究值得探索如何将这些生物标志物嵌入决策支持系统,实现动态、个体化的风险监测和治疗调整。同时,亟需补充社会经济因素和多样化种族群体数据,以全面评估哮喘发作的多维驱动机制。此外,探索支气管反应性与发作风险的非线性关系,为重新定义哮喘表型及个体治疗靶点开辟了新思路。长远看,结合基因组学、环境暴露及免疫组学多组学数据构建更精细化预测模型依然是未来趋势。
原始出处
Meulmeester FL, Mailhot-Larouche S, Celis-Preciado C, et al. Inflammatory and clinical risk factors for asthma attacks (ORACLE2): a patient-level meta-analysis of control groups of 22 randomised trials. Lancet Respir Med. 2025;13(6):505–516. https://doi.org/10.1016/S2213-2600(25)00037-2
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)