首页 > 医疗资讯/ 正文
骨关节炎(OA)是全球最常见的退行性关节疾病,以软骨退变、炎症及骨重塑为特征,影响全球约5.95亿人,是致残的主要原因之一。传统治疗如非甾体抗炎药(NSAIDs)和关节腔注射虽能缓解症状,但存在胃肠道毒性、软骨损伤加重及疗效短暂等问题。手术置换适用于晚期患者,但存在感染和假体寿命限制。壳聚糖(chitosan)是一种天然多糖,具有软骨保护、抗炎及促进细胞增殖的特性,但其水溶性差和渗透性低限制了临床应用。纳米技术通过制备壳聚糖纳米颗粒(NPs)解决了上述问题,显著提高生物利用度和靶向性。本研究旨在系统评价壳聚糖NPs在膝OA中的疗效、安全性及作用机制,为优化治疗策略提供依据。

本研究为系统综述,遵循PRISMA指南,检索PubMed、Cochrane Library、ScienceDirect等数据库(2000–2024年),使用布尔逻辑关键词筛选涉及壳聚糖NPs治疗膝OA的体外、体内及临床研究。纳入标准包括明确使用壳聚糖NPs、以膝OA为模型、报告疗效或机制数据;排除非OA研究、未明确结局指标或数据不全的文献。由两名研究者独立筛选文献并提取数据,分歧通过讨论解决。质量评估采用SYRCLE偏倚工具(动物实验)和QUADAS-2(临床研究)。数据分析以定性合成和关键数据提取为主,重点关注软骨再生、炎症调控及临床结局指标。
研究结果
体外研究:壳聚糖NPs显著促进软骨细胞增殖(如Wang等研究显示增殖率提升至36.42% vs 对照组13.62%)并抑制基质金属蛋白酶(MMP-1/MMP-13 mRNA下降50%)。负载姜黄素的壳聚糖NPs可上调Ⅱ型胶原表达(COL2A1增加40%),同时降低IL-1β和TNF-α水平(分别减少60%和55%)。抗氧化方面,羟基酪醇壳聚糖NPs使SOD2活性提升18%–42%,并减少H₂O₂诱导的细胞损伤。
体内研究:动物模型中,壳聚糖NPs显著改善关节病理。Kang等报道壳聚糖NPs使OARSI评分降低3分,软骨厚度增加40%,且关节腔滞留时间达24天。Ramírez-Noguera等发现NPs减少软骨下骨丢失,Mankin评分从7分降至2分。抗炎方面,负载塞来昔布的壳聚糖NPs使COX-2表达下降70%,TNF-α减少65%。Gao等证实壳聚糖-SOD复合物可抑制IL-6和IL-1β(分别降低50%和45%),并减轻氧化应激(MDA水平下降35%)。
临床数据:临床试验显示,壳聚糖NPs联合甲氨蝶呤治疗6个月后,ACR20/50/70应答率分别为72.41%、53.45%和34.48%,与阿达木单抗相当(P>0.05)。安全性方面,仅2例出现轻度肝损伤和带状疱疹,胃肠道反应发生率低(≤5%)。成本效益分析表明,壳聚糖NPs总费用较阿达木单抗降低54.8%,质量调整生命年(QALY)增益显著(10.08 vs 9.86)。
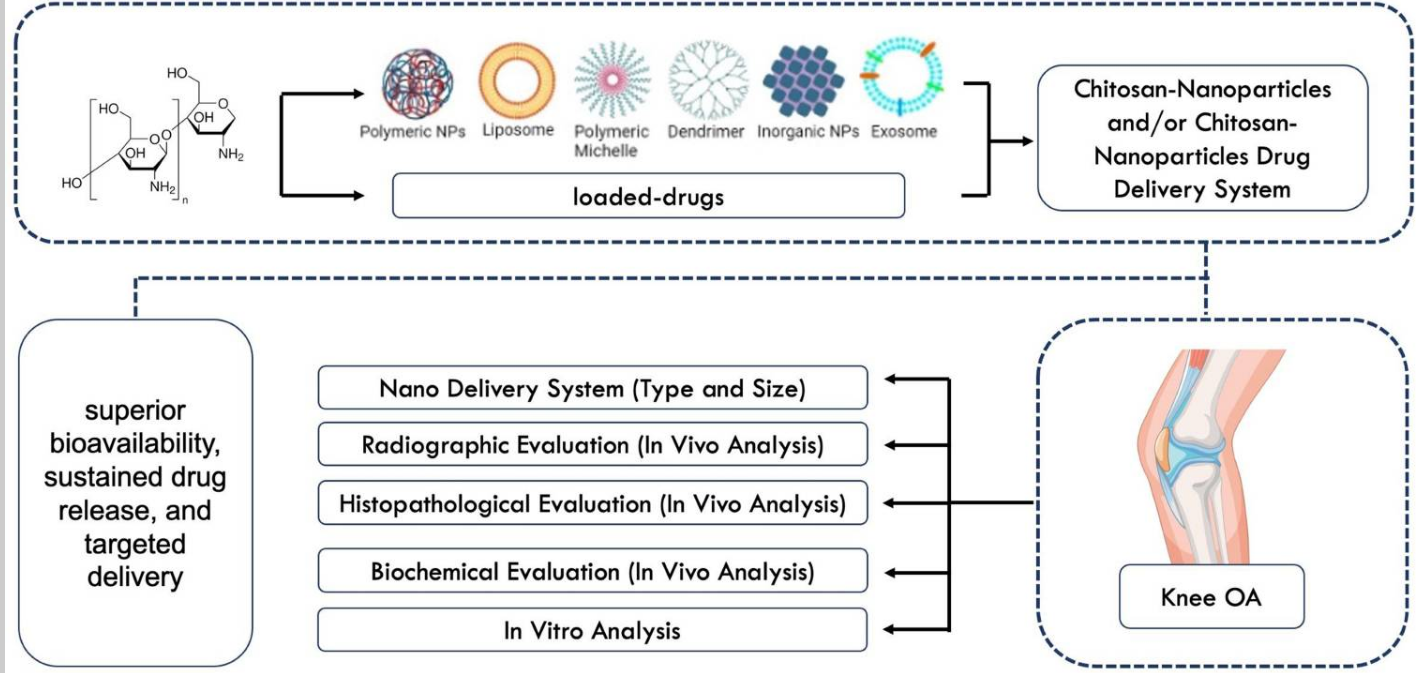
多糖基纳米载体在骨关节炎治疗中的应用
壳聚糖NPs通过促进软骨再生、抑制炎症及调控氧化应激,在膝OA治疗中展现出多重优势。其靶向缓释特性可减少给药频率,降低成本,且生物相容性优于传统生物制剂。然而,纳米颗粒尺寸(50–400 nm)和降解速率的异质性限制了疗效稳定性,需进一步优化配方。未来研究应聚焦于延长关节腔滞留时间(如PEG修饰)和增强载药效率(如外泌体载体),以推动临床转化。本综述支持壳聚糖NPs作为膝OA的潜在替代疗法,尤其适用于长期管理及医疗资源有限地区。
原始出处:
Novy TCT, Joni IM, Lesmana R, Biben V, Setiawan. Chitosan Nanoparticles as an Alternative Therapeutic Approach for Knee Osteoarthritis Treatment: A Systematic Review. Int J Nanomedicine. 2025 May 17;20:6187-6203. doi: 10.2147/IJN.S503829. PMID: 40400782; PMCID: PMC12094476.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)