首页 > 医疗资讯/ 正文
肝癌是全球癌症相关死亡的第三大杀手,约70%患者确诊时已处于中晚期,丧失手术机会。经导管动脉化疗栓塞术(TACE)联合放射治疗(RT)是临床治疗不可切除肝癌的主要方案,但传统化疗药物与放疗的协同效率低下,且存在脱靶毒性等瓶颈。厦门大学公共卫生学院刘刚教授联合医学院楚成超教授团队深耕肝癌精准治疗领域,在《Advanced Functional Materials》发表重要研究成果“X-Ray Triggered Phase SHIFT in Radiosensitizer-Lipiodol Formulation for Controlled Synergistic TAE−XDT Cancer Therapy”。团队研发出新型纳米放射增敏剂 - 碘油制剂(DSeSeP-API (Lip)),创新性提出 “X-tag”(X 射线一触即发式相移)策略,通过 X 射线诱导的三重动态相移效应,首次实现栓塞治疗与精准增敏放疗的时空协同,为肝癌治疗提供全新范式。
核心技术:“3S” 效应赋能,打造智能递送系统
1、相移触发,精准释放
团队设计的 AuPtICG (API) 纳米颗粒搭载 X 射线敏感的二硒键(Se-Se)连接体,通过团队自主研发的SHIFT技术(1S - SHIFT),实现在碘油载体中稳定存在(2S - Stability)。当 TAE 将药物精准输送至肿瘤部位后,首次 X 射线照射(1X-Tag)触发二硒键断裂,亲水性放疗增敏剂(SeP-API)从碘油相迅速转移至肿瘤组织水相(3S – phase Shift,相移),避免了传统制剂的过早释放或过缓问题。
2、时空可控,协同增效
利用自主研发的超稳定均匀混合技术(SHIFT),构建了稳定的碘油 - 纳米颗粒复合体系。在肿瘤细胞对 SeP-API 摄取达到峰值时,二次 X 射线照射(2X-XDT)激活高 Z 元素(Au/Pt)的物理剂量沉积效应与吲哚菁绿(ICG)的化学 ROS 生成机制,通过 “物理增敏 + 化学杀伤” 双重途径,显著增强肿瘤细胞凋亡,同时减少正常组织损伤。
3、三重验证,安全高效
体外验证:在 HepG2 细胞(2D)及脱细胞肝模型(3D)中,X 射线触发后 0.5 小时内即可观察到荧光信号增强,证实相移过程一触即发的快速且可控;
体内疗效:小鼠皮下瘤模型验证了API显著放疗增敏效果;大鼠原位肝癌模型显示,DSeSeP-API (Lip)+X 组肿瘤生长抑制率显著高于单一治疗组;均无明显全身毒性;
机制创新:通过 CT 成像与 MRI 动态监测,揭示碘油作为 “能量池” 协同纳米颗粒增强 X 射线沉积的独特机制,为放射增敏剂设计提供新思路。
临床价值:从 “联合治疗” 到 “精准协同” 的跨越
相较于传统 TACE-RT 方案,该策略突破了三大瓶颈:
稳定性难题:解决了水溶性药物在碘油中易分层的问题,制剂可稳定保存一周以上;
释放可控性:X 射线作为 “分子开关”,实现了治疗药物在时空上的精准释放,避免系统毒性;
协同效应最大化:通过两次 X 射线照射的时序设计,使放射增敏剂在肿瘤细胞内的富集与作用达到最优匹配,显著提升放疗疗效。
研究展望:开启 TAE-XDT 精准治疗新纪元
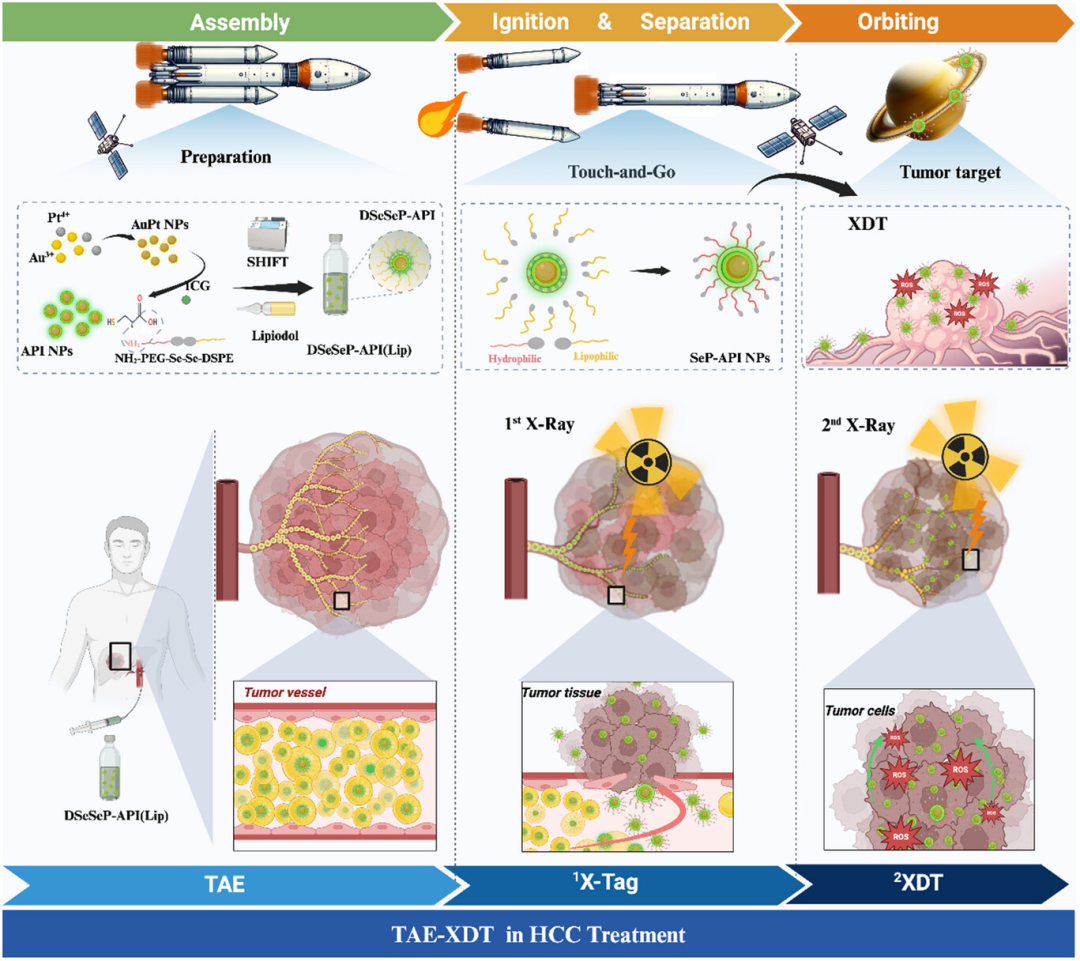
这项研究不仅构建了 “卫星发射式” 的智能递送系统(从碘油载体 “火箭” 分离出 SeP-API “卫星”,精准进入肿瘤细胞 “轨道”),更首次将 X 射线触发的相移概念引入肝癌联合治疗,为开发新型放射增敏剂载体提供了普适性策略。未来,团队将进一步优化 “X-tag” 时间窗口,探索其在肝转移癌等复杂场景中的应用,为更多癌症患者带来精准治疗新希望。
相关论文以 “X-Ray Triggered Phase SHIFT in Radiosensitizer-Lipiodol Formulation for Controlled Synergistic TAE−XDT Cancer Therapy” 为题发表于Advanced Functional Materials。本研究得到国家重点研发计划、国家自然科学基金等项目资助。
参考文献:
Q. Dai, L. Wang, S. Shao, Z. Jia, S. F. A. Rizvi, X. Gao, M. Teng, H. Chen, E. Ren, C. Chu, G. Liu, X-Ray Triggered Phase SHIFT in Radiosensitizer-Lipiodol Formulation for Controlled Synergistic TAE−XDT Cancer Therapy. Adv. Funct. Mater. 2025, 2501159.
原文链接:
https://doi.org/10.1002/adfm.202501159
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)