首页 > 医疗资讯/ 正文
原发性肺黏液样肉瘤(PPMS)是一种极为罕见的低级别恶性肉瘤。这种肿瘤常浸润肺组织,并在支气管内生长。它可通过涉及EWSR1基因的基因重排以及独特的染色体易位t(2; 22)(q33; q12)来识别,主要变异类型为EWSR1::CREB1融合。PPMS于2015年首次被WHO分类所认可,当时它属于间叶性肿瘤类别。随后,在2021年的WHO肺部肿瘤分类中,它被归类为肺间叶性肿瘤。PPMS起源于支气管壁、肺间质或血管中的间叶组织成分。其临床表现通常无特异性,有时仅在体检时才能发现,这使得它很难与其他肺部肿瘤相鉴别。



一位40多岁女性的临床病理诊断为“倾向于肺黏液样肉瘤”,建议FISH检测EWSR1等辅助诊断。该患者送检石蜡切片+对照血,进行了我司“骨与软组织肿瘤 DNA272+RNA1560 基因检测”项目检测。这项检测采用先进的目标区域探针捕获技术和二代测序技术,基于DNA+RNA双组学平台,面向骨与软组织肿瘤患者,预测可能获益的靶向、免疫、化疗等治疗方案,同时辅助预后评估、分子分型以及遗传风险评估。该患者的基因检测结果显示,RNA水平检出EWSR1-CREB1基因融合,进一步辅助肺黏液样肉瘤的诊断。

一、PPMS的流行病学与临床特征
PPMS是一种极为罕见的低级别肉瘤,表1汇总了共计39例临床病例。PPMS在临床上表现出的大多数症状都不具有特异性,比如咳嗽、咯血和体重减轻。在这39例病例中,女性患者有20例,男性患者有19例,男女比例为0.95:1。PPMS患者的年龄范围在21岁至80岁之间,中位年龄为43.6岁。在有记录的病例中,12人从不吸烟,而11人有吸烟史。这表明PPMS的发生与吸烟史没有直接关联。PPMS在肺部并没有特定的好发部位偏好,它可以侵犯左右肺,但更常见于右肺。PPMS通常会浸润支气管组织,在39例病例中有17例表现出向支气管内生长的趋势,4例没有支气管内受累的情况,其余病例没有提供足够的信息。不过,这种肿瘤也可以在肺实质外发生,出现在叶间裂内而不侵犯肺实质。
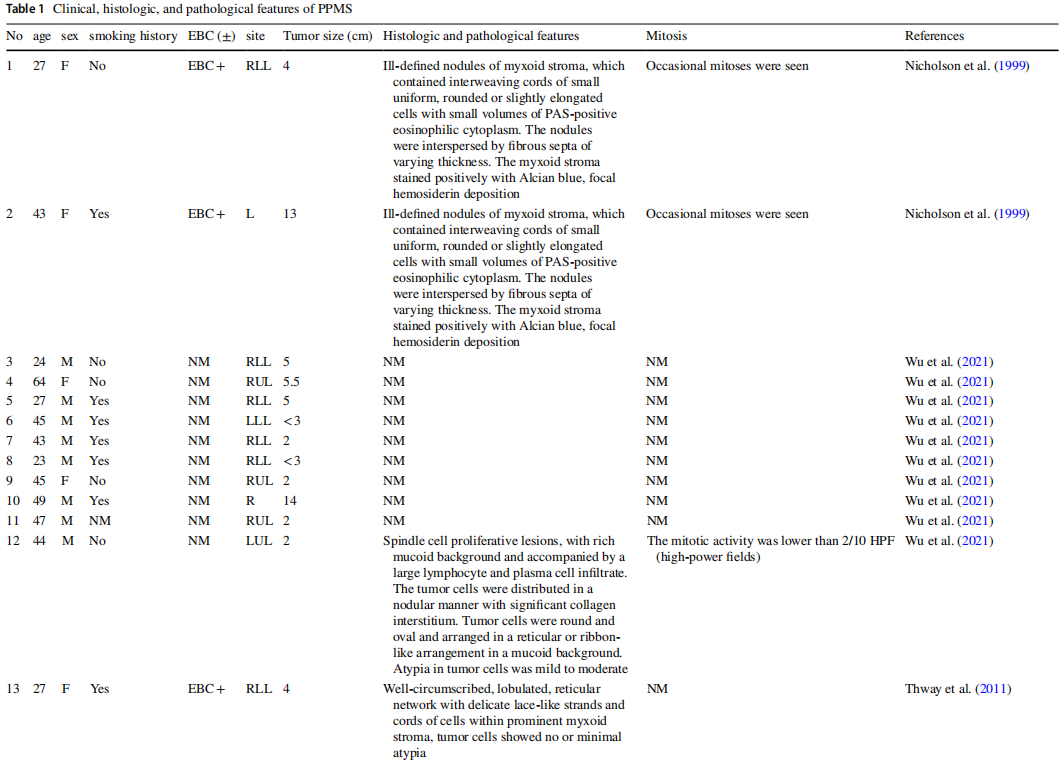





表1
二、PPMS的影像学特征与组织病理学特征
目前,CT是诊断PPMS的主要影像学检查方法,X线检查起辅助作用。然而,这种肿瘤的具体影像学特征仍有些不明确。现有的关于PPMS的文献综述和病理报告都强调了CT检查结果对于增进我们对这种疾病理解的重要性。在CT扫描图像上,PPMS常常靠近支气管,并且经常浸润肺实质。在影像学报告中观察到的大多数PPMS病例表明,原发性肺肿块主要位于右下叶(28%,11/39)和右上叶(23%,9/39)。这些肿瘤通常表现为边界清晰的实性肿块,大小在1.4厘米至14厘米之间。增强CT扫描通常显示这些病变为轻度且不均匀强化的肿块,实性和囊性成分都有强化。此外,PPMS的X线图像显示肺野有肿块阴影,可能类似胸腔积液。从大体上看,原发性肺黏液样肉瘤病变通常表现为孤立的、边界清晰的肿块,呈分叶状外观,切面苍白且有结晶状表现。具体组织病理学特征见图1。
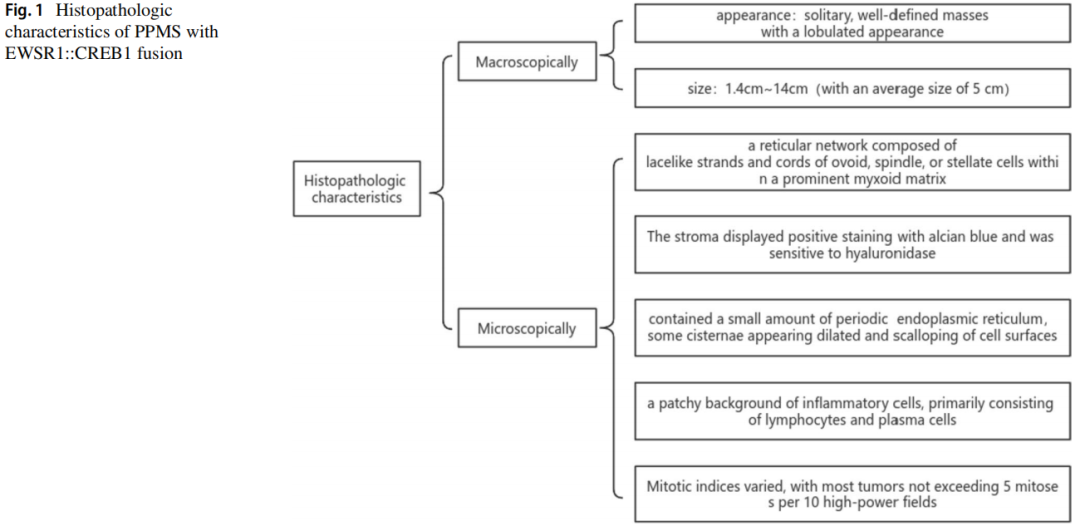
图1
三、PPMS的分子基因学与免疫组化
最近的研究证实,PPMS的关键基因特征是EWSR1基因重排以及EWSR1::CREB1融合基因的形成。这种基因变异是一个重要的诊断标志物。检测EWSR1基因重排,可以对FFPE组织样本进行荧光原位杂交(FISH)检测。这项检测显著提高了诊断的准确性。在表2中,汇总了39例PPMS病例,其中34例进行了FISH分析,结果显示EWSR1基因重排的阳性率为85%(29/34)。此外,通过针对特定融合转录本的RT-PCR可以证实EWSR1::CREB1融合的存在。EWSR1::CREB1融合常见于发生在不同部位的各种间叶性肿瘤中,表现出广泛的生物学行为。在进行了RT-PCR检测的26例病例中,EWSR1::CREB1融合的阳性率为73%(19/26)。EWSR1::CREB1融合是PPMS的一个重要特征;然而,必须注意的是,这种融合并非PPMS所特有,在其他肿瘤中也有发现,包括血管瘤样纤维组织细胞瘤(AFH)、透明细胞肉瘤、唾液腺透明细胞癌以及软组织或胃肠道透明细胞癌。此外,Nishimura等人报告了一例独特的PPMS病例,该病例存在EWSR1::ATF1基因融合。ATF1和CREB1都属于CREB家族,它们都可以与EWSR1形成融合基因。如果在发生EWSR1::CREB1易位的肺黏液样肉瘤中检测到EWSR1::ATF1融合,该肿瘤可能会被归类为“具有EWSR1::CREB易位的肺黏液样肉瘤”。
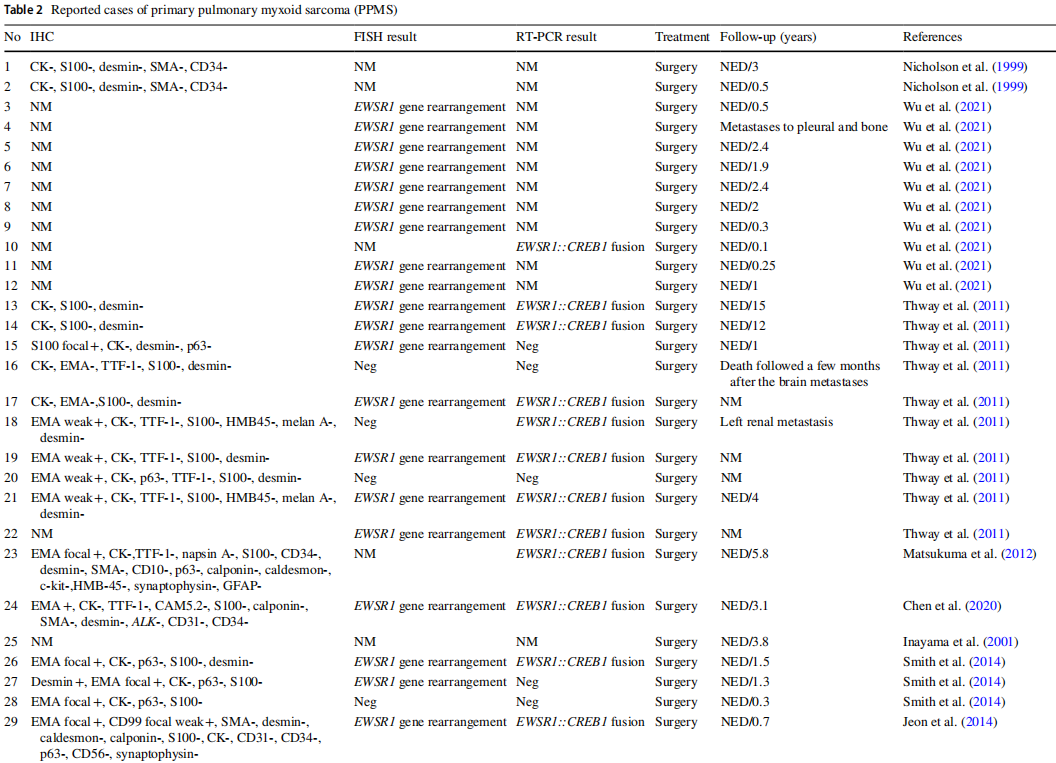
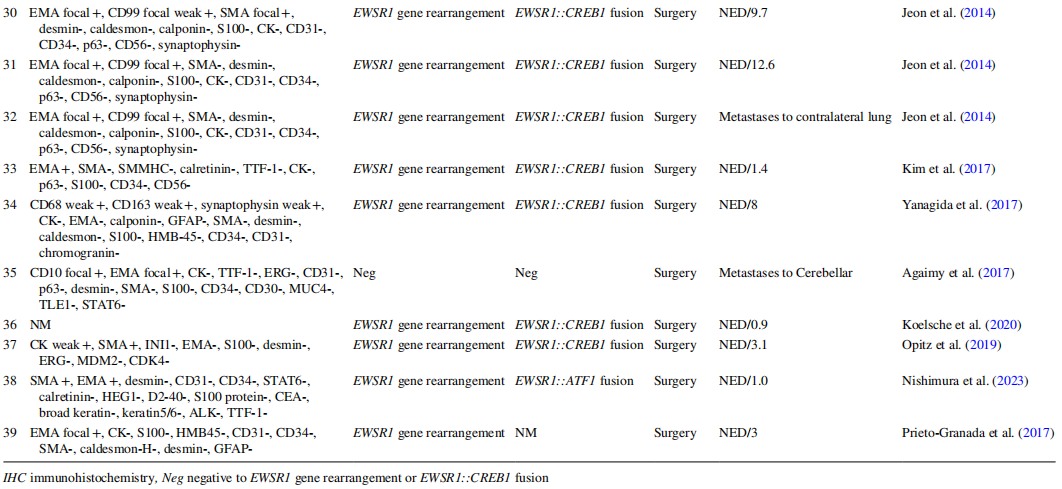
表2
PPMS缺乏高度特异性的免疫组化标志物。免疫组化分析显示,肿瘤细胞持续表达上皮膜抗原(EMA)。相反,它们对细胞角蛋白(CK)、甲状腺转录因子-1(TTF-1)、 napsin A、S-100蛋白、CAM5.2、CD10、CD31、CD34、结蛋白、平滑肌肌动蛋白(SMA)、p63、钙调蛋白、h-钙调素、间变性淋巴瘤激酶(ALK)、c-kit、黑色素细胞标志物(HMB-45)、突触素或胶质纤维酸性蛋白(GFAP)均无免疫反应。
PPMS的关键基因特征包括EWSR1基因重排和EWSR1::CREB1融合。此外,免疫组化通常显示EMA呈阳性。这些基因和免疫组化特征的结合有助于对这种肿瘤的诊断。
四、PPMS的诊断与鉴别诊断
PPMS缺乏独特的临床表现,常规血液检查和肿瘤标志物水平通常在正常范围内,这使得它很难与其他具有相似临床表现的肺部疾病相鉴别。因此,PPMS的诊断主要依赖于肿瘤的位置和组织病理学特征。病理诊断通常通过穿刺活检获得,这是临床诊断的金标准,对患者的治疗管理具有重要意义。鉴别诊断在PPMS的评估中至关重要。PPMS应与以下几种胸部肿瘤相鉴别:
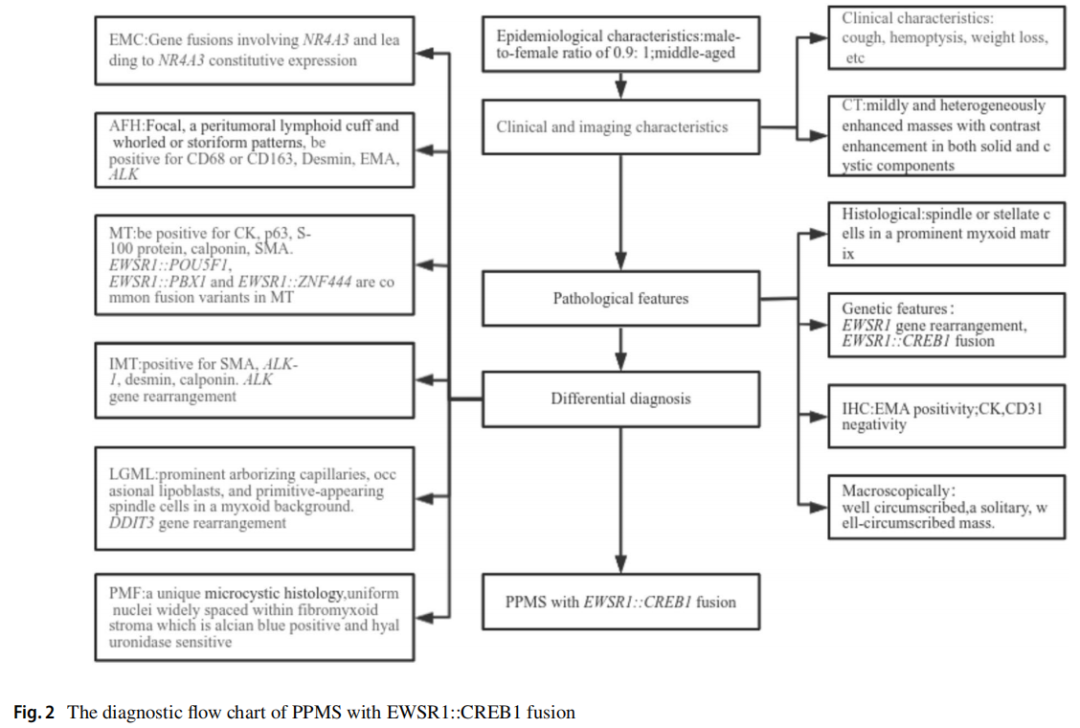
图2
骨外黏液样软骨肉瘤(EMC)
EMC是一种罕见的肿瘤,其特征是多结节生长,以及短的吻合状条索样的卵圆形至梭形细胞,这些细胞嵌入丰富的黏液样基质中。EMC具有独特的超微结构特征,细胞条索沉浸在富含糖胺聚糖的基质中。PPMS和EMC的关键鉴别因素在于它们的基因差异。从基因学角度来看,涉及NR4A3的基因融合以及由此导致的NR4A3组成型表达是EMC所特有的,被认为是这种疾病的一个标志。在EMC中鉴定出的主要融合基因是EWSR1::NR4A3和TAF15::NR4A3基因融合,而PPMS的特征是EWSR1::CREB1基因融合。
血管瘤样纤维组织细胞瘤(AFH)
AFH是一种罕见的软组织间叶性肿瘤。研究显示PPMS在软组织形态上与AFH的粘液样变体重叠。AFH的粘液样变体主要发生在软组织中,很少在肺部出现,粘液样变AFH表现出明显的黏液样特征,并且常常可以阳性表达EMA和EWSR1基因重排。因此,很难将其与PPMS区分开来。但是,肺部AFH的黏液样基质通常是局灶性的。AFH病例最常见的形态学特征包括肿瘤周围的淋巴套袖以及涡状或席纹状结构,这些特征在PPMS中通常没有描述。免疫表型差异也可作为鉴别因素;AFH常常对CD68、CD163、结蛋白、EMA和ALK呈阳性表达。相比之下,PPMS的特征是EMA阳性,而结蛋白和ALK呈阴性。此外,低至中度恶性潜能的AFH由于t(2; 22) (q33; q12) 也可能出现EWSR1::CREB1融合。虽然在AFH中可以检测到EWSR1::ATF1和FUS::ATF1融合基因,但在PPMS病例中很少发现。
有研究指出,PPMS和AFH具有相似的组织学特征、临床表现、免疫表型和分子变异,并且它们在谱系和发病机制上密切相关。然而,EWSR1阳性的PPMS和AFH是否可能代表同一种疾病的谱系,以及它们是否源自由相同或相似的EWSR1融合基因产物驱动的原始间叶细胞,仍有待进一步研究。
肌上皮肿瘤(MT)
MT具有多样的形态学特征和免疫表型。它们通常表现为多结节或分叶状生长模式,由梭形、卵圆形或上皮样细胞组成。免疫组化方面,超过44%的肌上皮肿瘤病例显示存在EWSR1基因重排,并且大多数MT病例对CK、p63、S-100蛋白、钙调蛋白和SMA呈阳性反应,而这些标志物在PPMS中呈阴性。此外,MT中常见的融合变异包括EWSR1::POU5F1、EWSR1::PBX1和EWSR1::ZNF444,而PPMS的主要融合基因是EWSR1::CREB1。
炎性肌纤维母细胞瘤(IMT)
IMT是一种独特的肿瘤,其特征是肌纤维母细胞性梭形细胞,并具有浆细胞、淋巴细胞和嗜酸性粒细胞的炎性浸润。IMT免疫组化对SMA、ALK-1、结蛋白和钙调蛋白呈阳性。大约50%至70%的IMT存在ALK基因重排,而PPMS对这些标志物呈阴性。
低级别黏液样脂肪肉瘤(LGML)
LGML是一种恶性脂肪源性肿瘤,在黏液样背景中具有明显的分支状毛细血管、偶尔可见的脂肪母细胞和原始梭形细胞。LGML常常涉及DDIT3基因重排,而PPMS中不存在这种重排。
肺微囊性纤维黏液瘤(PMF)
PMF边界清晰,具有明显的囊性改变和黏液样基质。显微镜下,PMF的特征是形态温和、间距较宽的梭形至星状肿瘤细胞,核多形性极小,且无核分裂象活性。这些形态一致的细胞核广泛分散在纤维黏液样基质中,该基质对阿利新蓝染色呈阳性,且对透明质酸酶敏感。PMF独特的微囊性组织学特征在PPMS中不存在。PMF没有诊断性的分子基因变异,并且它不会出现支气管内定位。
五、PPMS的治疗策略
目前,对于具有EWSR1::CREB1融合的PPMS的主要治疗方法是手术。鉴于PPMS的罕见性以及非特异性的临床特征,目前尚无明确的已知因素会影响其预后。
手术治疗
手术切除通常作为所有PPMS患者的主要治疗方式。术后密切监测患者以评估治疗效果和预后至关重要。PPMS是一种边界清晰的低级别恶性实性肉瘤,Ki-67指数较低,手术切除后已显示出良好的临床效果。根据现有文献,手术是大多数患者的主要治疗方法。可用的手术切除方式包括楔形切除术、肺段切除术、肺叶切除术和全肺切除术,具体取决于肿瘤的大小和分期。准确的TNM分期和分子病理分类可以指导术后的综合治疗。总之,手术治疗是PPMS患者的主要治疗手段,并且可以取得积极的治疗效果。对于不适合手术切除的患者,可以考虑药物治疗等替代治疗方法。
化疗
目前,关于PPMS化疗的数据有限,其疗效也尚不清楚,需要进一步研究。Garnier等人最初报告了一种基于阿霉素的化疗方案,用于治疗具有EWSR1::CREB1转录本融合的颅内非黏液样血管瘤样纤维组织细胞瘤,在停止治疗后,病情持续稳定了14个月。尽管PPMS与AFH都存在EWSR1::CREB1融合,但尚无报告表明阿霉素对具有EWSR1::CREB1融合的PPMS能产生显著的治疗效果。因此,对于具有EWSR1::CREB1融合的PPMS的化疗方案仍不确定。
分子靶向治疗:
虽然EWSR1基因重排和EWSR1::CREB1融合是PPMS的独特特征,但目前对这一靶点的认识仍然有限。因此,有必要研究靶向治疗在治疗PPMS方面的潜在疗效。Subbiah等人探索了使用c-Met/ALK抑制剂克唑替尼以及VEGF抑制剂帕唑帕尼治疗具有EWSR1::CREB1融合的转移性胃肠道神经外胚层肿瘤(GNET)。这两种药物在GNET中显示出持续的、近乎完全的治疗反应。此外,该研究纳入了11例具有相同EWSR1::CREB1融合的患者,包括未另行指定的肉瘤(NOS)、原发性不明的恶性肿瘤、黑色素瘤以及头颈部黏液表皮样癌。EWSR1::CREB1融合被确定为这些病例中的主要驱动因素。Subbiah等人认为,具有这种EWSR1::CREB1融合的患者也可能从克唑替尼和帕唑帕尼治疗中获益。此外, Ngo等人报告了具有EWSR1::CREB1融合和ALK过表达的转移性血管瘤样纤维组织细胞瘤对克唑替尼有持久的治疗反应。然而,克唑替尼和帕唑帕尼在具有EWSR1::CREB1融合的PPMS临床治疗中的应用尚未得到研究。这两种药物在具有EWSR1::CREB1融合的PPMS病例中的疗效仍不确定,需要更多的数据来确定它们是否适合治疗具有EWSR1::CREB1融合的PPMS。
六、PPMS的预后
根据现有的研究结果,肿瘤的临床分期、患者的整体健康状况、年龄和性别都是重要的预后因素。回顾性研究表明,大多数患者在手术后恢复良好,没有复发或转移的迹象。根据表2,PPMS手术干预后的转移率为14.7%(5/34),只有1例患者因术后脑转移死亡。在接受手术的34例患者中,85.3%(29/34)在最后一次随访时无病生存(NED)。这29例患者的NED为0.1至15年,平均NED为3.5年。然而,基于回顾性研究,没有确凿的临床证据表明术后转移与EWSR1基因重排或EWSR1::CREB1融合的存在之间存在直接联系。这些基因变异在预测PPMS预后中的作用仍然不确定,需要在未来进一步研究。
综上,具有EWSR1::CREB1融合的PPMS是一种极为罕见的低级别恶性肉瘤,通常发生在支气管和肺实质内,中年人中更为常见,且男女发病率几乎相同,临床症状相对不具特异性,主要包括咳嗽、咯血和体重减轻。显微镜下,PPMS的特征是在显著的黏液样基质中,存在由纤细的花边状条索和卵圆、梭形或星状细胞组成的网状结构。EWSR1基因重排和EWSR1::CREB1融合是PPMS的关键基因特征,也是重要的诊断标志物。免疫组化方面,PPMS的EMA呈阳性。在治疗方面,近年来手术一直是主要的治疗方法。因此,放疗、化疗和免疫靶向治疗等其他治疗方法的疗效仍需进一步研究。
除了上述提到的骨与软组织肿瘤DNA272+RNA1560基因检测,我司的骨与软组织肿瘤DNA1308+RNA1560基因检测、骨与软组织肿瘤DNA160+RNA1560基因检测以及实体瘤1560基因融合RNA检测,均包括了EWSR1基因的全部转录组,辅助肺黏液样肉瘤的诊断。
参考文献:
Miao X, Chen J, Yang L, Lu H. Primary pulmonary myxoid sarcoma with EWSR1::CREB1 fusion: a literature review. J Cancer Res Clin Oncol. 2024 Feb 29;150(3):108. doi: 10.1007/s00432-024-05634-4. PMID: 38421462; PMCID: PMC10904531.

猜你喜欢
- Clinical Nutrition: 老年住院患者营养不良风险较高与肌肉内脂肪组织增加有关
- 西藏娃失联36小时后现身陡峭山顶 村民称在牧场看到三只豹子
- 男性阳痿治疗方法哪些最有效 男性阳痿治疗的中医针灸疗法
- EANM 2024 | 中国之声:北京协和医学院揭示[68Ga]Ga-FAPI-04 PET/CT能更精准反映肺纤维化活动状态
- 天呐!减肥还能引起脱发?该怎么应对?
- 菜花焖羊肉的做法-咸鲜味炒菜谱
- 【NEJM】张磊教授团队使用达雷妥尤单抗治疗儿童复发难治ITP安全有效
- 不吃主食就能减肥 事实并不是这样!
- 如何正确做瑜伽 这些瑜伽动作教你拥有苗条身材
- 瘦腿的最快方法有哪些?推荐30秒瘦腿操打造修长美腿
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)