首页 > 医疗资讯/ 正文

动脉止血材料需在含血环境中同时满足两大关键性能:快速形成强效湿界面粘附和高内聚力,以承受80-120 mmHg的动脉压力。然而,现有动脉止血材料依然面临双重挑战:一方面,血管外表面血液形成的水合层阻碍材料-组织有效接触,削弱界面粘附;另一方面,低模量(柔软)材料虽有利于界面结合,却难以提供足够的机械强度来抵抗动脉高压。因此,开发兼具高效移除水合层能力和内聚自增强特性的新型动脉止血材料迫在眉睫。
近日,吉林大学超分子结构与材料全国重点实验室李文课题组联合吉林大学第二医院赵建武课题组创新性地构建了一种基于天然玉米蛋白(zein)和聚赖氨酸(PLL)的蛋白质粉末型止血材料。该材料通过十二烷基硫酸钠(SDS)改性的玉米蛋白胶体与聚赖氨酸链与聚赖氨酸静电交联、凝聚而成,具有以下突出特性:1. 优异的储存稳定性:脱水状态下可研磨成粉末便于长期保存;2. 快速水合响应:遇水后借助PLL氨基及SDS硫酸基的强水合能力,实现刚性粉末向柔性胶粘剂的快速转变;3. 自增强效应:吸水成胶的过程中存在未完全水合的粉末颗粒,这些刚性的粉末颗粒充当物理填料显著提升胶粘剂的内聚力。实验证实,该材料在含水、含血液或其他湿润界面可快速移除界面水,转变为水性胶粘剂,并表现出卓越性能:
• 爆破压力达118.2-129.4 mmHg,超越人体正常收缩压范围
-
优异的生物相容性和可降解性
• 在大鼠、大耳兔及香猪等多物种模型中均展现快速、可靠的动脉止血效果
这一研究进一步揭示了粉末遇水粘附性自增强的作用机制主要包括界面水排除和本体结构异质性。该蛋白粉末的快速界面水移除能力源于离子复合物的高水合性及水合诱导的自主凝胶化。本体结构异质性则来自未完全水合的粉末颗粒—作为刚性填料与水合的凝胶形成物理交联的网络结构,进而提升了材料的交联密度和内聚力。该研究提出的“本体结构异质性增强内聚力”策略为新一代止血材料设计提供了新的重要思路。
1.蛋白粉末胶的制备工艺:
疏水玉米蛋白在超声辅助下可均匀分散于十二烷基硫酸钠(SDS)水溶液中形成稳定的zein/SDS复合胶体。胶体表面丰富的负电性硫酸基可进一步与水溶性阳离子聚赖氨酸通过多重静电及氢键相互交联,形成宏观可见的水下胶粘剂(zein/SDS-PLL胶粘剂)。胶粘剂经过干燥、研磨处理即可获得zein/SDS-PLL粉末,该粉末能快速吸收水,转化为具有粘性增强的凝胶状胶粘剂。
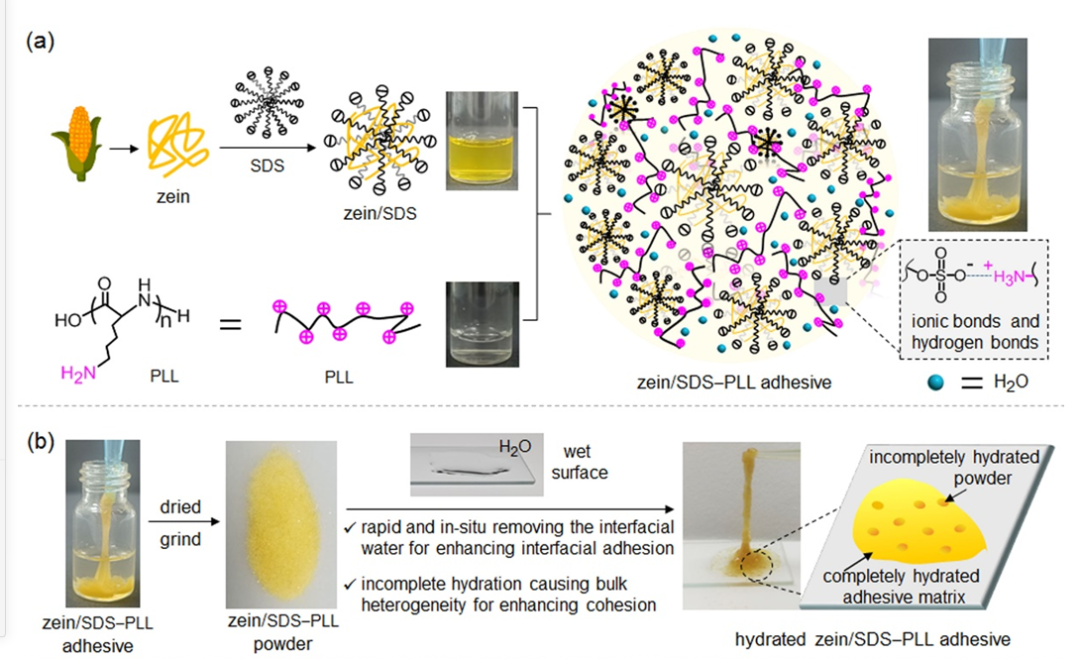
图1.(a)溶液法制备zein/SDS-PLL水性胶粘剂的模型图,(b)蛋白胶粘剂脱水、研磨成粉末后重新吸水成胶的光学照片及内部结构示意图。
2.zein/SDS-PLL粉末吸水增强粘附强度的原理:
粉末吸水后的胶粘剂对于钛(Ti)、不锈钢(SS)、聚醚醚酮(PEEK)、聚丙烯(PP)和猪皮的水下剪切强度分别为120.7±2.9、98.2±2.2、65.4±2.3、55.3±2.5和40.5 (5.1 kPa),较溶液法制备的zein/SDS-PLL水下胶粘剂提升2-3倍。既往研究表明,水接触型粘附增强主要遵循界面水排除机制,然而,本研究中水合态zein/SDS-PLL粉末胶粘剂的剪切粘附失效模式呈现双重特征:在PEEK和PP表面表现为界面剥离,而在钛合金(Ti)和不锈钢(SS)表面则呈现本体断裂。这一差异表明该胶粘剂的粘附增强效应不仅源于传统的水排除机制,更与材料内部结构重构密切相关。光学显微镜观察显示水合后的粉末胶粘剂呈现出非均相结构,随着水合时间延长,这些异质区域的尺寸逐渐减小。通过向湿法制备的zein/SDS-PLL胶粘剂基质中掺入了刚性SiO2颗粒(50-70 μm)进行对照进一步证实了这一观点,随着SiO2加入量增加,存储模量明显增加。
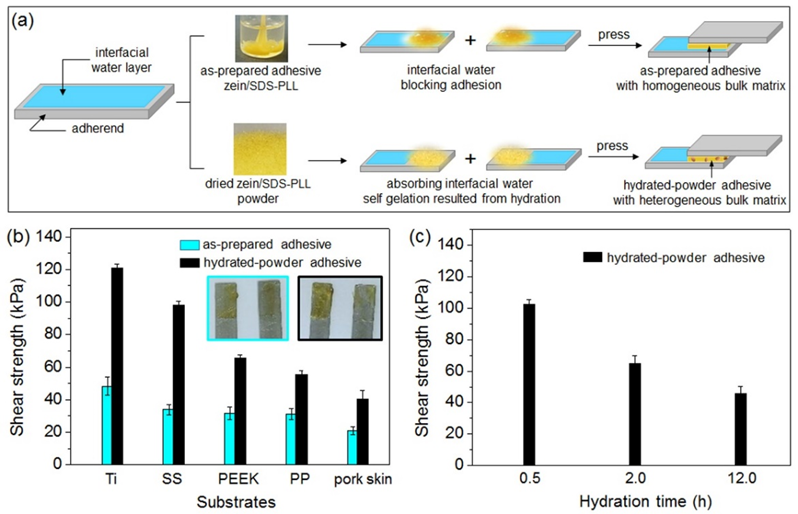
图2. (a)溶液法制备的zein/SDS-PLL水性胶粘剂及蛋白粉末吸水粘接实验的模型示意图, (b)溶液法制备的zein/SDS-PLL水性胶粘剂及蛋白粉末吸水后对不同基底的水下搭接剪切强度,(c)蛋白粉末在不同水合时间段的搭接剪切强度
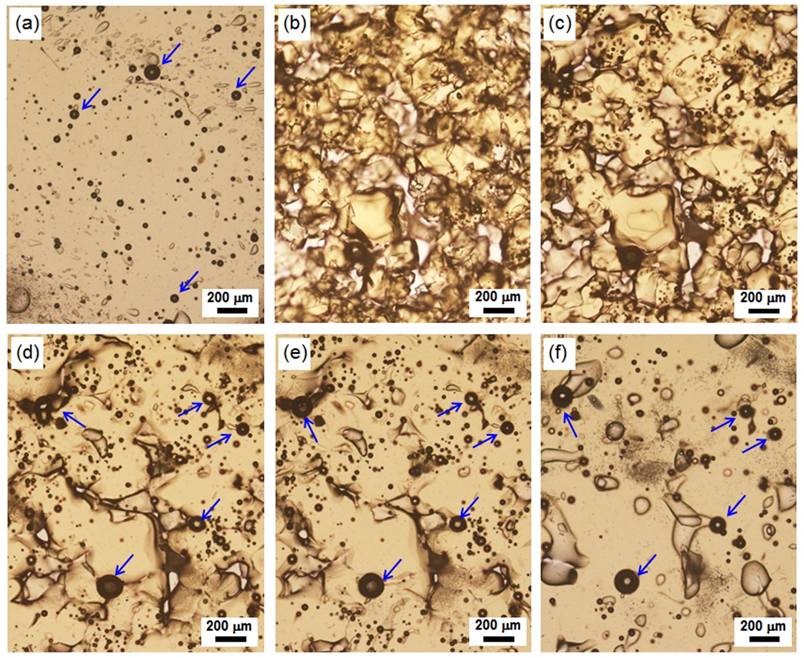
图3. zein/SDS-PLL光学显微镜图:(a)溶液湿法制备的蛋白水性胶粘剂,(b-g)脱水后的蛋白粉末重新遇水后随水合时间的结构变化。
3.动脉止血:
该水合态胶粘剂展现出优异的生物相容性、血液相容性、生物降解性和抗压性能(爆破压:118.2-129.4 mmHg)。将所得蛋白粉末分别应用到兔腹主动脉损伤模型、猪颈动脉穿刺模型、大鼠股动脉穿刺模型,通过失血量、血流量和止血时间等参数表明该粉末胶粘剂是一种可靠的动脉止血剂。
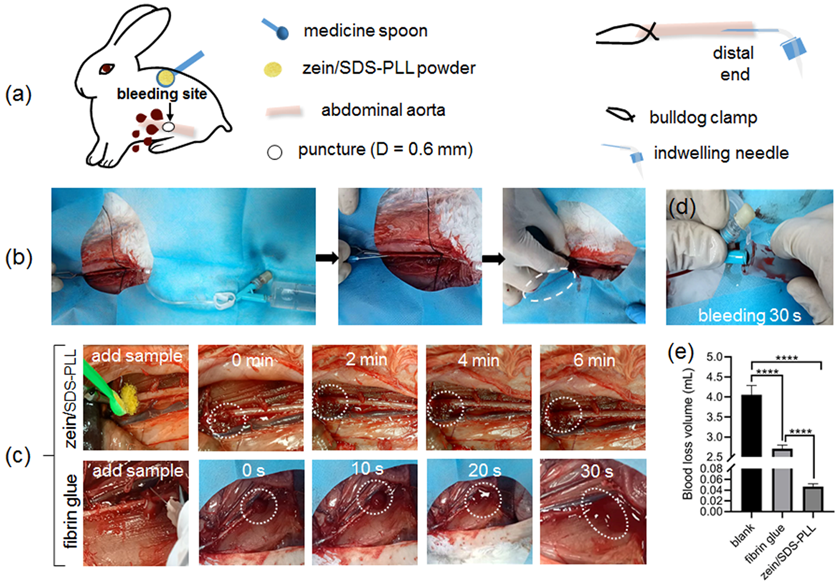
图4. zein/SDS-PLL水合态粉末胶对兔腹主动脉的止血实验:(a)大耳兔止血模型示意图,(b)失血量测试实验,(c)腹主动脉止血光学照片,(d)粉末胶封堵止血后血管的流畅性评价,(e)动脉止血模型的失血量统计分析结果
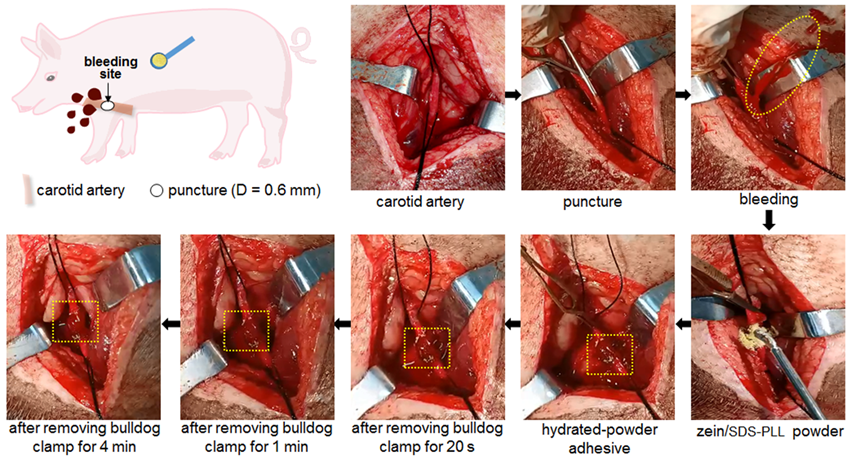
图5. zein/SDS-PLL水合态粉末胶对猪颈动脉的止血实验
4.止血机制:
定性和定量的红细胞/血小板粘附实验表明,该胶粘剂对红细胞/血小板的粘附率远高于市售的纤维蛋白胶;同时,ITC实验表明过量的PLL的质子化胺基与血小板之间的静电吸引是实现止血的另一因素。因此,作者提出zein/SDS-PLL粉末的快速止血作用涉及“物理封堵-生物激活”的双重机制:1) zein/SDS-PLL粉末与血液接触时,原位形成的胶粘剂剂起到物理屏障作用,实现快速有效止血;2) zein/SDS-PLL胶粘剂中阳离子PLL与血小板发生静电吸引,加速血小板和红细胞的粘附和聚集,促进止血。
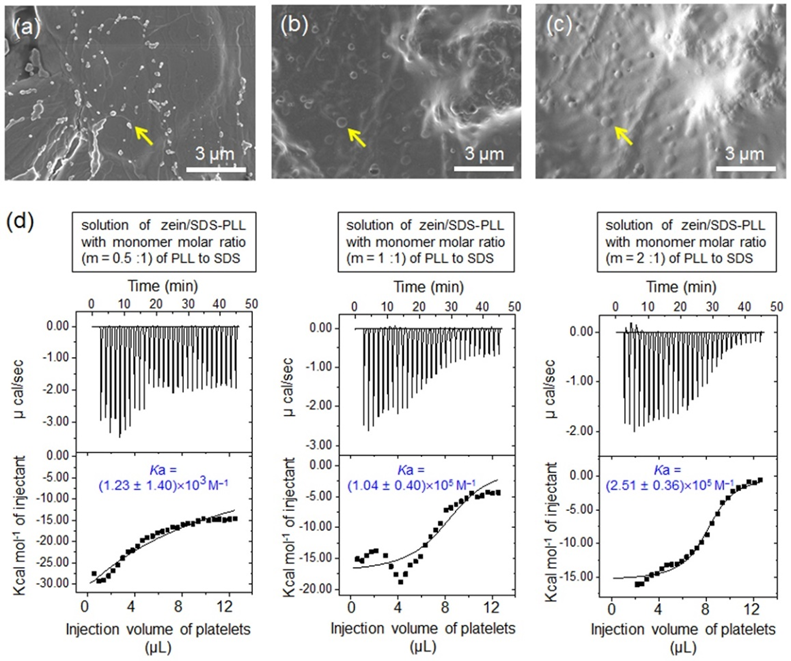
图6. zein/SDS-PLL胶粘剂对红细胞/血小板的粘附实验(a-c)及zein/SDS-PLL胶粘剂与血小板结合的ITC曲线图(d)
总之,本文通过简单、绿色的超分子交联、凝聚策略,创造性的将天然可再生玉米蛋白开发成一类性能优异的动脉止血材料。脱水后的蛋白粉末中极性离子基的超强水合能力赋予其快速吸水成胶的特性。该粉末材料基于双重协同机制实现快速水触发凝胶化与强效粘附:1)界面脱水机制;2)本体结构异质性强化内聚力机制。其中“本体结构异质性增强内聚机制”进一步拓展了粉状胶粘剂水接触粘附增强效应的认知边界。该蛋白粉末具有优异的生物相容性和可降解性,在动脉快速止血及不可压迫性止血中具有重要应用价值。
参考文献:
Nie, J.; Sun, Y.; Zhang, S.; Wen, G.; Li, T.; Zhao, J.; Li, W., Dynamic hydration driven adhesiveness self-reinforcement of powdery protein for rapid artery hemostasis. Biomaterials, 2025, 321, 123328.
原文链接:
https://www.sciencedirect.com/unsupported_browser
猜你喜欢
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)