首页 > 医疗资讯/ 正文
炎性乳腺癌(IBC)是一种预后极差的特殊类型乳腺癌,IBC的发生及快速恶性进展原因及机制尚未被阐明。
2024年6月4日,中山大学附属第一医院、广东省中医院、中山大学附属肿瘤医院、江门市中心医院、广东省妇幼保健院、揭阳市人民医院和丹娜法伯癌症研究所共同合作在Cancer Research 上发表了题为“A Subpopulation of Luminal Progenitors Secretes Pleiotrophin to Promote Angiogenesis and Metastasis in Inflammatory Breast Cancer”的研究论文,首次从单细胞角度描绘了IBC肿瘤和红肿皮肤的微环境组成,揭示了管腔祖细胞通过PTN-NRP1轴促进血管生成和转移的机制,为IBC的治疗提供潜在靶点和研究新见解。

IBC的诊断依据其临床表现,即特殊的水肿和红斑样皮肤改变。目前其治疗参考非炎性乳腺癌(non-IBC)的治疗策略,但IBC对治疗的反应较差。既往研究通过分析IBC肿瘤的基因组和转录组数据以探讨其分子特征,但未能找到IBC发生发展的关键分子机制和特殊治疗靶点。因此,需要全面剖析IBC的肿瘤微环境以探索新的靶点。
研究人员对初治的17例IBC和5例non-IBC的肿瘤和皮肤样本进行了单细胞转录组、普通转录组和全外显子测序,结果发现,IBC中特异性存在一簇高表达多效生长因子(PTN)的管腔祖细胞。同时IBC中血管生成表型的尖端型内皮细胞(tip cells)显著增多。进一步应用细胞互作分析、多色免疫荧光和细胞实验证实管腔祖细胞通过分泌PTN与内皮细胞上的NRP1受体相互作用促进血管生成,并且这一过程不依赖VEGFA/VEGFR信号轴。既往临床试验证实IBC患者未能从抗VEGFA治疗中获益。以上证据提示PTN-NRP1轴是促进IBC血管生成的关键信号轴。此外,研究还发现伴随血管生成,IBC红肿皮肤中富集的未成熟表型的血管旁细胞(PVL)可能通过重塑IBC红肿皮肤微环境促进肿瘤转移。
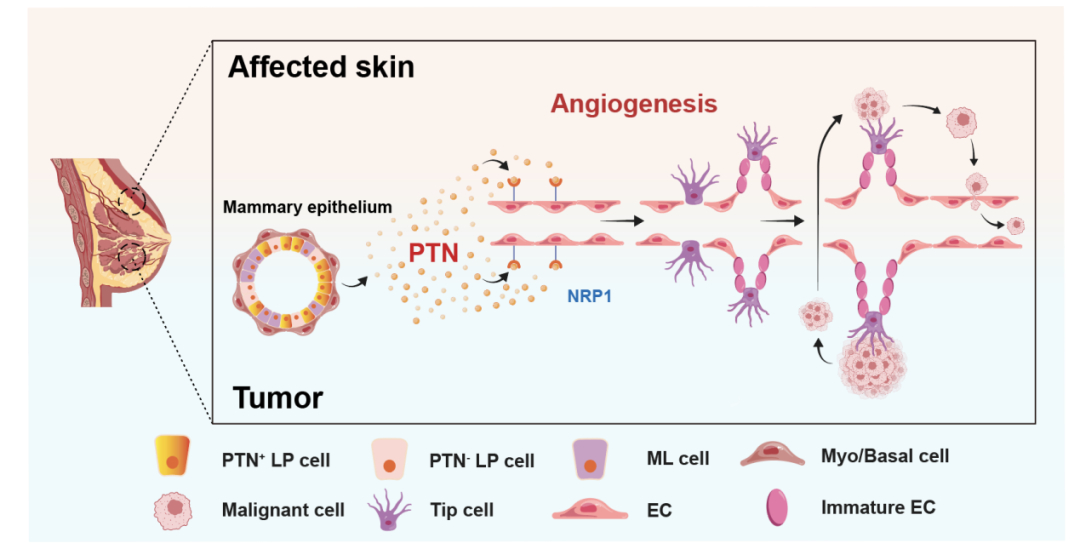
图注:PTN+管腔祖细胞通过分泌PTN与内皮细胞上NRP1受体结合,诱导尖端型内皮细胞形成,进而促进血管生成及肿瘤转移。
综上,该研究首次提出IBC乳腺实质改变的科学假说,即PTN-NRP1轴是诱导IBC血管生成的关键信号轴;首次阐述IBC红肿皮肤中未成熟表型PVL细胞亚群促肿瘤转移的重要作用。为研究IBC的发病和进展提供了全面且深入的理论依据,为IBC的治疗提供了潜在靶点。
中山大学附属第一医院乳腺疾病诊疗中心张萌萌博士是该论文的第一作者,周铠文硕士、王梓林博士和刘婷博士是共同第一作者,乳腺疾病诊疗中心林颖主任医师是最后通讯作者,乳腺疾病诊疗中心邵楠副主任医师和精准研究院郭剑平研究员是共同通讯作者。
原文链接:
https://aacrjournals.org/cancerres/article/84/11/1781/745517/A-Subpopulation-of-Luminal-Progenitors-Secretes
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)