首页 > 医疗资讯/ 正文
微卫星稳定(MSS)结直肠癌(CRC)被称为"冷肿瘤",因为对抗PD-1抗体几乎无应答。最近的一项REGONIVO试验表明,瑞戈非尼联合纳武利尤单抗对MSS转移性CRC(mCRC)具有令人鼓舞的疗效。然而,只有一小部分患者可能从联合治疗中获益。本研究旨在评估免疫检查点抑制剂联合瑞戈非尼治疗难治性MSS mCRC的疗效和安全性数据,并发现可有效分层获益患者人群的生物标志物。研究者回顾性分析接受瑞戈非尼联合抗PD-1抗体治疗的MSS mCRC患者。回顾和评估客观缓解率(ORR)、疾病控制率(DCR)、无进展生存期(PFS)、总生存期(OS)及基因突变情况。
21例患者接受联合治疗。中位治疗持续时间为4个月时,最佳反应为完全缓解(CR)1例,部分缓解(PR)3例,疾病稳定(SD)2例。总体人群的ORR和DCR分别为19%和28.5%。中位PFS为4个月,中位OS为25个月。只有erbb2受体酪氨酸激酶2/erbb3受体酪氨酸激酶3(ERBB2/ERBB3)突变状态被证实是有效治疗的潜在预测因素。ERBB2/ERBB3突变患者的ORR、DCR和PFS均较野生型患者显著改善。3例患者(14.3%)发生了3级或更高级别的治疗相关不良事件。瑞戈非尼联合PD-1抑制剂为难治性MSS mCRC提供了一种可行的治疗方案,且不良反应可耐受。ERBB2/ERBB3突变患者可能是该联合方案的首选人群。
研究背景
免疫检查点抑制剂(ICIs),包括抗程序性死亡受体1(PD-1)和抗程序性死亡配体1(PD-L1),已在具有错配修复缺陷(dMMR)或高微卫星不稳定性(MSI-H)的mCRC中显示出显著疗效,这些肿瘤的特征是高肿瘤突变负荷和肿瘤浸润淋巴细胞富集。然而,MSI-H/dMMR癌症仅占全部mCRC病例的2%-4%。大多数CRC患者表现出MSS或错配修复正常(pMMR)状态,被称为“冷肿瘤”,具有较少的致癌基因突变和较少的炎症肿瘤免疫微环境。在肿瘤微环境中免疫细胞的募集和活化不足被认为是免疫检查点抑制剂在MSS mCRC无效的根本机制。在MSS患者中,增强肿瘤微环境的免疫原性和开发ICIs获益性的联合策略是迫切需要的。
瑞戈非尼是一种小分子酪氨酸激酶抑制剂,已被批准用于治疗化疗难治性mCRC。同时,临床前研究表明,瑞戈非尼还可以(a)抑制免疫抑制性细胞浸润,(b)抑制免疫抑制分子的表达,(c)诱导肿瘤相关巨噬细胞(TAMs)重编程为M1表型,这恢复了免疫抑制的肿瘤微环境,协同增强了ICIs的疗效。一项Ib期研究(REGONIVO)报告了瑞戈非尼联合纳武利尤单抗在24例难治性MSS mCRC患者中的疗效,ORR为33%,中位PFS延长超过6个月。最近另一项瑞戈非尼联合特瑞普利单抗的Ib/II期研究显示,在33例mCRC患者中,ORR较低,为15.2%。这些研究表明,一部分患者可能从联合治疗中获益。进一步确定mCRC患者的获益亚群仍然是一个引人注目的临床挑战。
2020年,研究者出于同情治疗,使用瑞戈非尼+纳武利尤单抗方案治疗了1例有广泛肝和肾盂转移的难治性mCRC患者。患者肿瘤基因型为MSS,肿瘤突变负荷(TMB)低,但治疗8个月后病灶完全消退,达到完全缓解(CR)。至今已维持28个月,未见复发和转移。研究者对患者的肿瘤样本进行了第二代测序(NGS),并在ERBB3中同时发现了G284R突变和扩增。临床前研究表明,ERBB2/ERBB3突变可促进胆囊癌中PD-L1介导的免疫逃逸。由于二聚体HER2/HER3分别由ERBB2和ERBB3表达,是酪氨酸激酶瑞戈非尼的靶点,研究者推测瑞戈非尼可能逆转具有免疫抑制作用的肿瘤微环境,并协同增强具有ERBB2/ERBB3突变或扩增患者的ICIs疗效。
ICIs联合瑞戈非尼可能是MSS mCRC患者,尤其是ERBB2/ERBB3突变患者的一种有前景的治疗策略。为了阐明这些问题,研究者进行了这项回顾性研究,以评估瑞戈非尼联合ICIs在真实世界中对伴或不伴ERBB2/ERBB3突变的MSS mCRC患者的疗效和安全性,探讨ERBB2/ERBB3突变对联合治疗方案疗效的影响。
研究方法
研究者回顾性分析2018年11月至2023年4月在上海交通大学医学院附属新华医院接受瑞戈非尼联合抗PD-1抗体治疗的MSS mCRC患者。根据医师决定确定不同类型抗PD-1抗体的使用情况,包括纳武利尤单抗、特瑞普利单抗、斯鲁利单抗和信迪利单抗。纳入标准包括MSS mCRC患者在标准治疗(包括氟尿嘧啶、奥沙利铂和亚叶酸钙[FOLFOX]以及氟尿嘧啶、伊立替康和亚叶酸钙[FOLFIRI])发生疾病进展后,出于同情目的接受瑞戈非尼和抗PD-1抗体联合治疗作为三线或更多线治疗。既往接受过瑞戈非尼单药治疗的患者也被纳入研究。排除标准包括:(a)治疗少于2个周期的患者,(b)关于肿瘤缓解的信息很少的患者,(c)确认MSI-H/dMMR状态的患者。患者口服瑞戈非尼80-120 mg,1次/天,持续21天,每28 天为1个周期。为了控制与治疗相关的毒性,将一些患者的剂量降低至最低剂量80 mg。PD-1抑制剂(纳武利尤单抗,每2周3 mg/kg;特瑞普利单抗,每2周3 mg/kg;斯鲁利单抗,每2周3 mg/kg;信迪利单抗,每3周200 mg)在口服瑞戈非尼第1天静脉给药。
研究结果
患者基线特征:
共有21例MSS状态的mCRC患者符合研究标准并被纳入本研究[男性15例(71.4%);中位年龄52(范围:32-73)](表1)。东部肿瘤协作组体能状态评分(ECOG PS)为1分的患者占71.4%,28.6%的患者ECOG PS为0分。10名患者(47.6%)同时发生转移。左侧原发性结直肠癌16例(76.2%),右侧原发性结直肠癌5例(23.8%)。最常见的转移部位为肝(66.7%)、肺(33.3%)、腹膜(28.6%)和淋巴结(19%)。所有患者既往均接受过≥3线化疗,包括95.2%的患者接受过抗血管内皮生长因子(VEGF)治疗。9例(42.9%)患者既往接受过瑞戈非尼治疗,均在联合治疗前出现疾病进展。21例(100%)患者确认了MSS/pMMR状态。8例(38.1%)患者存在KRAS或NRAS突变状态,3例(14.3%)患者存在BRAF V600E突变。5例(23.8%)患者存在ERBB2/ERBB3突变或扩增状态(2例为ERBB2突变,2例为ERBB2扩增,1例为ERBB3突变和扩增同时存在),16例(76.2%)为野生型。抗PD-1抗体类型包括纳武利尤单抗(61.9%)、特瑞普利单抗(19%)、斯鲁利单抗(9.5%)和信迪利单抗(9.5%)。其中特瑞普利单抗、斯鲁利单抗和信迪利单抗为中国国产ICIs。
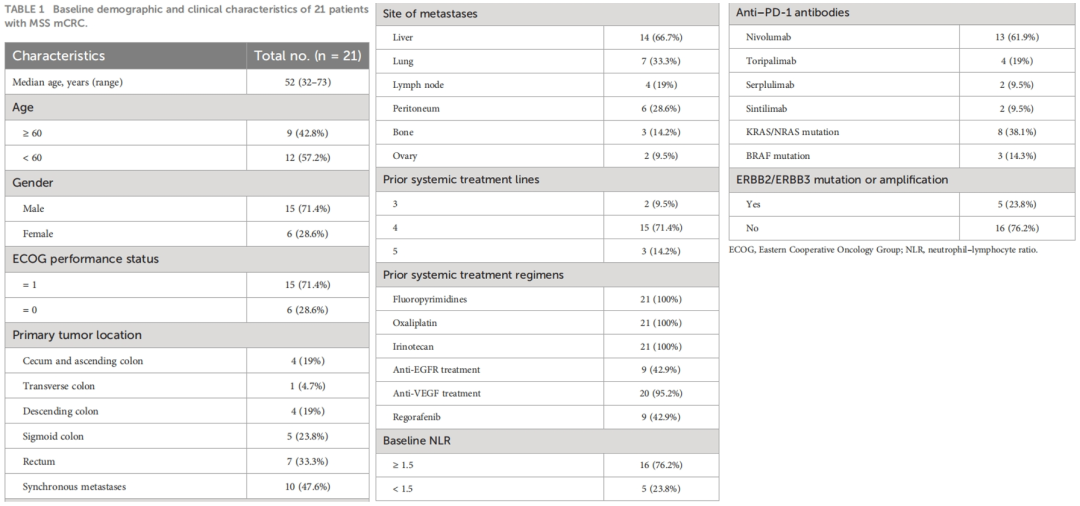
表1
疗效:
中位治疗持续时间为4个月(范围:2-28个月)。最佳反应为1例患者(4.8%)获得CR,3例患者(14.3%)获得PR,2例患者(9.5%)获得SD(表2;图1A、B)。在总体人群中,ORR和DCR分别为19%(4/21)和28.5%(6/21)。3例患者在分析时仍处于缓解状态,其中1例患者已达28个月CR。21例患者均可评估PFS和OS。中位PFS为4个月(95%CI,3.3-4.6)(表2;图1C),中位OS为25个月(95%CI,13.3-36.6)(表2;图1D)。
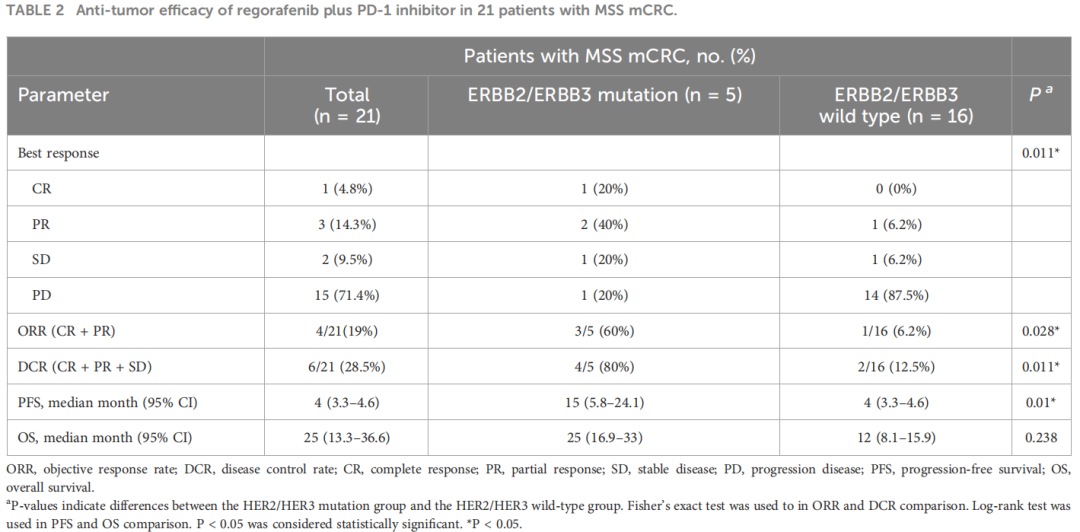
表2
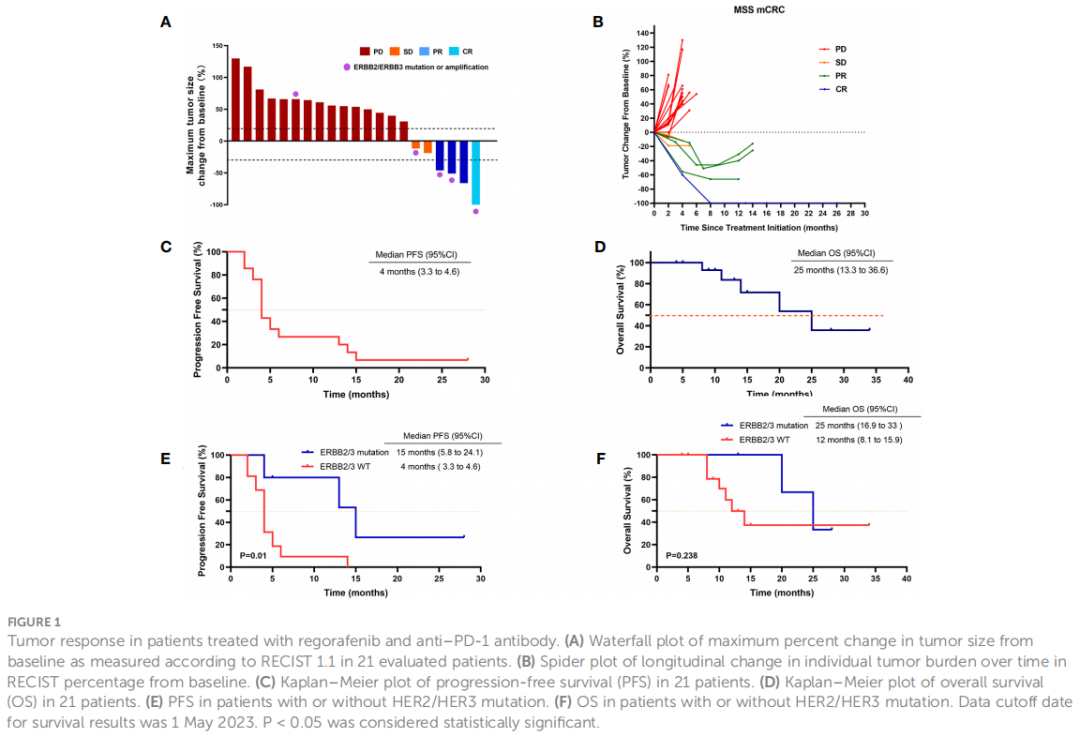
图1
预测因素的亚组分析:
研究者还进行了单变量分析来评估临床病理因素对DCR的预测价值,包括年龄(≥60vs.< 60)、ECOG(1 vs.0)、原发肿瘤部位(左结直肠 vs.右结肠)、同步转移(是 vs.否)、肝转移(有 vs.无)、既往瑞戈非尼治疗(是 vs.否)、基线中性粒细胞-淋巴细胞比率(NLR)(≥1.5 vs.<1.5)、KRAS状态(野生型 vs.突变)、BRAF状态(野生型 vs.突变)和ERBB2/ERBB3状态(野生型 vs.突变)(表3)。只有ERBB2/ERBB3突变状态被证实是一个潜在的预测因素,并与疾病控制风险增加相关[OR,28(95%CI,1.9-394.4);p=0014]。在对ECOG PS、RAS突变状态、BRAF突变状态和肝转移进行校正后,ERBB2/ERBB3突变的疾病控制风险增加仍然显著[校正后的比值比(aOR),54.8(95%CI,1.2-2497.3);p=0.04]。

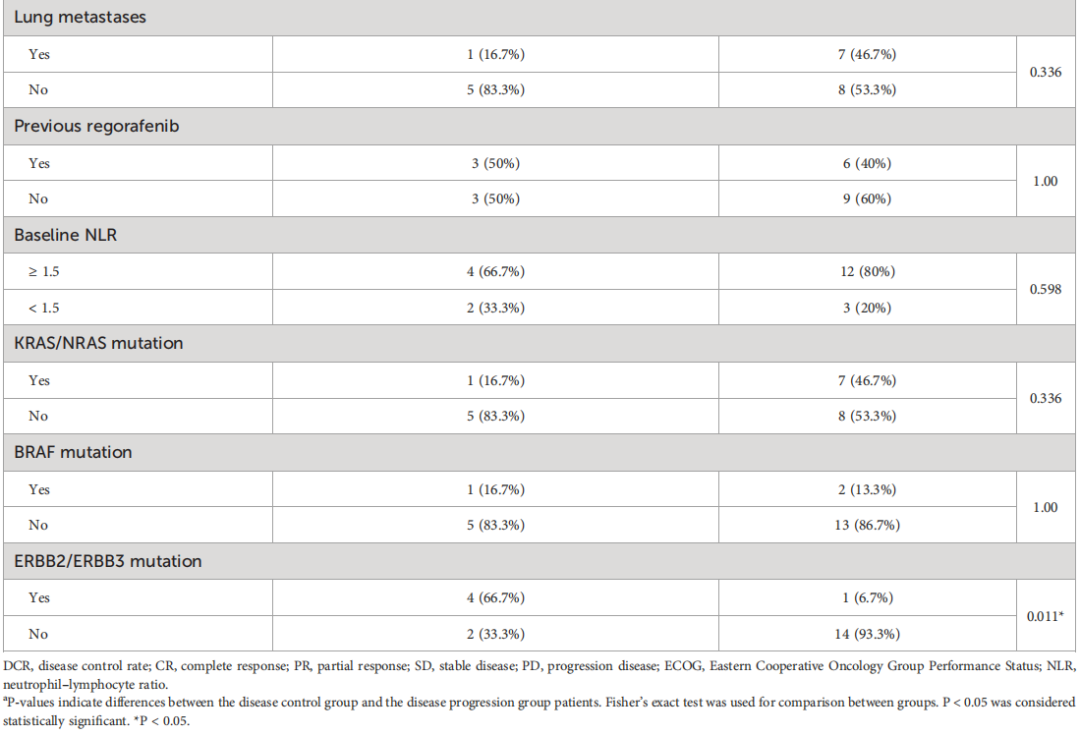
表3
此外,ERBB2/ERBB3突变患者的ORR和DCR(分别为60%和80%)显着高于野生型患者(分别为6.2%和12.5%)(表2)。ERBB2/ERBB3突变患者的中位PFS为15个月,野生型患者为4个月(p=0.01)(表2;图1E)。然而,两组间的OS没有显著差异(p=0.238)(表2;图1F)。
安全性:
联合治疗的耐受性良好,治疗期间未记录到4级或以上的毒性(表4)。在21例患者中,76%的患者发生了1-2级TRAE(治疗相关不良事件),14.3%的患者发生了3级TRAE。最常见的1-2级TEAE(治疗期间不良事件)包括高血压(28.5%)、食欲下降(28.5%)、乏力(19%)、腹泻(19%)、转氨酶升高(19%)和手足皮肤反应(14.2%)。2例患者(9.5%)出现3级转氨酶升高,1例患者(4.7%)出现3级心肌酶升高。
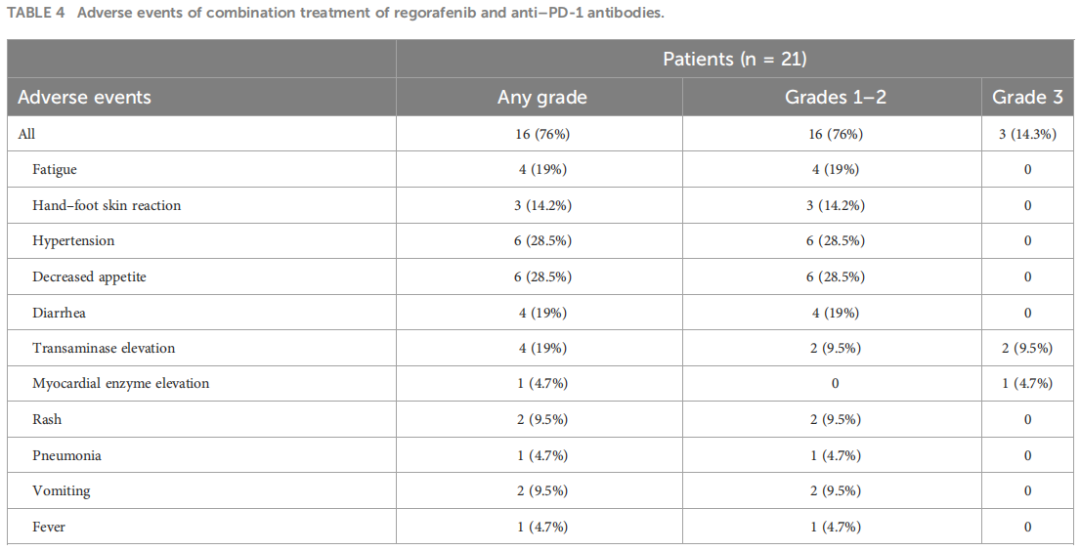
表4
一例完全缓解病例报告:
研究者在这里报告了一名32岁的女性患者,在三线治疗进展后被诊断为难治性转移性结肠癌,预期生存时间很短。2019年11月患者首次诊断乙状结肠癌,伴肝脏和盆腔多发转移和出血性腹水。患者因不完全性肠梗阻于2019年11月11日行结肠切除术,未行转移灶切除术。术后病理诊断为腺癌(pT4N2cM1),KRAS/NRAS/BRAF均为野生型,MSS状态。不幸的是,分别接受mFOLFOX6加西妥昔单抗和FOLFIRI加贝伐珠单抗治疗5个周期后,患者发现疾病持续进展,癌胚抗原(CEA)增加(从230 ng/mL增加到398 ng/mL)、CA199增加(从570 U/mL增加到9,620 U/mL)和肝转移病灶大小增加(图2、3)。瑞戈非尼[120 mg每日(dq)]单药作为三线治疗3个周期后,CEA(从398 ng/mL降至294 ng/mL)和CA199(从9,620 U/mL降至8,210 U/mL)略有下降(图2)。然而,2020年12月CT扫描显示肝脏严重疾病进展(图3)。
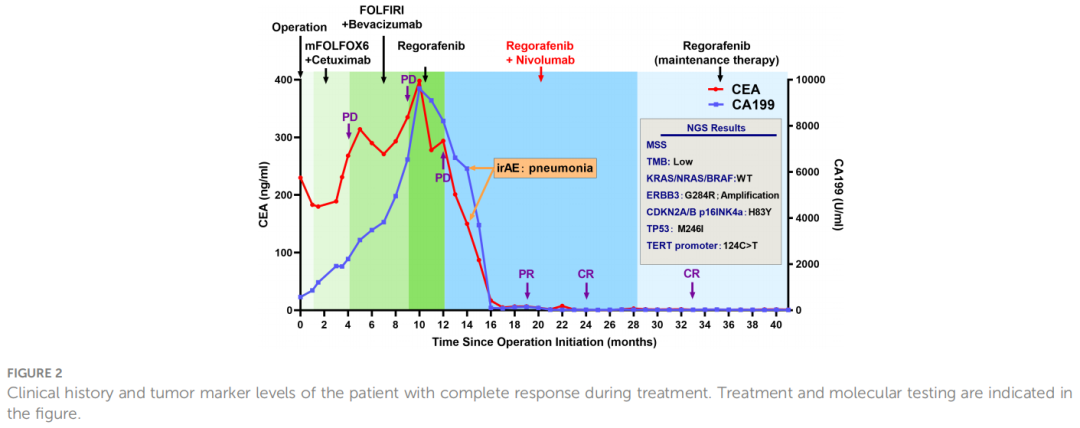
图2
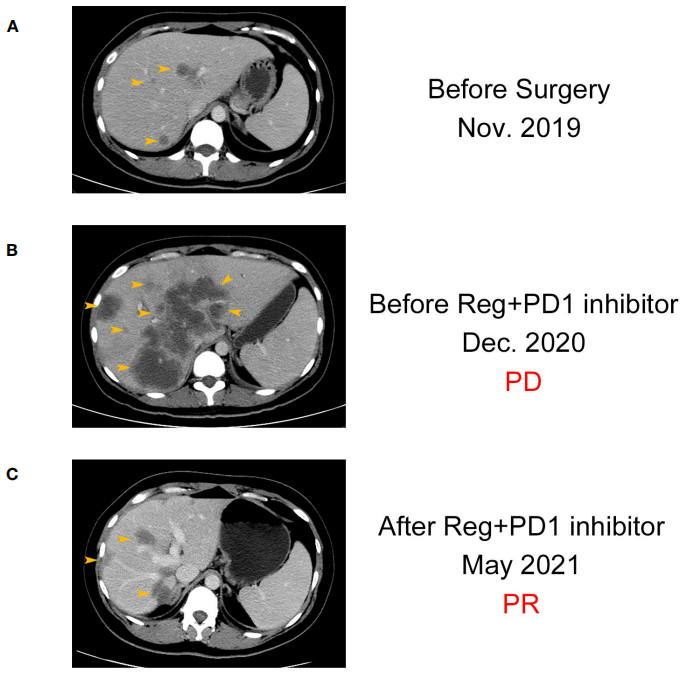
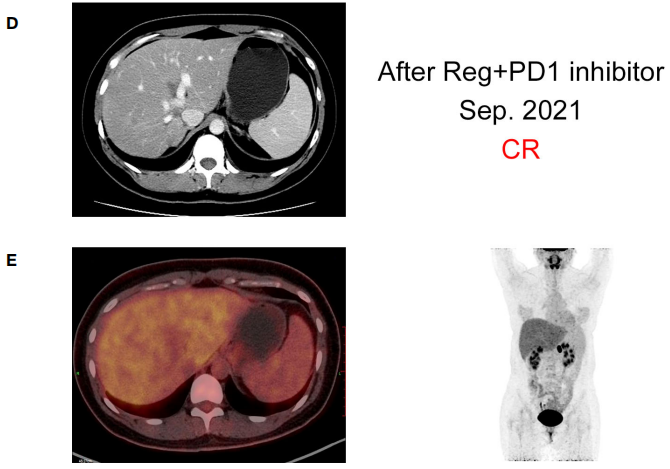

图3
出于同情目的,患者从2020年12月开始接受纳武利尤单抗[每2周200 mg(q2w)]联合瑞戈非尼(120 mg qd)治疗(图2)。然而,在联合治疗2个月后,患者发生了伴有咳嗽和发热的免疫相关性肺炎(2级)。患者在停止治疗1个月后成功从肺炎中恢复,并接受地塞米松治疗1周,随后选择接受纳武利尤单抗(180 mg q2w)联合瑞戈非尼(80 mg qd)方案再激发。出乎意料的是,8个月的疗程后,患者的肝脏和盆腔多发转移灶迅速消退,CEA从398 ng/mL降至3 ng/mL,CA199从8210 U/mL降至35 U/mL,达到CR。联合治疗16个月后,患者接受瑞戈非尼(80 mg qd)维持治疗,恢复正常工作和日常活动。截至2023年5月,CR持续了28个月,没有任何复发或转移的证据。
对患者的肿瘤组织样本进行NGS检测,发现ERBB3 G284R突变和扩增是主要的致癌性分子变异。此外,还检测到CDKN2A/B p16INK4a (H83Y)、TP53 (M246I)和TERT启动子(124C>T)的突变和低TMB(图2)。
讨 论
虽然ICIs在MSI-H状态的患者中显示出显著的疗效,而此类患者仅占全部mCRC病例的2%-4%。MSS型CRC的特点是肿瘤突变负荷低和免疫细胞浸润可忽略不计,由于对免疫治疗几乎没有反应而被称为“冷肿瘤”。目前的研究正在积极探讨联合治疗策略作为一种将MSS“冷肿瘤”转化为免疫反应性“热肿瘤”的手段的可行性。虽然一些临床试验已经对ICIs联合化疗、贝伐珠单抗、西妥昔单抗和丝裂原活化蛋白激酶激酶(MEK)抑制剂进行了研究,但这些研究未能显示该联合方案显著改善ORR、PFS或OS。
MSS结直肠癌患者肿瘤微环境中存在免疫抑制细胞,包括调节性T细胞(Tregs)和TAMs。这些细胞能有效抑制T细胞的活性。临床前研究表明,多激酶抑制剂瑞戈非尼可通过抑制集落刺激因子1受体(CSF1R)和血管内皮生长因子受体(VEGFR)减轻Tregs和TAMs对T细胞的免疫抑制作用。这一机制可用于克服MSS CRC的ICIs耐药。
日本最近的一项试验REGONIVO研究报告,25例MSS mCRC患者的ORR为36%,PFS为7.9个月。在北美REGONIVO试验中,在MSS mCRC患者中,瑞戈非尼联合纳武利尤单抗的ORR为7%。PFS和OS分别为1.8个月和11.9个月,均低于日本REGONIVO研究的结果。与REGONIVO研究的结果相反,最近对18例MSS mCRC患者进行的一项回顾性研究显示,瑞戈非尼联合纳武利尤单抗或帕博利珠单抗的临床活性较差。DCR率仅为31%,无患者达到客观缓解。该研究的作者建议,临床应避免在MSS mCRC患者中使用该联合方案,尤其是有肝转移的患者。
本研究评估了瑞戈非尼和抗PD-1抗体作为三线或三线以上治疗21例难治性MSS mCRC患者的疗效。总体而言,本研究的治疗方案在患者中显示出一定的治疗效果。尽管本研究的缓解率低于日本REGONIVO研究,但总体ORR和DCR分别达到19%和28.5%,观察到1例患者达到CR, 3例患者达到PR, 2例患者达到SD。此外,中位PFS为4个月,中位OS为25个月。值得注意的是,在既往接受过瑞戈非尼治疗并发生疾病进展的mCRC患者中,中位PFS和OS分别为2和7个月。本研究结果发现,与常规治疗相比,本研究结果更有利。因此,联合治疗可能是难治性MSS结直肠癌的一种可行的治疗选择。
尽管联合治疗的结果很有前景,但仍有相当一部分MSS CRC(71.5%)出现疾病进展。因此,进一步研究能够有效分层患者人群、提高生存获益的生物标志物至关重要。在DCR预测因素的亚组分析中,治疗的临床获益与ERBB2/ERBB3状态相关。ERBB2/ERBB3突变患者对这一联合方案的应答良好(ORR,60% vs 6.2%;P=0.028)。ERBB2/ERBB3突变患者的中位PFS显著优于野生型患者(15个月 vs 4个月;P=0.022)。在唯一一例CR患者中,研究者发现该患者同时存在ERBB3 G284R突变和ERBB3扩增。
HER2和HER3分别由ERBB2和ERBB3表达,是在细胞膜上形成异二聚体的酪氨酸激酶受体。ERBB2/ERBB3突变导致ERBB信号通路异常激活,促进肿瘤增殖和转移,这一过程可被瑞戈非尼抑制。全外显子组测序发现CRC中ERBB2和ERBB3突变(包括短变异突变和拷贝数扩增)的频率为6.5%-11.5%,并且ERBB2/ERBB3突变患者预后较差。HER2/HER3也可能成为用于ERBB2/ERBB3突变CRC的治疗方案的一个有吸引力的治疗靶点。临床前研究表明,基因组ERBB2/ERBB3突变通过抑制肿瘤反应性T细胞的能力和减少干扰素(IFN-γ)和白细胞介素-2(IL-2)的释放,促进胆囊癌中PD-L1介导的免疫逃逸。ERBB信号通路抑制剂和抗PD-L1抗体的联合治疗逆转了这些免疫抑制作用,显示出有前景的治疗活性。
先前的研究发现,ERBB2和ERBB3在CRC中的变异频率为6.5%-11.5%,而在本研究中,23.8%的mCRC患者存在ERBB2/ERBB3变异。本研究为真实世界的回顾性分析,根据患者的实际情况制定治疗方案。对于有ERBB2/ERBB3变异的难治性MSS mCRC患者,研究者倾向于使用瑞戈非尼单药或联合治疗,因为ERBB2/ERBB3突变是瑞戈非尼的靶点之一,这导致本研究人群中ERBB2/ERBB3变异的发生率较高。然而,ERBB2/ERBB3变异发生率的升高并不影响结果的分析。据公共数据库报道,在CRC患者中ERBB2和ERBB3变异与DFS和OS无关。在本研究中,较高的ERBB2/ERBB3变异率并不预示更好的预后或疗效。
联合治疗的毒性耐受性与之前的研究相当,TRAE的发生率与常规治疗(如瑞戈非尼单药治疗)相似。值得注意的是,本研究中唯一获得CR的患者在治疗2个月后发生了免疫相关性肺炎(ir-肺炎,2级),可能是由于免疫反应过度。停药1个月,给予地塞米松治疗后痊愈。在肺炎发作期间,CEA和CA199显著下降,再次激发治疗获得CR。因此,irTRAEs可能预示着PD-1治疗更好的抗肿瘤效果,需要仔细考虑权衡irTRAEs的风险和潜在的疗效获益。
本研究有几个局限性。首先,本研究为回顾性研究,样本量较小。因此,任何疗效分析都是初步的,ERBB突变作为潜在生物标志物的作用尚不能完全评估。这一策略需要在大型队列中进行前瞻性验证。研究者目前正在进行一项 II期前瞻性研究,在有ERBB2/ERBB3突变的MSS mCRC患者中评估瑞戈非尼联合特瑞普利单抗的潜在疗效。其次,这是一项真实世界研究,包括本研究中使用的四种不同的抗PD-1抗体。瑞戈非尼和抗PD-1抗体的剂量在患者间不均匀,这将进一步增加本研究的异质性。
基于本研究结果,研究者推测ERBB2/ERBB3突变导致MSS患者发生免疫逃逸,而瑞戈非尼可以通过靶向ERBB通路重新激活肿瘤微环境,使“冷肿瘤”转化为“热肿瘤”,从而协同增强抗PD-1抗体的治疗效果。综上所述,研究者发现瑞戈非尼联合PD-1抑制剂为化疗难治性MSS mCRC提供了一种可行的治疗方案,且毒性可耐受。ERBB2/ERBB3突变患者可能对该联合方案敏感。
参考文献:
Dai X, Ding W, He Y, Huang S, Liu Y, Wu T. Refractory microsatellite stable metastatic colorectal cancer with ERBB2/ERBB3 mutation may be preferred population for regorafenib plus PD-1 inhibitor therapy: a real-world study. Front Oncol. 2023;13:1227644. Published 2023 Aug 23. doi:10.3389/fonc.2023.1227644
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)