首页 > 医疗资讯/ 正文
导读
目前PARP抑制剂的选择主要基于同源重组修复(HRR)基因中的胚系或体细胞致病性变异,尤其是BRCA1、BRCA2和PALB2基因。但并非所有携带HRR基因突变的肿瘤都具有HRD表型,基于基因组疤痕的检测(HRDsig)识别HRD是目前最具应用前景检测方法。
该研究入组了携带HRR基因的患有不可切除、局部晚期或转移性实体瘤的后线治疗患者,根据不同的致病性胚系或体细胞突变分为队列A(BRCA1、BRCA2、PALB2、RAD51C和RAD51D)及队列B(BARD1、BRIP1、FANCA、NBN和RAD51B)。主要研究终点为队列A的总体缓解率(ORR)。
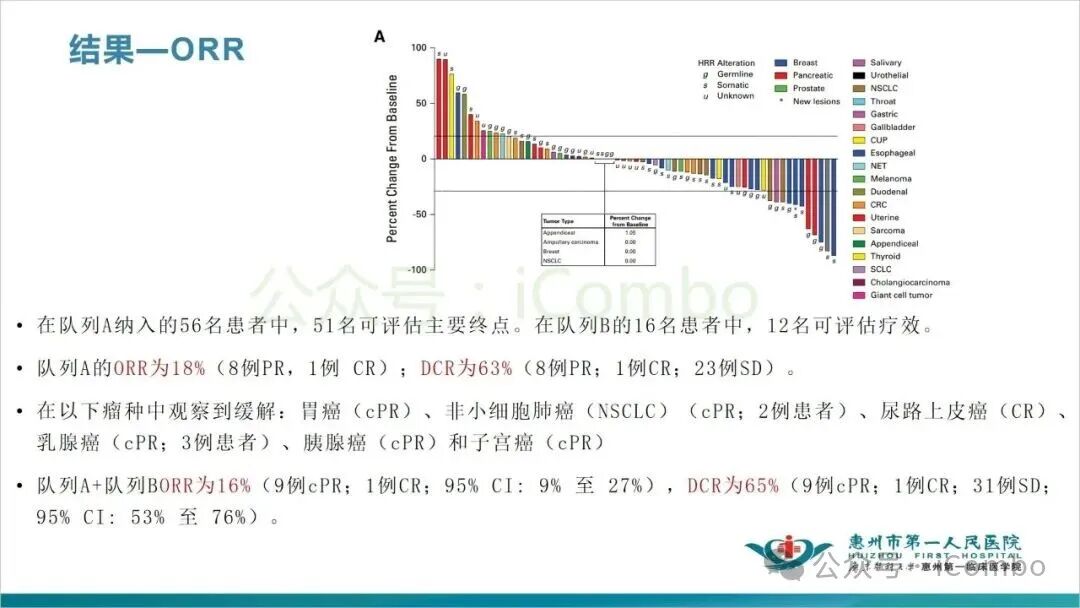
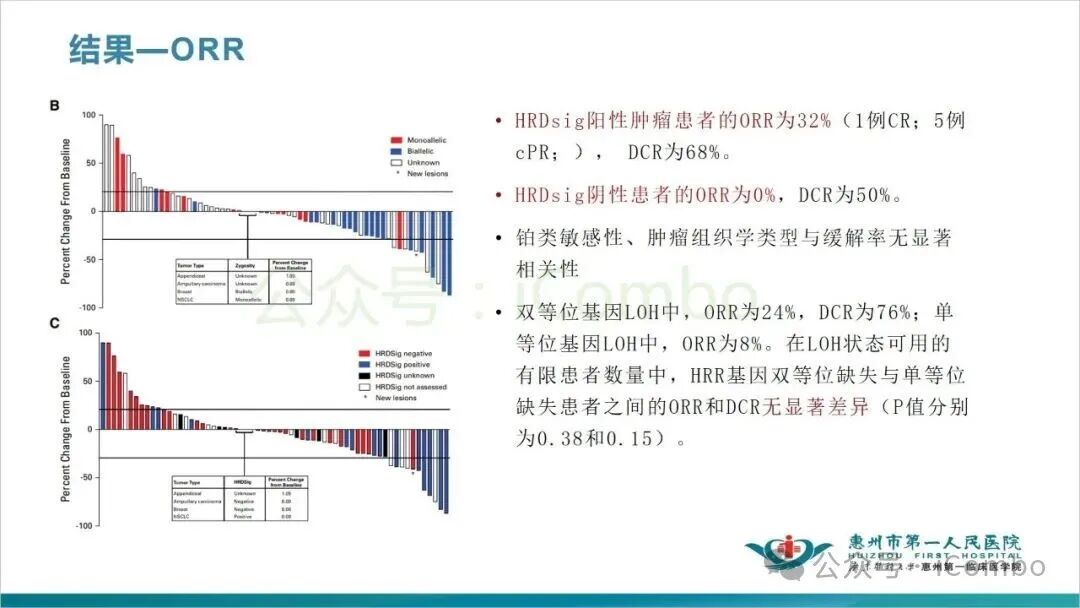
入组83名患者,其中63名在队列A,20名在队列B。最终分析纳入了队列A的56名患者和队列B的16名患者。队列A的ORR为18%(8例PR,1例 CR);DCR为63%(8例PR;1例CR;23例SD)。队列A+队列B的ORR为16%(9例cPR;1例CR;95% CI: 9% 至 27%),DCR为65%(9例cPR;1例CR;31例SD;95% CI: 53% 至 76%)。HRDsig阳性肿瘤患者的ORR为32%(1例CR;5例cPR;), DCR为68%。HRDsig阴性患者的ORR为0%,DCR为50%。
次要研究终点方面,所有患者的mPFS为5.5m,队列A的mPFS为5.52m。HRDsig阳性:mPFS 5.52m;HRDsig阴性:mPFS为3.98m(HR 0.59);铂敏感:mPFS 7.82m;铂耐药:mPFS 3.52m(HR 0.16;P = 0.02)。所有患者的mOS为12.12m,队列A的mOS为13.63m;HRDsig阳性:mOS 11.83m;HRDsig阴性:mOS 9.99m(HR 0.56;P = 0.19)铂敏感:mOS 未达到;铂耐药:mOS 5.45m(HR 0.11;P = 0.01)。
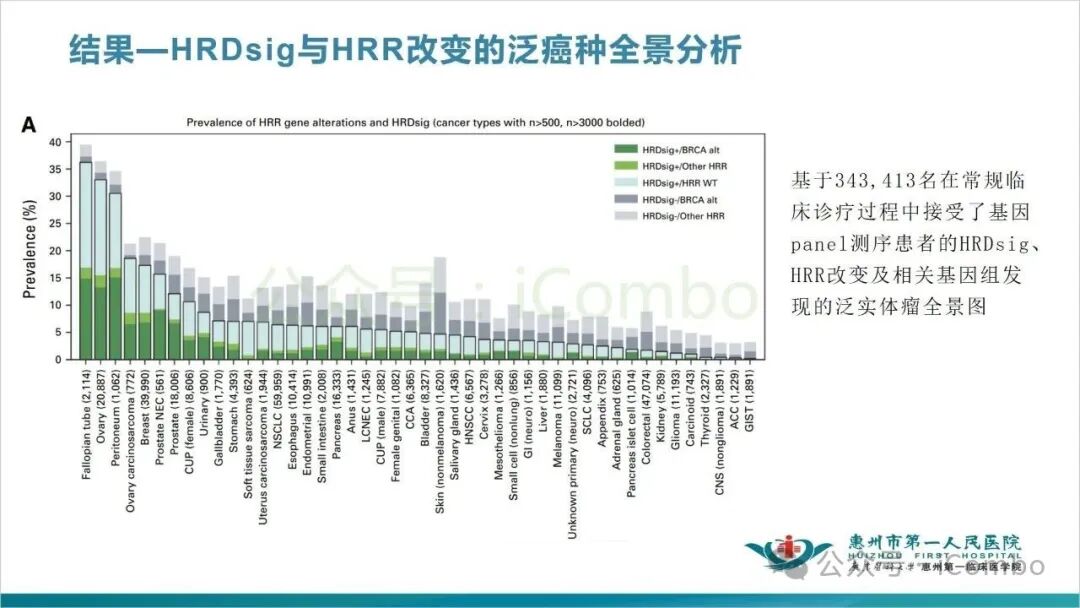
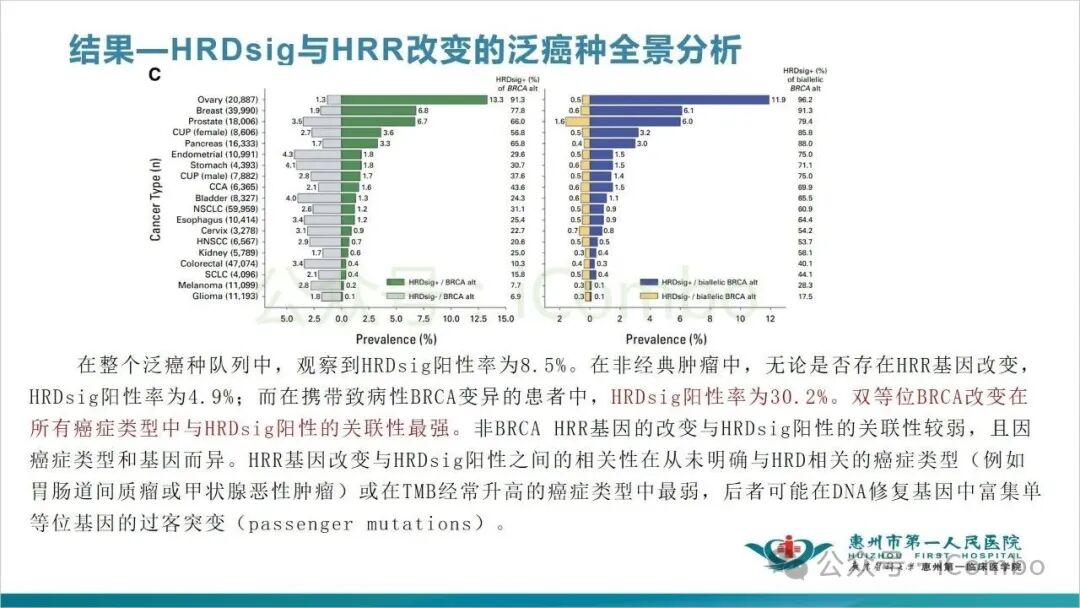
在HRDsig与HRR改变的泛癌种全景分析中,在携带致病性BRCA变异的患者中,HRDsig阳性率为30.2%。双等位BRCA改变在所有癌症类型中与HRDsig阳性的关联性最强。非BRCA HRR基因的改变与HRDsig阳性的关联性较弱。
研究表明,只有一部分HRR基因改变(特别是核心基因的双等位缺失)会导致真正的HRD并预测PARPi敏感性,尤其是在铂类敏感的情况下。HRDsig可能有助于识别可能从PARPis中获益的肿瘤,尤其是在非经典的HRR基因改变的瘤种中。在HRDsig阴性的肿瘤患者中未观察到任何缓解(JCO Precis Oncol. 2025 Jul:9:e2500090. doi: 10.1200/PO-25-00090)


















- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)