首页 > 医疗资讯/ 正文
当我们谈论衰老,总会好奇:为什么有些人年过半百仍身手矫健,而另一些人却早早被慢性病缠身?为什么皮肤的皱纹可以通过保养延缓,而血管的老化却常常悄无声息地引发致命危机?这些看似无解的衰老谜题,或许能从人体蛋白质的动态变化中找到答案。
一项发表在《Cell》杂志上的研究,通过分析跨越50年人生的蛋白质组图谱,首次揭开了不同器官衰老的"秘密时刻表"。研究团队对13种人体组织、516份样本进行了深入分析,从蛋白质的视角绘制出人类衰老的全景画卷,不仅发现了血管系统是最"早衰"的器官,还找到了加速全身衰老的关键蛋白质"元凶"。

跨越半世纪的蛋白质追踪计划
为了破解衰老的分子密码,研究人员开展了一项规模宏大的"人体蛋白质时空之旅"。他们收集了76名14至68岁个体的组织样本,涵盖了心血管、消化、免疫等七大系统的13种组织——从跳动的心脏到坚韧的主动脉,从过滤血液的脾脏到抵御外界的皮肤,甚至包括流动的血液样本,构建了目前最全面的跨组织衰老蛋白质组数据库。
通过先进的质谱技术,研究团队精准量化了超过12771种蛋白质,这些蛋白质如同一个个"分子时钟",记录着不同器官随年龄增长的变化轨迹。更特别的是,他们同时分析了基因转录与蛋白质表达的关系,发现了一个令人惊讶的现象:随着年龄增长,基因蓝图(mRNA)与最终产物(蛋白质)之间的"沟通"变得越来越不顺畅。
这种"转录组-蛋白质组解耦"现象在脾脏、肌肉和淋巴结中尤为明显。打个比方,就像工厂的设计图纸与实际生产的产品出现了偏差,随着年龄增长,这种偏差越来越大。这解释了为什么单纯研究基因表达难以完全揭示衰老的秘密——蛋白质才是执行生命功能的"实际操作者",它们的动态变化更能反映衰老的真相。
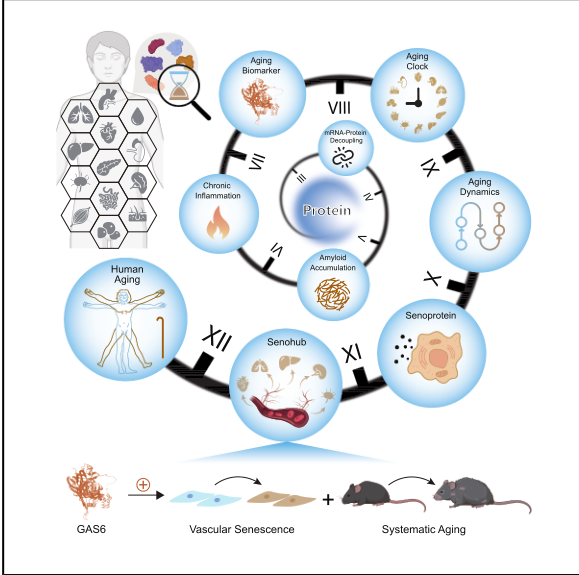
研究截图,直观展示了蛋白质是衰老的核心调控者,并以 GAS6 为例,阐明 “血管衰老→全身衰老” 的级联机制,同时整合了衰老的多维度蛋白质组特征
器官衰老的"异步交响曲"
如果把人体比作一座城市,那么每个器官就像不同的建筑:有的坚固耐用,有的却早早出现裂缝。研究通过构建"蛋白质衰老时钟"发现,不同器官的衰老速度差异显著,构成了一曲并不和谐的"异步交响曲"。
血管系统,特别是主动脉,是这场衰老交响乐中"抢拍"最明显的乐器。研究发现,主动脉的蛋白质组从30岁开始就出现显著变化,其衰老速度远超其他器官。这也解释了为什么心血管疾病常常成为人类健康的"头号杀手"——血管的衰老启动得比我们想象中早得多。
与之相对,肝脏、胰腺等消化器官的衰老节奏则相对缓慢,其蛋白质组的显著变化多发生在50岁之后。更有趣的是,所有器官似乎都存在一个"衰老拐点"——50岁左右,蛋白质组的变化会出现一次"加速换挡",多种衰老相关蛋白的表达在此阶段发生剧烈波动。这与临床观察中50岁后慢性病发病率显著上升的现象不谋而合。
蛋白质稳态的崩塌:衰老的共同特征
在所有组织的衰老轨迹中,研究人员发现了一个共同的"罪魁祸首":蛋白质稳态的逐渐崩溃。就像一个精密的工厂,细胞内的蛋白质需要精准合成、正确折叠、及时运输并在失效后被妥善降解,这个平衡一旦被打破,衰老就会加速到来。
研究观察到,随着年龄增长,负责蛋白质合成的核糖体蛋白、帮助蛋白质折叠的分子伴侣(如CCT家族蛋白),以及负责清理"垃圾蛋白"的蛋白酶体成分(如PSMB1)的数量都在减少。与此同时,错误折叠的淀粉样蛋白(如SAA1、SAA2)和过度激活的免疫球蛋白、补体成分却在不断积累,形成了一种"清理能力下降而垃圾不断堆积"的恶性循环。
这种蛋白质稳态的失衡在血管组织中表现得尤为突出。主动脉中淀粉样蛋白的堆积会激活免疫反应,引发慢性炎症,就像血管壁上不断扩大的"锈迹",最终导致血管弹性下降、血压升高,为心脑血管疾病埋下隐患。
游走全身的"衰老信使"
最令人惊讶的发现是,某些蛋白质不仅在衰老组织中异常增多,还会释放到血液中,成为驱动全身衰老的"信使"。研究团队将这类蛋白质命名为"衰老蛋白"(senoproteins),它们就像流动的"衰老信号弹",从早衰的器官扩散到全身,加速其他组织的老化。
GAS6蛋白就是其中的典型代表。这种蛋白在衰老的主动脉中大量产生并释放到血液中,通过与广泛存在的TAM受体结合,引发一系列连锁反应:在血管内皮细胞中,它会增加衰老标志物SA-β-Gal的活性,提高p21Cip1的表达,破坏血管的修复能力;在免疫细胞中,它会促进炎症因子IL-6的释放,加剧慢性炎症状态。
更可怕的是,研究人员通过动物实验证实,向中年小鼠注射GAS6蛋白后,短短几周内,小鼠就出现了gripstrength下降、平衡能力减弱等衰老症状,其主动脉出现明显的氧化损伤和脂质沉积,肝脏、脾脏等多个器官也呈现出加速衰老的迹象。这意味着,血液中这些"衰老信使"的水平,可能直接决定了人体的衰老速度。
另一类关键的衰老蛋白GPNMB则在皮肤和血管组织中表现突出。体外实验显示,它能诱导血管平滑肌细胞出现衰老表型,而体内注射会导致小鼠血管壁增厚、弹性下降,进一步证实了这些蛋白质在全身衰老中的驱动作用。
从实验室到临床:抗衰老的新希望
这项研究不仅揭示了衰老的分子机制,更为抗衰老干预提供了精准靶点。通过分析血浆中与组织衰老同步变化的蛋白质,研究团队开发出"血浆蛋白质替代时钟",只需一滴血就能评估多个器官的生物学年龄,为个性化抗衰老方案提供了可能。
更重要的是,那些被鉴定出的衰老蛋白,如GAS6和GPNMB,成为了极具潜力的治疗靶点。研究人员提出,通过PROTAC技术降解这些异常蛋白,或开发中和抗体阻断其作用,可能成为延缓全身衰老的新策略。此外,针对血管这一"衰老枢纽"进行早期干预,或许能从源头阻断衰老的扩散,为预防心脑血管疾病开辟新途径。
当然,研究也存在一定局限。由于人体组织样本的限制,大脑、肾脏等关键器官的衰老数据尚未纳入分析,未来还需要更大规模的队列研究来验证这些发现。但不可否认的是,这幅跨越半世纪的蛋白质组图谱,已经为我们打开了理解衰老的全新窗口。
当我们站在蛋白质的微观视角重新审视衰老,会发现这场生命的自然过程并非不可捉摸的宿命。那些在血管中堆积的淀粉样蛋白,那些随血液游走的衰老信使,既是衰老的标志物,也是干预的突破口。或许在不久的将来,我们真的能通过调节这些蛋白质的活性,让心脏、血管和皮肤的衰老节奏重新同步,实现健康长寿的美好愿景。而这一切的起点,正是对人体蛋白质密码的不懈探索。
参考文献:
Ding Y, Zuo Y, Zhang B, Fan Y, Xu G, Cheng Z, Ma S, Fang S, Tian A, Gao D, Xu X, Wang Q, Jing Y, Jiang M, Xiong M, Li J, Han Z, Sun S, Wang S, He F, Yang J, Qu J, Zhang W, Liu GH. Comprehensive human proteome profiles across a 50-year lifespan reveal aging trajectories and signatures. Cell. 2025 Jul 22:S0092-8674(25)00749-4. doi: 10.1016/j.cell.2025.06.047. Epub ahead of print. PMID: 40713952.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)