首页 > 医疗资讯/ 正文
论坛导读:LMNB1相关常染色体显性白质营养不良症(ADLD)是一种由LMNB1致病性变异引起的成人发病的进行性神经退行性遗传疾病,其典型特征是在临床症状出现前几十年,中枢神经系统中对称性进行性白质丢失,这通过MRI上大脑和脊髓中的白质高信号得到证实。这种致命的疾病通常开始于40和50岁,通常以自主特征如便秘和膀胱功能障碍开始,随后发展为锥体和小脑受累。锥体受累的临床体征包括快速反射和阵挛,而小脑体征包括共济失调和震颤。精神和认知方面的体征和症状表现为晚期症状,通常在首次发病后10-20年出现。存活的中位年龄约为66岁,并且死亡是由于以虚弱和瘫痪为特征的显著神经恶化的结果。
脑白质病是一组各种原因引起的以白质病变为主要特点的疾病统称,谱系极广。脑白质营养不良是一组髓鞘形成或维持发生障碍的遗传性疾病,是脑白质病谱系中最重要的类型之一。 近年来,随着分子遗传学的进步,多数脑白质营养不良能够确诊并发现突变基因。但是,影像学改变仍然是临床诊断脑白质营养不良的主要依据,依赖于放射技术的发展,部分患者或携带者在疾病早期便可发现其脑白质异常,从而有助于进一步诊断和针对性治疗。 脑白质营养不良主要见于儿童,常在婴幼儿期发病,但目前除佩梅病没有成人型外,其他多数可在成人期发病。成人脑白质营养不良,或称为晚发型脑白质营养不良,临床主要表现为认知功能下降、精神行为异常、运动障碍、周围神经病、球麻痹和癫痫等,一般较儿童患者进展缓慢。
LMNB1相关的常染色体显性脑白质营养不良(LMNB1-related autosomal dominant leukodystrophy,ADLD)是一种极其罕见但报道不足的成人发病脑白质营养不良。它最初在19842年被描述为原发性进行性多发性硬化的鉴别诊断,此后在来自不同种族背景的超过33个家族中被描述。遗传病因学和临床表型现已明确。这是一种以自主神经功能障碍为特征的缓慢进行性疾病,随后出现锥体和小脑异常,导致痉挛、震颤和共济失调。自主神经功能障碍是普遍的,可能包括膀胱功能障碍、便秘、体位性低血压和/或勃起功能障碍。认知功能障碍可作为晚期表现出现。受影响的个体可能在发病后存活超过20年,但是生活质量受到显著影响。
ADLD是一种非常罕见的、缓慢进展的、以中枢神经系统对称性广泛髓鞘缺失为特征的、脑白质营养不良。由编码核纤层蛋白 B1 的 LMNB1 基因异常所致。通常于成年期(20~50 岁)起病,首发症状多为自主神经功能异常(尿便功能障碍,直立性低血压),后出现锥体束征和小脑症状。LMNB1中的致病性变异,主要是影响启动子的基因重复或上游缺失,导致核纤层蛋白B1的过量产生,核纤层蛋白B1是一种对核结构维持至关重要的核纤层蛋白。这种过度表达导致中枢神经系统脱髓鞘,部分是通过参与脂质生物合成和髓鞘维持的基因的下调。过量层粘连蛋白B1导致白质病理的确切途径仍在阐明,其潜在机制涉及基因表达改变、少突胶质细胞成熟中断和氧化应激。虽然锥体和小脑功能障碍与中枢神经系统脱髓鞘有关,但自主神经功能被认为是由于层粘连蛋白B1过度表达的其他作用。这是因为非髓鞘纤维参与了心血管系统和膀胱功能的去甲肾上腺素能调节,而这两者受到了特别的影响。
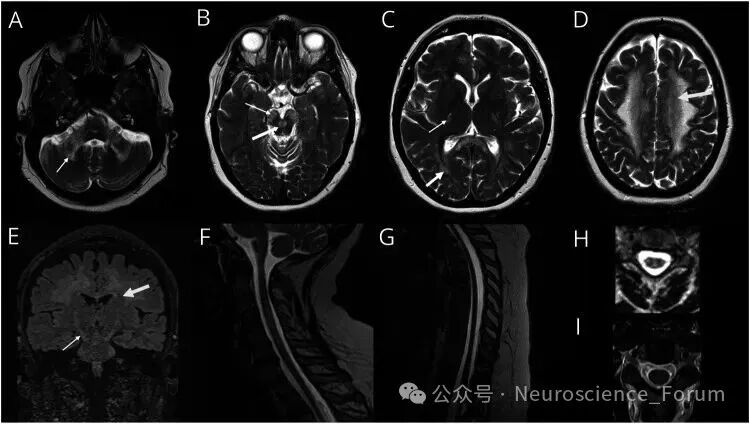
在报告的症状出现4个月后,45岁时获得的具有LMNB1重复的ADLD患者的大脑(A-E)和脊髓(F-H)的MR图像。doi: 10.1212/NXG.0000000000200287.
受影响个体的脑部MRI扫描显示异常,包括从运动皮质下方延伸并沿着皮质脊髓束向延髓锥体延伸的脑白质中的对称T2高信号。小脑脚早期受累。在大脑中,对称的高强度区域首先扩散到额叶和顶叶,然后是枕叶和颞叶。脑室周围区域受影响较小。放射学改变的进展最终导致脑萎缩。临床上,症状前个体的大脑和脊髓中可能存在白质变化,并伴有脊髓萎缩。磁共振波谱分析显示侧脑室脑脊液中有病理性乳酸盐积聚,但脑白质中没有。ADLD 的 MRI 特点:异常信号多见于额顶叶和小脑白质、小脑脚、皮质脊髓束和胼胝体;脑室旁白质相对受累不明显;晚期可有弥漫脑白质病变。
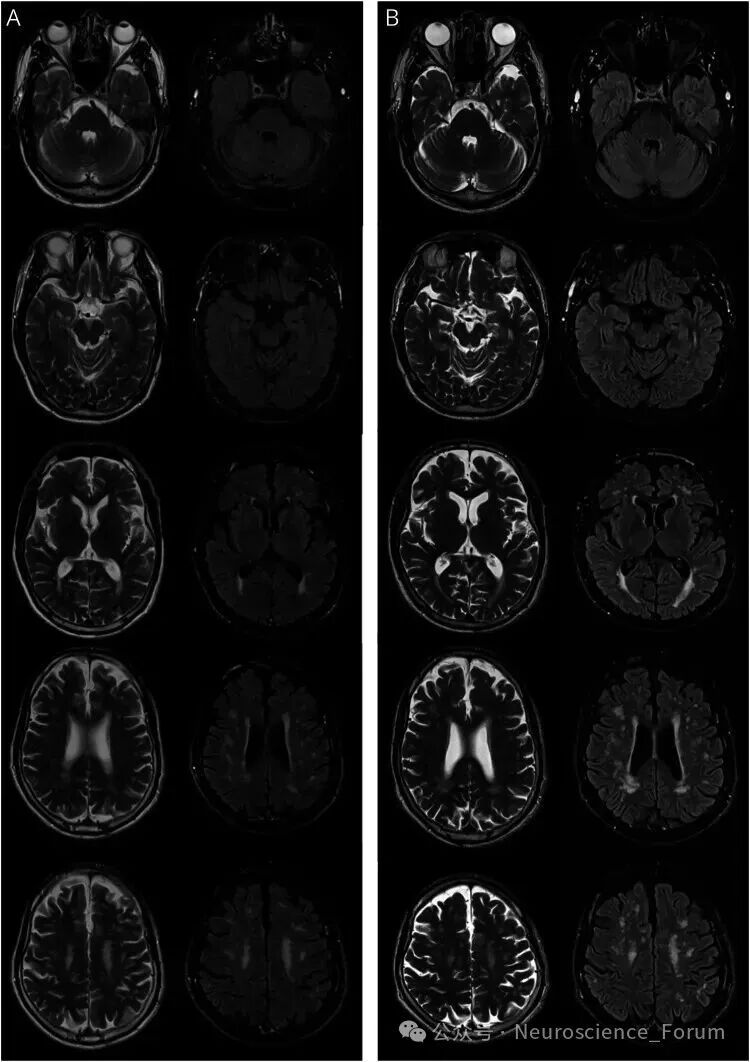
在基线(A)和2年(B)时进行MRI脑部检查,显示t 2加权和液体衰减反转恢复(FLAIR)图像。左边的图像对应于T2加权序列,而右边的图像代表FLAIR序列。doi: 10.1212/NXG.0000000000200261.
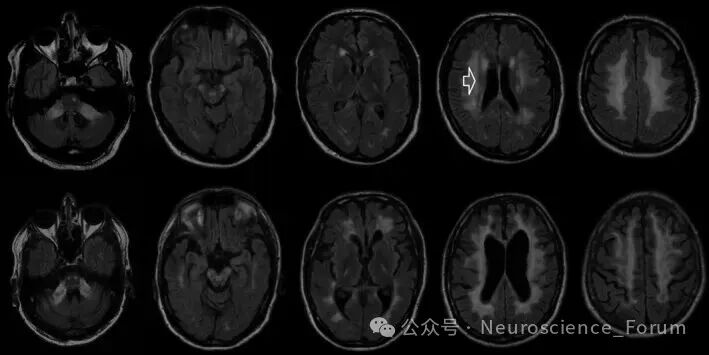
最轻微和最严重患者的MR图像。患者1,顶行,出现MRI级改变,小脑脚、皮质脊髓束以及额叶、顶叶和枕叶的幕上白质出现T2高信号。可以看到较少受影响的室周边缘(箭头)。患者2,底部一行,呈现5级变化,白质变化延伸至颞叶,以及脑室和脑沟扩大。T2加权流体衰减反转恢复(FLAIR)序列。doi: 10.1111/ane.13024.
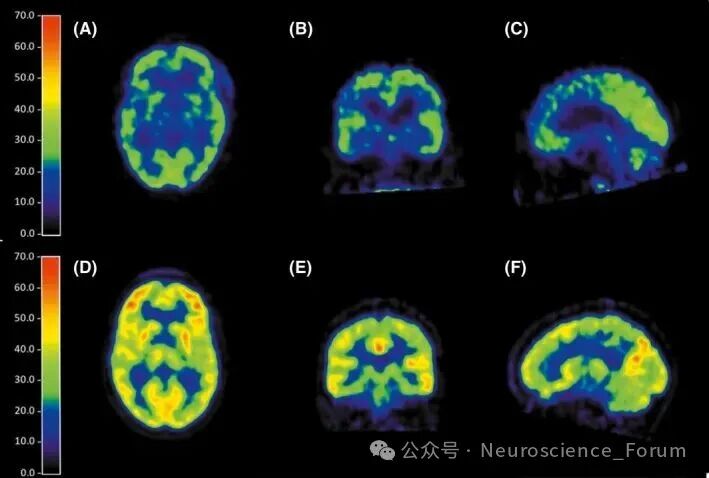
与健康对照(D‐F)相比,受影响最严重的患者(患者5,A‐C)的FDG PET图像。轴向(A,D)、冠状(B,E)和矢状(C,F)图像显示患者葡萄糖代谢降低。doi: 10.1111/ane.13024.
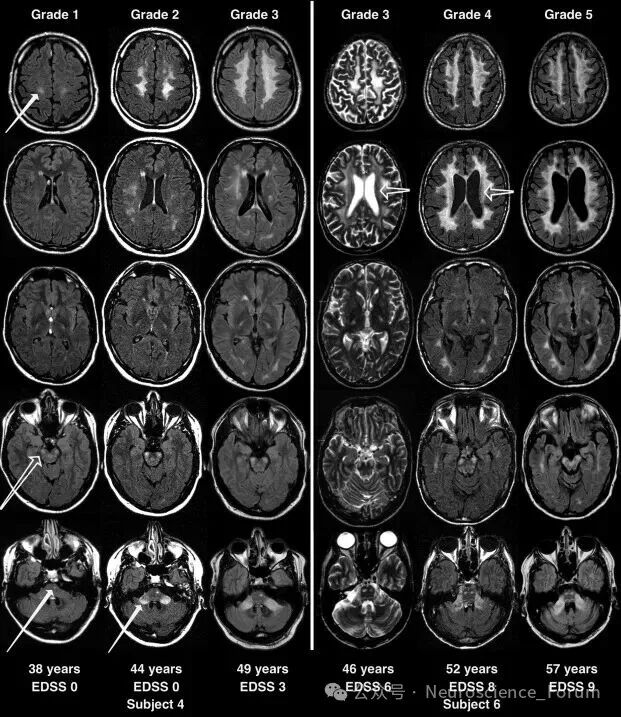
doi: 10.1002/ana.24452.
一项研究MRI显示了所有受试者的脑和脊髓中的病理发现,以及有症状和无症状受试者的脑变化的规律进展。在大脑中,受试者首先在运动皮层下的白质中出现T2高信号。这些甚至在我们最年轻的受试者(29岁)中也存在,所以我们不能肯定在什么年龄可以首次观察到它们。T2高信号通过锥体束向下发展,这些发现可以先于疾病症状长达16年。一些无症状受试者的变化程度令人吃惊。许多病变面积很大的患者表现出相对较轻的症状。一种解释可能是缺乏炎症和神经元的保存。质子磁共振波谱仅显示水含量增加,与病变中髓鞘的空泡化相一致,但与主要代谢物之间没有病理关系。脑白质中ADC值的增加与扩散率的增加一致,一些T2加权FLAIR图像中信号强度的下降也与自由水含量的增加一致。在所有14名成像受试者中,脊髓是细的,并显示病理性白质信号强度。
与识别受ADLD影响的个体和一般临床概述相关的建议得到了已发表的关于LMNB1相关ADLD的工作的有力支持。当特征性脑MRI发现与自主神经功能障碍症状、显示显性遗传的家族史或特征性脊髓MRI一起被识别时,临床应怀疑LMNB1相关ADLD。典型地,发病在成年期是隐匿的,并逐渐发展。偶尔的急性恶化可能由疾病引发,随后恢复到基线水平。这些诊断建议得到了已发表的LMNB1相关ADLD病例系列和专家共识的一致支持。利用这一临床概述,建议将有助于早期考虑这一诊断,并显著减少LMNB1相关ADLD患者的诊断时间。
准确的诊断:标准化的基因检测协议确保受影响的个体得到准确和及时的诊断,从而能够使用2025 ICD-10厘米诊断代码G90。B为LMNB1相关的ADLD,并结束了许多诊断奥德赛。
管理:一种结构化和标准化的临床评估方法,包括MRI和自主功能测试,允许针对疾病的具体症状和进展制定个性化的管理计划,以及跨中心的统一护理。
早期干预:通过标准化评估进行定期监测,可以早期发现并发症,促进及时的个性化干预,从而提高生活质量和结果。
多学科护理:专家(神经学家、遗传学家、遗传顾问、理疗师等)的协同努力。确保全面的护理,除了遗传风险和计划生育之外,解决该疾病的神经和非神经方面的问题。
改善患者教育:标准化指南有助于卫生保健提供者提供关于疾病、其管理和可用支持资源的一致信息,增强受影响个人及其家庭的能力。
参考文献- Dhamija R, et al. Clinical Practice Guidelines for the Diagnosis, Management, and Surveillance of LMNB1-Related Autosomal Dominant Leukodystrophy. Neurol Genet. 2025 Aug 29;11(5):e200287. doi: 10.1212/NXG.0000000000200287.
- Wang JDJ, et al. Atypical Presentation of an LMNB1 Duplication Involving the Silencer Region: Beyond Classical Autosomal-Dominant Leukodystrophy. Neurol Genet. 2025 Apr 17;11(3):e200261. doi: 10.1212/NXG.0000000000200261.
- Finnsson J, et al. Glucose metabolism in the brain in LMNB1-related autosomal dominant leukodystrophy. Acta Neurol Scand. 2019 Feb;139(2):135-142. doi: 10.1111/ane.13024.
- Finnsson J, et al. LMNB1-related autosomal-dominant leukodystrophy: Clinical and radiological course. Ann Neurol. 2015 Sep;78(3):412-25. doi: 10.1002/ana.24452.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)