首页 > 医疗资讯/ 正文
-01-
引言
T细胞接合器(TCE)是一种很有前途的癌症免疫疗法,可以重新引导T细胞杀死肿瘤细胞。然而,它们的临床应用受到几个挑战的限制,包括细胞因子释放综合征(CRS)、脱靶毒性以及受到血液学和实体瘤中的免疫抑制。
最近,TCE设计中出现了许多旨在提高其安全性和有效性的创新。关键进展包括优化几何形状以促进有效的免疫突触,优化抗CD3/TCR结构域的亲和力,以及靶向特定的T细胞亚群,这些都旨在减少CRS。逻辑门控方法,如由肿瘤微环境因素激活的双靶向和条件性TCE,有可能降低靶向、非肿瘤毒性,并可能增加反应的深度和持久性。此外,利用共刺激信号传导有可能进一步提高血液学和实体瘤的疗效。下一代TCE有望克服传统TCE的一些局限性,增强其治疗窗口并实现联合治疗。随着该领域的发展,TCE有望成为癌症免疫疗法的基石,改善更广泛患者的预后。
-02-
一、影响TCE疗效和安全性的特征
优化TCE几何结构
TCEs的大小和结构是影响其疗效和药代动力学(PK)特性的关键因素。通常,TCEs被设计成具有小而灵活的结构,以允许T细胞和肿瘤细胞之间的紧密接近,从而提高突触形成的效率。这种形式的一个例子是BiTE,由串联的scFv组成,其中两个scFv通过一个短的柔性接头连接。然而,由于其大小和形式(没有Fc尾部),BiTE会迅速从体内清除,因此需要频繁给药。为了应对这些挑战,各种修饰,如聚乙二醇化、白蛋白结合结构域的掺入或与抗体Fc区的融合,已被用于延长TCE的半衰期,而不会损害其结合特性和功效。
除了大小,TCE的结构在决定T细胞和肿瘤细胞之间的突触距离方面也起着重要作用,这对T细胞活化和肿瘤细胞杀伤至关重要。TAA结合臂的定位、靶向表位和接头长度等几个因素有助于有效的免疫突触形成。研究表明,T细胞和抗原呈递细胞之间有效形成突触的最佳膜距离约为15 nm,5该距离对应于天然TCR肽-MHC复合物的大小,并与IgG1抗体的Fab臂跨度相匹配。
此外,TCE亲和力和价态也是优化的关键组成部分。与单价对应物相比,通过结合多个TAA结合结构域来增加对肿瘤靶点的价态可增强TCE的亲和力,可导致更有效的肿瘤杀伤,以及在以低TAA表达和异质性TAA表达为特征的肿瘤环境中的活性。此外,二价TAA结合可在不影响活性的情况下降低单个TAA结合物的亲和力,从而潜在地避免与可溶性抗原的相互作用,从而导致下沉效应和减少暴露。具有靶向TAA的双Fab结构域和CD3(2+1形式)的Crossmab的TCE已在临床前研究和癌症患者中证明了抗肿瘤功效。同样,基于IgM的双特异性接合器具有五聚体或六聚体结构,通过多个结合位点提供高亲和力。虽然增加价态会增强结合强度,但这些更大、更复杂的分子可能具有不太有利的生物分布。因此,优化价态需要在最佳结合与有效肿瘤穿透和保留效力之间保持谨慎的平衡。
总体而言,创建最佳突触距离通常需要经验调整,因为接头长度、表位定位和TCE灵活性以及价态均影响细胞毒性潜力。
优化CD3结合和亲和力
越来越多的证据表明,TCE结合的CD3特定结构域可以显著影响T细胞活化、信号强度和整体治疗方案。CD3是由CD3ε、CD3δ、CD3γ和CD3ζ链组成的多亚基复合物,与TCR相关。每个亚基在信号转导中起着不同的作用,它们的可及性和方向各不相同。研究表明,不同的CD3结合抗体结合CD3ε链上的不同表位,这些差异会影响TCR信号传导,从而不同程度地影响细胞毒性和细胞因子释放,当整合到TCE中时,可能会导致更优的治疗方案。
TCE对T细胞上CD3/TCR复合物的亲和力是优化疗效和安全性之间平衡的另一个关键因素,特别是改善CRS方面,这是TCE疗法的一个显著副作用。CRS的严重程度取决于几个因素,如靶抗原表达、肿瘤负荷、TCE给药的剂量和时间表、TCE的PK和生物分布以及患者特征。CD3结合结构域的亲和力决定了TCE和T细胞之间相互作用的强度和持续时间,这会影响T细胞活化和细胞因子释放的程度和动力学。TCE最初倾向于高亲和力CD3结合(KD<10nM),因为它们在临床前模型中引发了强效的肿瘤细胞杀伤。然而,高亲和力的CD3结合也会诱导高水平的细胞因子释放,导致严重的CRS和治疗窗口狭窄。因此,具有亲和力减弱的CD3结合臂的TCE已被证明在体外和体内诱导了强大的肿瘤抗原特异性细胞毒性,细胞因子释放显著减少,表明有可能平衡有效的肿瘤杀伤与CRS。此外,降低抗CD3结构域亲和力还可以改善TCE的生物分布和PK特性,避免它们在富含T细胞的区域(如淋巴组织)积聚。
下表总结了已批准和处于临床开发后期的TCE的关键特征。
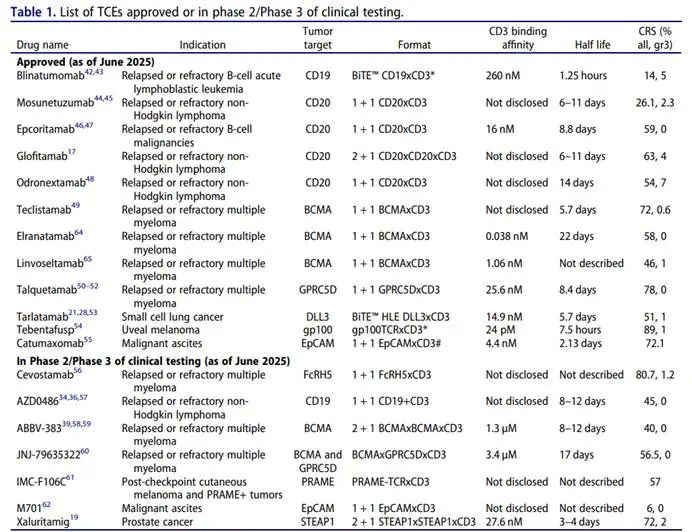
-03-
二、癌症治疗TCE开发的新策略
靶向特定T细胞亚群的TCE
激活特定的T细胞亚群,通过减少激活的T细胞数量和降低CRS相关毒性来提高TCE治疗指数是一种选择。研究表明,在体外使用双特异性TCE时,CD8+T细胞主要负责对癌细胞的定向杀伤。虽然CD4+T辅助细胞可以支持CD8+T功能并表现出细胞溶解活性,但它们的激活可导致细胞因子分泌和CRS相关的副作用。此外,TCE靶向CD4+细胞也可影响调节性T细胞增殖和活性。
在早期的研究中,用抗CD8抗体替代抗CD3以更选择性地靶向CD8+T细胞的尝试并没有取得很大成功。研究发现,虽然抗CD3和抗CD8抗体都能使用预激活的CD8+T细胞有效地重定向细胞毒性,但只有抗CD3对新分离的CD8+T淋巴细胞有效,这表明静息T细胞群需要“信号1”。针对T细胞上的CD3/TCR复合物和CD8的多特异性抗体的开发为这种方法提供了一种替代方案。这种替代方法比如 AstraZeneca 的 TITAN 平台,通过“CD8引导”,最大限度地减少了CD4+T细胞的活化,减少了细胞因子的释放,同时保持了细胞毒性。
靶向特定T细胞亚群的另一个例子,是Marengo Therapeutics的 tri-STAR平台,该平台包含一个肿瘤靶向结构域,并通过对特定TCR可变β链(Vβ)特异性选择性激活实体瘤中富含的T细胞亚群。这种方法允许肿瘤导向的细胞毒性,但只会激活一小部分T细胞,从而降低CRS的可能性。
此外,尽管传统的基于CD3的TCE也可以招募γδT细胞,但选择性靶向γδT淋巴细胞也可能提供一个减少CRS的机会,因为与γδT细胞核相比,这些细胞的频率较低。针对此类细胞的靶EGFR-Vδ2双特异性T细胞接合器(LAVA-1223)目前正在临床试验中。
肽-MHC复合物作为TCE的新靶点
2022年1月,美国食品和药物管理局(FDA)批准ImmTAC双特异性抗体tepentafsp用于葡萄膜黑色素瘤,这标志着TCE治疗实体瘤的一个重要里程碑。Tebentafsp通过亲和性增强的可溶性TCRαβ可变片段结合癌症细胞上的gp100肽-MHC(pMHC)复合物,并使用抗-CD3 scFv指导T细胞对黑色素瘤细胞的活性。这种pMHC-特异性TCE提供了靶向多种癌症抗原(包括细胞内蛋白)的可能性,将免疫疗法的范围扩大到传统的表面TAA之外。
同样,未成熟T细胞接合受体(TCER)由双重结合分子组成,其中TCR结构域靶向HLA背景下的肿瘤抗原,另一臂为T细胞接合结构域。靶向MAGEA4/A8的IMA401和靶向PRAME的IMA402在临床前研究和临床试验的早期阶段显示出有希望的安全性和显著的肿瘤抑制作用。此外,模拟TCR与HLA-呈递肽结合的TCR模拟抗体(TCRm)在靶向呈递突变Ras和p53新抗原的pMHC复合物方面也显示出有前景的临床前结果。
逻辑门控TCE增强肿瘤特异性
双靶向TCE代表了一类新兴的多特异性分子,旨在同时结合两种不同的TAA,为增强癌症免疫疗法的疗效和特异性提供了一种新的方法。这些TCE可以以两种形式开发:OR门控和and门控分子。每种形式都通过解决肿瘤异质性和靶向离瘤效应的挑战,为改善TCE治疗窗口提供了独特的优势。
OR门控双靶向TCE在识别肿瘤细胞表面的一个或两个TAA的同时激活T细胞。这种灵活的激活策略可以改善肿瘤识别,特别是在异质抗原表达的情况下,其中一些细胞可能只表达两种靶向抗原中的一种。通过在任一抗原存在时与T细胞结合,OR门控TCE可以帮助克服抗原异质性,并有助于预防由抗原阴性克隆的选择和外生长引起的肿瘤复发。然而,OR门控限制了常规药物组合提供的灵活性,因此需要仔细设计两个TAA臂,以确保两个臂都能达到最佳的效应剂量。
由于仅在肿瘤细胞上表达而不在健康基本组织中表达的TAA的稀缺性,以及肿瘤本身内抗原表达的异质性,给实体瘤双靶向TCE的开发带来了更大的挑战。
AND门控双靶向TCE通过TAA结合域的亲和力调节,优先靶向共表达TAA的肿瘤细胞。这种更严格的靶向方法可以提高治疗的特异性,从而降低对可能只表达两种抗原之一的健康组织的毒性。例如,三特异性TCE,tNY-aCD3/aEGFR,在临床前研究中显示出显著提高的治疗效果和选择性,并降低了肿瘤外效应的风险。
对于所有通过结合亲和力驱动AND门控的TCE,双TAA表达细胞相对于单个TAA表达细胞的选择性靶向可能受到多种参数的影响,如抗原表达水平、T细胞组织浸润水平和靶标内化。因此,需要对双重表达细胞的潜在优先活性进行实证评估,以充分评估这类分子的潜在治疗指数。总体而言,这些数据支持双靶向TCE通过减轻抗原异质性来提高疗效的潜力,以及通过提高肿瘤特异性来降低毒性的潜力。
基于TME因素的条件性TCE
条件性活性TCE利用TME的独特生理特性实现精确靶向,同时最大限度地减少全身毒性。目前的重点是设计仅在TME内普遍存在的特定环境条件下激活的TCE。这些包括蛋白酶介导的激活、pH或高ATP依赖性结合模块以及创新的工程分子相互作用。通过利用TME特有的功能,这些条件激活疗法有望增强治疗特异性,减少脱靶效应,并提高安全性,这代表了TCE靶向治疗癌症的新前沿。下表总结了目前正在开发的临床和临床前条件性TCE。
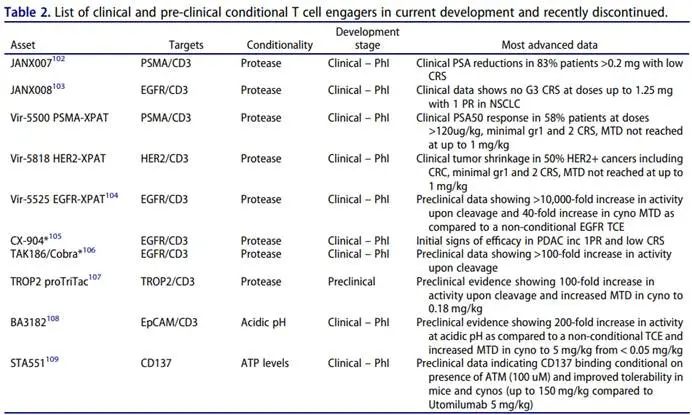
肿瘤相关蛋白酶是通过重塑细胞外基质、促进血管生成和促进转移在肿瘤进展中发挥关键作用的酶。与正常组织相比,这些蛋白酶,如基质金属蛋白酶(MMPs)、丝氨酸蛋白酶和半胱氨酸蛋白酶,在TME中的浓度更高。蛋白酶条件性激活的TCE核心是用蛋白酶不稳定的模块阻断CD3和/或TAA结合结构域,保护TCE不与其靶标结合,直到它们遇到富含蛋白酶的肿瘤环境。目前,有几种掩蔽策略正在进行临床前和临床研究,包括抗独特型抗体、大型非选择性非结构化多肽、以及选择性结合抗体结合袋的小肽。例如,JANX008(Janux Therapeutics)是一种双重掩蔽的条件性抗EGFR TCE,当蛋白酶激活被阻止时,其与CD3的结合受损1000倍,与EGFR的结合受损300倍。
与正常组织(pH 7.2–7.4)相比,TME的pH通常更显酸性(pH 6.5–6.9),这一特征可用于靶向治疗。这种pH差异源于癌症细胞代谢的改变,这导致了乳酸和其他酸性代谢产物在TME中的积累。例如,利用CDR区中的组氨酸,将抗体的结合结构域设计为对pH敏感,可使TCE在TME的酸性条件下优先具有活性,而在具有中性pH的正常组织中保持失活。例如,BF-588-DualCAB 在酸性条件下对 EpCAM 和 CD3 的亲和力显著提高,在非人灵长类动物中最大耐受剂量(MTD)较非条件性 TCE 提升 100倍。
三磷酸腺苷(ATP)的细胞外水平在TME中也显著升高,这是肿瘤内细胞更新和代谢应激增加的结果。STA551是一种抗CD137激动性抗体,在高ATP浓度存在的情况下,可以提高其与CD137的结合亲和力,确保其激动效应仅限于肿瘤区域。虽然目前还没有利用TME这一方面的TCE策略,但这可能被用来实现肿瘤部位TCE的激活,从而最大限度地降低全身免疫激活的风险。
工程分子相互作用也可以提供一种复杂的方法来实现TCE的高选择性和效力。一种这样的方法是前药激活链交换(PACE)技术,该技术通过独特的链交换反应在生理条件下产生多特异性抗体。该技术允许两种互补的非活性前药,靶向在肿瘤细胞上共表达的TAAs,通过链交换和仅在两个分子独立积聚的肿瘤部位重组活性CD3结构域形成活性TCE。此外,使用半体的TCE方法代表了一种新的策略,其由两个互补的半体组成,每个半体都整合了不同的抗原特异性单链可变片段,该片段与抗CD3抗体的可变轻链(VL)或重链(VH)结构域融合。当两个半体同时与靶细胞表面上的各自抗原结合时,它们会重建一个功能性的CD3结合结构域,从而激活T细胞以选择性地清除表达两种靶抗原的细胞。
通过共刺激信号提高TCE疗效
共刺激在支持T细胞激活、分化、获得效应器功能和存活方面发挥着至关重要的作用,这些信号的调节为改善癌症免疫治疗结果提供了机会。通过共刺激信号提高TCE疗效的策略包括靶向共刺激途径的TCE和靶向共刺激的分子与TCE的联合应用。
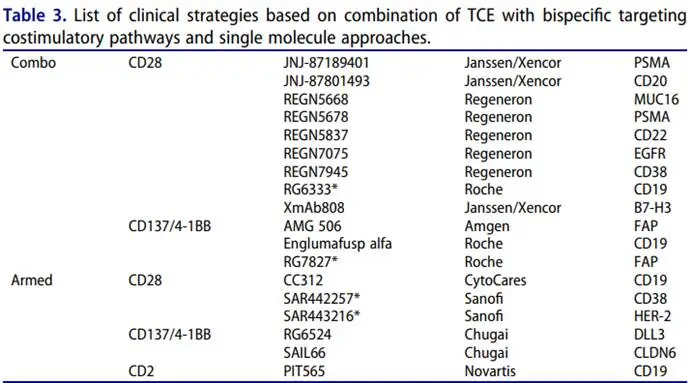
组合策略中,TCEs 可以与靶向共刺激分子(如 CD28、4-1BB)的双特异性抗体联用。例如,CD20 靶向 TCE(glofitamab)与 CD19-CD28 双特异性抗体联用,可显著增强 T 细胞在 B 细胞淋巴瘤中的活性。单分子策略,例如靶向 DLL3、CD3 和 CD137 的 TCE,在小细胞肺癌模型中可同时激活 T 细胞并提供共刺激信号,增强肿瘤浸润和杀伤。
-04-
结语
双特异性T细胞接合器是目前癌症治疗领域药物开发的热门方向,下一代的TCE需要提高肿瘤细胞的杀伤精度和安全性,并减轻耐药性的发展。成功开发下已开TCE的调整方向,包括微调TCE对CD3/TCR复合物的结合亲和力,实施双靶向TCE,设计条件激活策略,以及利用共刺激来改善血液学和实体瘤环境中的治疗结果等等。
通过这些努力,TCE有望成为各种肿瘤类型的标准护理的一部分,有可能扩大受益于免疫治疗的患者群体。创新将为TCE这种新型免疫疗法的发展奠定了基础,开创了一个有可能提高疗效和安全性的治疗新时代。
参考资料:
1.Innovative strategies for T cell engagers for cancer immunotherapy. MAbs. 2025 Jul 10;17(1):2531223
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)