首页 > 医疗资讯/ 正文
慢性肾病相关瘙痒(CKD-aP)是晚期肾病患者常见且令人极度困扰的症状,尤其是在接受血液透析的患者中,发病率高达60%以上,其中33%-50%患者存在中重度瘙痒。瘙痒不仅严重影响患者的生活质量,还与较高的死亡风险相关联。一项国际大型研究指出,血液透析患者中瘙痒与17%的死亡风险增加相关。传统治疗手段包括抗组胺药、皮质类固醇、钙调神经磷酸酶抑制剂等多为非特异性用药,且副作用明显,亟需更安全有效的新治疗方案。
目前,内源性阿片系统失衡被认为是CKD-aP发病机制的重要因素,尤其是κ-阿片受体(KOR)与μ-阿片受体信号的不平衡。安瑞克芬,前称HSK21542,是一种新型选择性、外周限制的κ-阿片受体激动剂,其独特的亲水性小肽及螺环结构增强了其对受体的亲和力,且极少穿透血脑屏障,降低了中枢神经系统相关副作用风险。

由浙江大学附属第一医院陈江华教授和东南大学附属中大医院刘必成教授联合牵头的一项安瑞克芬在中国50个中心完成的多中心、双盲、随机、安慰剂对照的Ⅲ期临床试验。结果显示,安瑞克芬显著降低了最严重瘙痒强度评分(WI-NRS),提高了瘙痒相关生活质量,且总体安全性良好。
研究人员纳入中国50个医疗中心的652例符合纳入标准的血液透析患者,最终545例患者随机分配至安瑞克芬组(n=275)或安慰剂组(n=270)。患者为每周3次血液透析,且瘙痒强度中重度(基线WI-NRS>5)。治疗周期为12周,使用静脉注射安瑞克芬0.3μg/kg体重或等量安慰剂,透析后1小时内给药。12周双盲治疗结束后,符合条件的患者可进入40周开放标签延长期,接受安瑞克芬治疗。 主要终点为12周内达到WI-NRS评分减少≥4分的患者比例。次要终点包括至少3分的WI-NRS下降比例及瘙痒相关生活质量的改善,评估工具为Skindex-10和5-D瘙痒量表。安全性评估覆盖整个试验,包括不良事件监测、临床检查等。
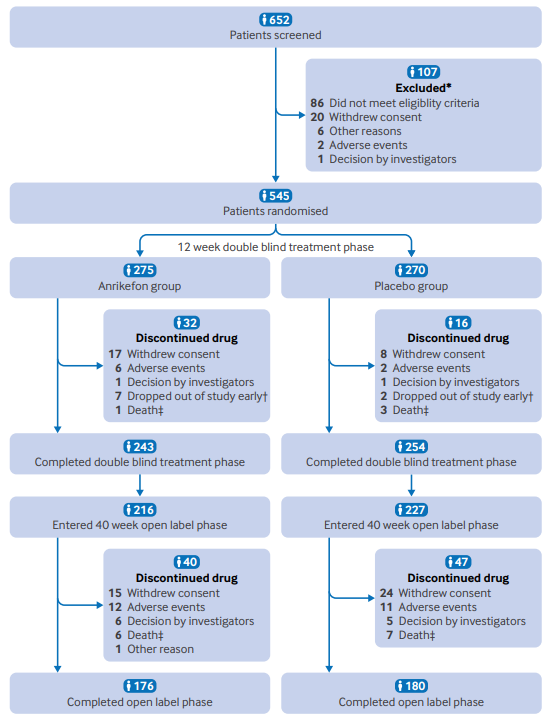
图:研究流程图
结果显示,12周双盲期完成率分别为安瑞克芬组88%和安慰剂组94%。安瑞克芬组达到主要终点的患者比例为37%,显著高于安慰剂组的15%(P<0.001,OR=3.56)。达到次要终点(WI-NRS下降≥3分)的患者比例为51%对比24%(P<0.001)。
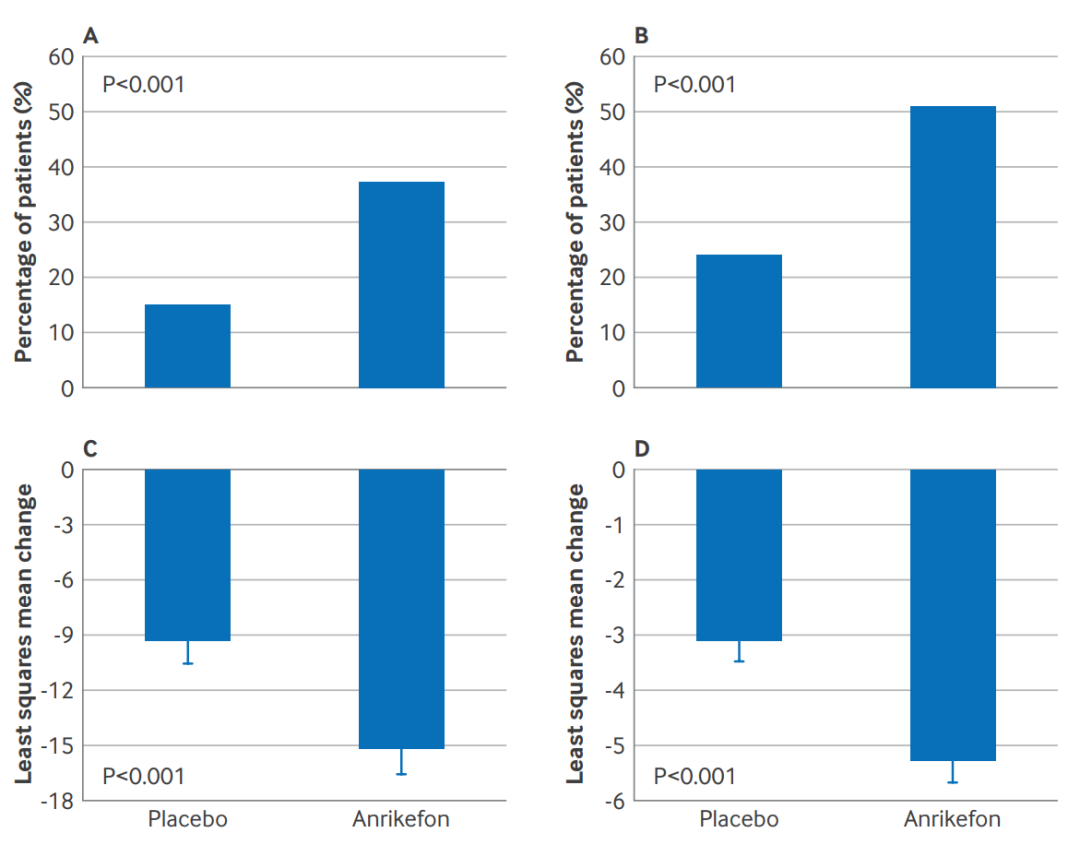
图A/B:双盲治疗期第12周WI-NRS的周平均值较基线改善≥4分/≥3分的受试者比例;图C/D:双盲治疗期第12周Skindex-10量表/5-D量表总分较基线变化
瘙痒相关生活质量在安瑞克芬组也显著改善,5-D瘙痒评分和Skindex-10评分的平均下降分别为5.3分和15.2分,优于安慰剂组(分别为3.1分和9.3分,P<0.001)。 40周开放标签延长期显示安瑞克芬疗效持续,患者5-D瘙痒评分持续改善。
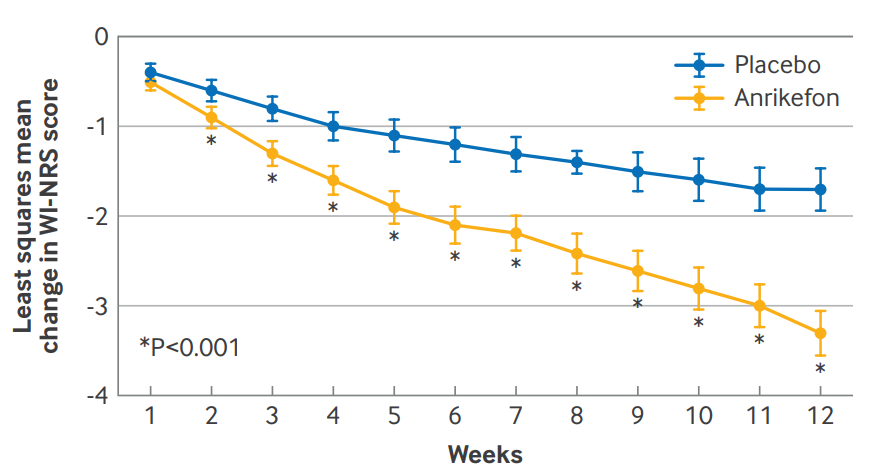
图:双盲治疗期 第1-12周WI-NRS的周平均值较基线的变化
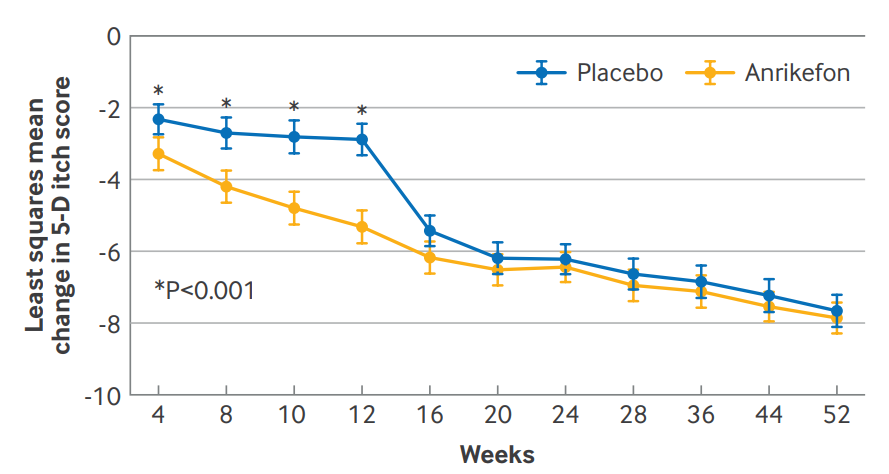
图:试验期间5-D量表总分较基线变化
在安全性方面,安瑞克芬主要相关不良事件为轻中度头晕,未见明显临床后果。严重不良事件发生率与安慰剂组相近,无癫痫、幻觉等中枢神经不良反应报告。
总之,本研究系统验证了安瑞克芬作为一种外周选择性κ-阿片受体激动剂,在血液透析患者中治疗慢性肾病相关中重度瘙痒的有效性与安全性。该药物通过靶向外周κ-阿片受体,避免了中枢神经系统相关不良反应,满足了临床亟需安全有效新药的需求。 长期开放标签数据支持其持续疗效和安全性,未见耐药或严重依赖性迹象,符合外周受体激动剂低滥用潜力的预期。 研究局限包括仅纳入血液透析患者,缺乏非透析CKD患者数据;未评估长期停药后的影响及依赖性风险;缺乏与现有活性药物的直接对比试验等。此外,开放标签延长期可能存在不良事件报告偏差。
原始出处
Bi-Cheng Liu,Zuo-Lin Li,Ping Zhang,et al.Efficacy and safety of anrikefon in patients with pruritus undergoing haemodialysis: multicentre, double blind,randomised placebo controlled phase 3 trial.http://dx.doi.org/10.1136/bmj-2025‑085208
猜你喜欢
- 纳米喷雾补水仪用什么水 补水仪适合哪些人补水
- 女生正确洁阴的5个基本方法
- 哀悼!连日来痛失4位知名医生!最小37岁,最大64岁!告别广东省中医院张北平教授,曾培养十多名三甲科主任!痛别瑞金烧伤专家陆树良
- 杨坤首部运动写真曝光 真实汗水展露男人坚毅态度
- 长沙市疾控中心专家提醒:冬季谨防一氧化碳中毒
- Molecular Neurodegeneration:Chitinase-3-like-1在神经炎症和退行性病理中的多面角色及其治疗意义
- 大家有没有想过通过登山减肥? 3大登山减肥小诀窍健身瘦身两不误
- 相克的7对食物和药物
- 杜蕾斯品牌 超薄冰火避孕套带起来什么感觉
- 秋季流感疫苗开打三价、四价如何选?
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)