首页 > 医疗资讯/ 正文
糖尿病视网膜病变(DR)是糖尿病常见的微血管并发症之一,其特征性病理改变是视网膜血管系统发生进行性损伤。这种血管病变可导致视网膜微循环障碍,若不及时干预,最终可能造成不可逆的视力损害甚至失明。早期通过眼底筛查发现并及时干预,可有效保留DR患者的视力,而晚期诊断往往会导致不可逆的视力丧失[1]。传统DR诊断依赖于眼科医生对眼底彩色照片的判读,这一过程不仅需要医生具备专业的眼底病学知识,还需承受巨大的工作压力。基层医疗机构中,全科医生和非眼科专科医师往往难以胜任这一专业性极强的诊断工作。
近年来,随着人工智能(AI)技术在医学影像分析领域取得突破性进展,为解决DR筛查提供了新的技术路径。基于深度学习的DR眼底图像辅助诊断软件(以下简称“AI-DR软件”)通过辅助分析眼底图像,显著提升了筛查效率和可及性[2-3]。高质量、标准化的数据集是此类技术的核心要素。为规范行业发展,我国已发布国产AI-DR软件相关注册审查指导原则[4-5],建立了多层次的标准体系:
1
基础性标准层面:发布了IEEE 2801-2022《医学人工智能数据集质量管理推荐标准》[6],指导制造商如何建立数据质量管理体系,为数据质量管理提供了框架性指导;
2
通用性标准层面:发布了YY/T 1833.2-2022《人工智能医疗器械 质量要求和评价 第2部分:数据集通用要求》(以下简称“YY/T 1833.2-2022”)[7]和YY/T 1833.3-2022《人工智能医疗器械 质量要求和评价 第3部分:数据标注通用要求》(以下简称“YY/T 1833.3-2022”)[8],提出了数据集的描述文档要求、质量特性与评价方法以及数据标注的质量特性、流程和工具要求,明确了人工智能医疗器械数据集的通用要求;
3
专用性标准层面:发布了YY/T 1949-2024《人工智能医疗器械 数据集专用要求:糖尿病视网膜病变眼底彩照》(以下简称“YY/T 1949-2024”),首次针对DR眼底图像数据集制定了专项技术要求,以指导具体临床方向的数据集质量评价,引导临床机构从源头加强数据集的质控。该标准参考了国内数据集质量评价[8]、数字眼科[9]、DR数据集建设[10-11]、远程眼底筛查[12]等相关领域的技术现状,有助于帮助眼科领域的数据集制造责任方(包括医院、体检机构、科研机构、医疗器械厂家、检测机构、监管机构、卫生技术评估机构等)建立统一的眼底彩照数据集的产品技术要求,为数据集的交付验收、内部质控提供依据,将在人工智能医疗器械厂家的进货检验、供应商资质审核、内部数据集质量管理等环节发挥作用。
上述标准体系的建立为医疗机构、研发企业和监管部门提供了统一的技术规范,亦推动了DR筛查技术的规范化和标准化应用。
本文对YY/T 1949-2024行业标准中的核心内容进行系统解读,重点分析标准中关于数据集描述文档、质量特性指标以及评价方法等关键技术要求,旨在指导相关机构建立规范的DR眼底彩照数据集建设流程,提升高质量医学数据集的供给水平,为DR人工智能医疗器械的全生命周期管理(包括研发验证、性能测试、临床评价、上市后监管、再评价及真实世界研究等环节)提供标准化数据支持,提升AI-DR产品的安全性和有效性。
1 数据集描述文档要求解读
数据集描述文档作为数据集质量管理的核心文件,由数据集制造责任方负责编制,旨在向监管部门、研发机构以及终端用户全面披露数据集的关键信息,是评估数据集透明度的重要依据。YY/T 1949-2024标准沿用了YY/T 1833.2-2022关于数据集描述文档的一般要求,并进行了专业化规范,其内容体系包含基础属性描述(数据模态、数据层次、应用场景)、质量控制要求(数据采集、数据预处理、标注规范)、技术特征指标(数据元、元数据、数据更新)、临床适配性(数据多样性)以及依从条件、规则和规范。值得注意的是,该标准在数据层次、标注规范、数据采集等方面紧密参考了相关临床指南和共识,充分体现了AI-DR产品的临床特点,为构建符合真实诊疗场景的高质量数据集提供了系统化指导框架。
1.1 数据层次
数据层次是检索数据、抽取数据、划分子集的主要依据,能反映数据的多样性。YY/T 1949-2024给出了数据层次描述的三个维度:
1 图像分类:眼底图像可分为正常眼底彩照、不同DR诊断分期或筛查分级、易混淆的其他疾病病种、激光治疗后眼底图像改变、技术性废片等,这些均可作为数据分层的考虑因素。
2 病灶特征:DR是糖尿病引发的视网膜血管微循环障碍,早期可出现视网膜微血管瘤、出血、渗出、水肿;随着病情进展,血管变化更为明显,视网膜缺血、缺氧愈加严重,形成大量新生血管,上述病灶特征也是数据分层考虑的因素。
3 数据来源:《糖尿病视网膜病变眼底图像辅助诊断软件注册审查指导原则》中明确此类产品的核心功能是采用深度学习等人工智能算法,对由眼底相机(采用照相技术用于眼底摄影成像的常规眼底照相机,不包括激光、荧光等特殊方式的眼底相机)拍摄的眼底彩照进行分析,并给出进一步就医检查的建议。数据来源相关信息还包括拍摄眼底图像的眼底相机型号、机构类型和应用场景等,这些都是数据集描述的重要因素。值得一提的是,YY/T 1949-2024明确要求描述数据集的临床适用场景(包括社区DR筛查、体检中心DR筛查、医疗机构门诊/住院/急诊),旨在提醒数据集制造责任方根据场景判断数据样本分布是否合理,例如体检中心提供的正常眼底彩照比例应显著高于医院门诊。
该分层体系分别对应了AI-DR软件的辅助分类功能、辅助检出功能、泛化能力,与AI算法的训练、测试需求形成了衔接,便于后续在测试阶段抽取不同子集,评估算法处理不同患者亚组的性能差异。这一体系既满足了AI模型开发的数据多样性需求,又确保了数据分层的临床合理性和技术可操作性,为构建具有临床代表性和技术可靠性的AI-DR训练数据集提供了标准化框架。
1.2 数据集标注解读
数据集说明应描述数据集标注的内容、规则和流程,描述标注规则所参考的DR临床指南、专家共识或参考文献,在设计标注规则时应充分考虑我国DR相关诊疗指南及方案[13-15]。YY/T 1949-2024明确给出了数据集标注信息的3个维度,系统规范了DR眼底图像数据的标注要求:
1 图像总体标注:应包括DR病变严重程度分期或分级、是否转诊、其他眼底疾病、图像质量分级、眼别、治疗标记(激光斑识别与分级);
2 病灶标注:应包括病灶编号、病灶区域、中心点坐标、边界坐标、病灶类型(微血管瘤/出血灶/渗出灶等);
3 病历标注:应包括视力、血糖、糖尿病分型、糖尿病家族史、眼底病变诊疗史。数据集元数据应包含患者标识、性别、出生年月、糖尿病家族史等必要信息,宜包含视力、血糖、糖尿病分型、眼底病变诊疗史等信息。
图像总体标注和病灶标注的划分,同样对应AI-DR软件的辅助分类功能、辅助检出功能,为AI算法的训练及测试提供了参考标准。病历标注一方面体现了患者多样性,另一方面为多模态(例如图像+文本)AI-DR软件的训练、测试提供了参考标准,具有一定的技术前瞻性。
YY/T 1949-2024在资料性附录B中对数据标注流程进行举例,包括标注医师/仲裁专家资质、人员培训与分工、检出与分类标注步骤、标注细则、标注医生之间的一致性检验等,可为数据集制造责任方提供参考。阅片流程示例参见图1,图片来源为附录B。
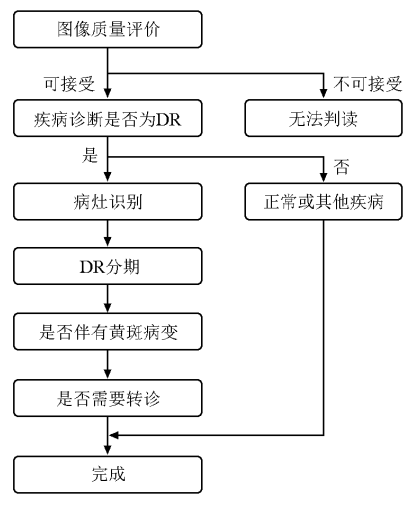
图1 阅片流程示例
DR:糖尿病视网膜病变
1.3 数据采集要求解读
DR眼底彩照是使用眼底照相机获取的数字化彩色眼底病变照片,人员、设备以及采集过程均会影响图像质量,在数据采集过程中需要严格把控。YY/T 1949-2024通过规范性附录A对数据采集全过程建立了严格的质量控制体系,具体包括以下关键要素:
1 采集人员资质要求:采集人员应为专业医疗人员,接受过医院的安全和标准作业流程培训,并在操作规范性、娴熟度、稳定度三方面接受考核。
2 采集设备技术要求:采集设备应获得医疗器械注册证,且符合眼底照相机相关标准[16]以及附录A的要求,内置固视点至少涵盖黄斑、视盘、黄斑-视盘连线中心;可支持无损压缩的tiff、jpg、png以及dicom格式。
3 拍照视野要求:拍摄单视野时,视场角应≥45°,拍摄多视野时,视场角应≥30°,单个病例的图像需覆盖黄斑和视盘。
4 图像质量要求:采集图像时应避免进行有损压缩。图像要求对焦准确,视盘表面、视网膜主干血管、视网膜分支血管、黄斑中心凹、视网膜病变等结构均应清晰可辨,避免虚化;眼底图像曝光适度,避免视盘苍白、后极部视网膜反光增强等现象。
出现以下情况需重新采集:光学系统或镜头污迹、睫毛/毛发虚影、周边黄色边缘、漏光样边缘或水滴样反光带。质量达标的图像示例参见图2,图片来源为公开数据集[17]。
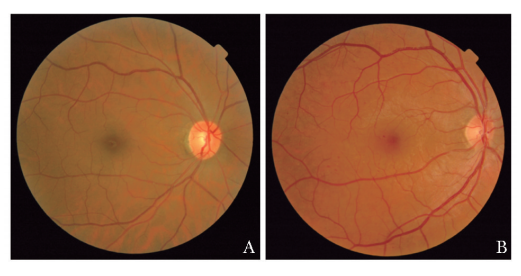
图2 质量达标图像示例(2240×1488)[17]
A.拍摄时对准黄斑-视盘连线中心;B.拍摄时对准黄斑中心
2 质量特性指标解读
YY/T 1949-2024沿用了YY/T 1833.2-2022的质量特性定义,在准确性、完备性、一致性、可理解性、代表性五个方面强调了DR眼底彩照的特色。
2.1 准确性
DR眼底彩照数据集的准确性指标由数据集制造责任方提供,并写入数据集描述文档,包括以下6个层面:
1 设备资质验证:采集设备应使用具有医疗器械注册证、处于有效期内的彩色眼底照相机,YY/T 1949-2024在附录A(数据采集要求)中对眼底相机的光学参数和功能给出了详细规定;
2 人员资质管理:提出了眼底相机操作人员培训、考核、操作规范要求,以及拍摄质量标准(参照附录A);
3 数据信息准确性:每张眼底彩照与受试者的个人信息和病历资料应准确对应;
4 文档规范要求:数据集说明使用的名词术语以及文档内容应准确、清晰、无歧义;
5 标注质量控制:以仲裁人员的标注结果作为参考标准,标注人员的准确率应满足诊断分类准确率≥ 80%、临床分期准确率≥70%、转诊指征判断准确率≥80%、病灶平均分割交并比≥70%;
6 病历资料标准化:若采集DR患者病历资料,其中所涉及的描述性文字应严格遵循WS/T 305《卫生健康信息数据集元数据标准》[18]。
其中上述(1)~(4)、(6)对DR数据采集环节提供了全方位规范,涉及设备、人员、操作、信息录入,而(5)旨在提醒数据集制造责任方加强对初级标注人员的考核。在数据集实际建设过程中,为降低标注成本和提高效率,标注任务的审核与仲裁环节可能无法覆盖全体样本,在此情况下,初级标注人员的准确性、一致性对最终标注结果的质量具有决定性作用,此类人员的水平与审核、仲裁专家越接近,则最终标注结果的准确性越有保证。
2.2 完备性
图像采集方面,YY/T 1949-2024要求图像包含黄斑和视盘,为数据标注提供基础信息;数据标注方面,YY/T 1949-2024要求标注结论包含“是否转诊”和临床分期,以适配算法训练、测试的常见需求;元数据采集方面,YY/T 1949-2024要求执行WS/T 305,与医院电子病历系统作好衔接。
2.3 一致性
DR眼底彩照数据集的一致性,首先表现为采集、预处理、标注方法的一致性。在多中心、多机构建库的场景下,意味着需要建立统一的操作规程,图像命名、眼别、编号、视野描述等细节同样需保持统一。在数据标注层面,则需考核不同标注人员之间的一致性,常用指标为Kappa系数。
2.4 可理解性
可理解性要求数据集制造责任方对标注结果给出充分的注释,例如提供DR标注的标签与临床分期、分级及病灶的对应关系,说明标注结果中各空间坐标的含义,说明如何使用标注结果来评估标注人员的一致性、准确性,如采用辅助标注算法需说明该算法的性能指标与评价方法。
2.5 代表性
YY/T 1949-2024对DR眼底彩照数据集中的患者来源、病种组成等细节进行了规定:
1 患者来源方面,应包含3个及以上的地理区划(华中、华北、华东、华南、西北、西南、东北);
2 数据来源方面,若AI-DR软件预期用于辅助筛查,数据来源70%以上应为体检机构或社会筛查;若AI-DR软件预期用于辅助诊断,数据来源70%以上应为医院;
3 病种组成方面,数据集应同时包含Ⅰ型、Ⅱ型糖尿病患者经手术、眼内激光治疗后的DR眼底彩照,并对正常眼底、不同DR分期、其他非DR眼病的比例进行了推荐。
3 标准实施评价解读
3.1 抽样检验差异
YY/T 1949-2024提出的数据集质量评价流程与YY/T 1833.2-2022基本一致,但在抽样检验方面存在显著差异。在YY/T 1949-2024第6章中,根据图像样本总量直接给出对抽样比例或数量的具体要求,不再由数据集制造责任方按照GB/T 2828.4等监督抽验标准[19]进行估算,简化了总体工作量且有助于直接比较不同DR眼底彩照数据集的指标。
3.2 测试验证
YY/T 1949-2024规定了用于AI医疗器械的DR眼底彩照数据集的专用要求和试验方法,在标准制定过程中进行了资料验证和试验验证,这些验证工作一方面论证了标准要求的可行性和方法的可靠性,另一方面也为AI-DR产品上市前后的第三方测试提供依据及技术支持,为AI-DR产品的质量评价指明了方向。
在数据集建设阶段,医院、科研机构、检测机构等主体应按照可追溯的要求,加强对数据采集人员、标注人员的培训及考核,对数据标注工具、数据预处理工具、数据库软件的管理,形成完备的过程记录。
由于DR数据集是AI-DR软件开展算法测试的质控品,医疗器械检测机构在开发测试集的同时,应按照本标准要求对测试集进行评价,并实时关注其管理与更新。
4 小结
高质量数据集作为AI医疗器械研发的核心要素,质量稳定可靠至关重要。YY/T 1949-2024行业标准的实施,为AI-DR医疗器械全生命周期管理提供了统一标准,通过建立覆盖研发、测试、临床质控、上市后监管的质量评价体系,可显著降低不同机构间的质量评价差异,增强此类产品的可比性。此外,该标准的实施有利于整合行业资源,促进多中心合作与数据共享,加速眼科AI辅助诊断技术的创新迭代,提升DR筛查的准确性,为患者提供更好的医疗服务。在该标准的引领下,数据集制造责任方应协同合作,共同应对市场挑战,推动AI产业的高质量发展。
参考文献
[1]中华医学会眼科学分会眼底病学组, 中国医师协会眼科医师分会眼底病学组. 我国糖尿病视网膜病变临床诊疗指南(2022年)[J]. 中华眼底病杂志, 2023, 39(2): 99-124.
[2]Dai L, Sheng B, Chen T L, et al. A deep learning system for predicting time to progression of diabetic retinopathy[J]. Nat Med, 2024, 30(2): 584-594.
[3]Li J J, Guan Z Y, Wang J, et al. Integrated image-based deep learning and language models for primary diabetes care[J]. Nat Med, 2024, 30(10): 2886-2896.
[4]国家药品监督管理局医疗器械技术审评中心. 国家药监局器审中心关于发布人工智能医疗器械注册审查指导原则的通告(2022年第8号)[EB/OL]. (2022-03-09)[2025-05-04]. https://www.cmde.org.cn//xwdt/shpgzgg/gztg/20220309090800158.html.
[5]国家药品监督管理局医疗器械技术审评中心. 国家药监局器审中心关于发布糖尿病视网膜病变眼底图像辅助诊断软件注册审查指导原则的通告(2022年第23号)[EB/OL]. (2022-06-02)[2025-05-04]. https://www.cmde.org.cn//xwdt/shpgzgg/gztg/20220602103048151.html.
[6]IEEE. IEEE recommended practice for the quality management of datasets for medical artificial intelligence: IEEE 2801-2022[S]. Piscataway: IEEE Press, 2022.
[7]王浩, 孟祥峰, 郝烨, 等. 行业标准《人工智能医疗器械质量要求和评价第2部分: 数据集通用要求》解析[J]. 协和医学杂志, 2023, 14(6): 1180-1184.
[8]郝烨, 王浩, 李佳戈. 行业标准《人工智能医疗器械质量要求和评价第3部分:数据标注通用要求》解析[J]. 协和医学杂志, 2023, 14(6): 1185-1188.
[9]魏文斌, 李赫妍, 董力. 重视数字眼科在眼科学发展中所发挥的重要作用[J]. 中国医学前沿杂志(电子版), 2023, 15(6): 4-9.
[10]杨爱平, 史芳, 蒋薇, 等. 医学标准数据库建设思路及应用研究[J]. 中国高新科技, 2024(10): 158-160.
[11]于伟泓, 张潇, 吴婵, 等. 糖尿病视网膜病变眼底彩照人工智能研究标准数据库的建立规范[J]. 协和医学杂志, 2021, 12(5): 684-688.
[12]张潇, 陈有信. 眼科远程医疗发展现状与前景[J]. 协和医学杂志, 2021, 12(5): 755-760.
[13]中华医学会眼科学会眼底病学组. 我国糖尿病视网膜病变临床诊疗指南(2014年)[J]. 中华眼科杂志, 2014, 50(11): 851-865.
[14]中华医学会眼科学分会眼底病学组, 中国医师协会眼科医师分会眼底病专业委员会. 我国糖尿病视网膜病变筛查的图像采集及阅片指南(2017年)[J]. 中华眼科杂志, 2017, 53(12): 890-896.
[15]中华预防医学会公共卫生眼科学分会. 中国糖尿病视网膜病变远程医疗专家共识(2023年)[J]. 中华眼科杂志, 2023, 59(11): 870-879.
[16]国家药品监督管理局. 眼科仪器 眼底照相机: YY/T 0634-2022[S]. 北京: 中国标准出版社, 2022.
[17]Decencière E, Zhang X W, Cazuguel G, et al. Feedback on a publicly distributed image database: the Messidor database[J]. Image Anal Stereol, 2014, 33(3): 231-234.
[18]中华人民共和国国家卫生健康委员会. 卫生健康信息数据集元数据标准: WS/T 305-2023[S]. 北京: 中国标准出版社, 2023.
[19]全国统计方法应用标准化技术委员会. 计数抽样检验程序 第4部分: 声称质量水平的评定程序: GB/T 2828.4-2008[S]. 北京: 中国标准出版社, 2008.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)