首页 > 医疗资讯/ 正文
胶质瘤是一种侵袭性脑肿瘤,预后不良。建立一种能够精确复制原发肿瘤细胞组成和微环境的体外培养模型一直颇具挑战性,限制了其临床应用。
2025年 7 月 14 日,首都医科大学保肇实、北京大学郑乐民、首都医科大学江涛、张颖和Chen Qiaodong 共同通讯在Bioactive Materials 在线发表题为“A novel organoid model retaining the glioma microenvironment for personalized drug screening and therapeutic evaluation”的研究论文。该研究提出了一种从患者来源的胶质瘤组织中生成具有微环境的胶质瘤类器官(GlioME)的新方法。这些类器官保留了原发肿瘤的遗传和表观遗传特征,并保留了肿瘤微环境中细胞间相互作用,包括驻留免疫细胞。
利用批量RNA测序、全外显子组测序和DNA甲基化分析来确认类器官与原发性胶质瘤组织之间的分子相似性。免疫荧光和流式细胞术用于评估免疫细胞活力,并将GlioME与漂浮胶质瘤类器官进行比较。GlioME对化疗和靶向治疗表现出较高的反应性,展现出其在治疗筛选应用中的潜力。值得注意的是,GlioME准确预测了患者对近期获批的MET抑制剂维布雷替尼的反应。因此,该类器官模型为胶质瘤微环境相关研究和临床药物筛选提供了一个可靠的体外平台。

神经胶质瘤是最常见的恶性脑肿瘤,具有侵袭性和不良预后的特点。尽管放疗和化疗取得了进展,但神经胶质瘤患者的五年生存率仍然很低。一个重大挑战是缺乏能够准确复制人类神经胶质瘤的肿瘤微环境和细胞异质性的实验模型,这限制了对疾病机制的理解和有效疗法的开发。
目前的实验模型包括细胞系、患者来源的细胞系 (PDC) 和患者来源的肿瘤异种移植 (PDTX)。然而,细胞系无法代表原始肿瘤的复杂性,而 PDC 过于简单,缺乏肿瘤组织的结构和生理特征。此外,研究表明原发性肿瘤细胞和原始肿瘤细胞之间存在差异。PDTX 模型虽然有用,但建立耗时、成功率低,并且不能复制免疫系统。患者来源的肿瘤类器官最近已成为有前途的三维体外系统。这些类器官可以在短时间内从小组织样本中建立,同时保留原始肿瘤的组织病理学和基因组特征。目前已经开发出几种胶质母细胞瘤类器官模型。研究人员使用患者的肿瘤碎片并采用漂浮培养方法来创建可在体外传代的患者来源的胶质母细胞瘤类器官。其他人则使用酶消化将肿瘤组织分解成单个细胞,然后在 Matrigel 中培养,使肿瘤细胞自发形成类器官结构。此外,一些研究人员使用人类诱导多能干细胞 (iPSC) 结合 CRISPR-Cas9 技术来敲除 PTEN 和 TP53 等基因,从而产生胶质母细胞瘤样类器官。尽管取得了这些进展,复制体内肿瘤微环境仍然具有挑战性。漂浮培养的类器官会随着时间的推移而丢失免疫细胞,而酶消化会破坏肿瘤内复杂的细胞相互作用。源自iPSC的类器官缺乏非肿瘤成分。这些局限性使得这些模型无法保留原始的肿瘤微环境,从而限制了其在胶质母细胞瘤研究中的应用。迄今为止,尚未开发出能够在类器官模型中完全保留胶质母细胞瘤微环境的方法。
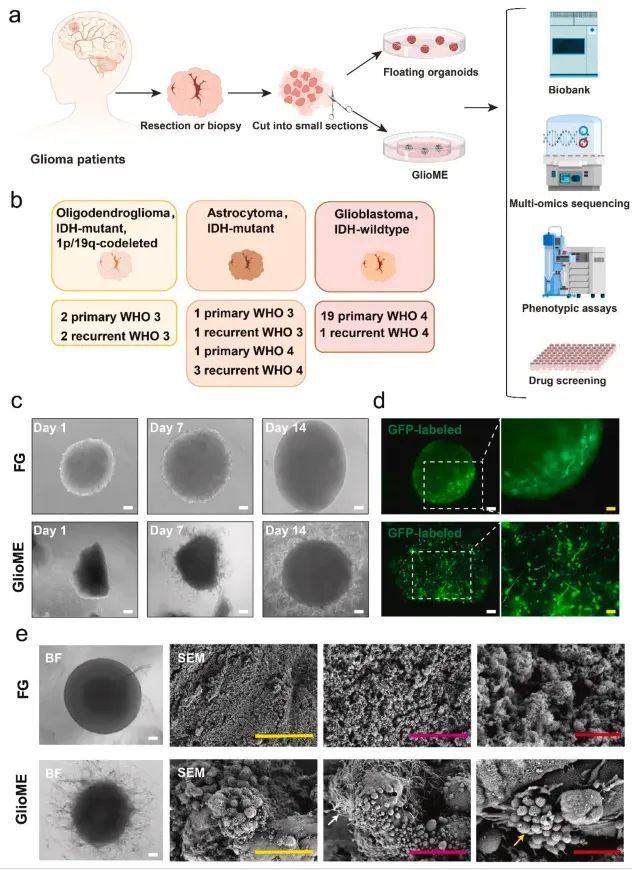
图1 Establishment and morphological characterization of floating organoids and glioma organoids with microenvironment (GlioME).(图源自Bioactive Materials )
为了解决这些局限性,作者构建了保留肿瘤免疫微环境的胶质瘤类器官。全面的组织学、分子和遗传学分析证实,这些类器官与原始肿瘤非常相似,保留了关键的生物标志物、相似的免疫细胞和基质细胞比例,以及肿瘤组织和细胞的异质性。作者还将该方法与另一种使用患者来源的肿瘤碎片构建胶质瘤类器官的方法进行了比较,这种方法无需单细胞分离即可构建。此外,还探索了药物筛选应用,证明这些类器官能够进行高通量药物测试,凸显了它们在维持肿瘤免疫微环境以用于治疗研究方面的潜在重要性。
原文链接:
https://www.sciencedirect.com/science/article/pii/S2452199X25003081
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)