首页 > 医疗资讯/ 正文
编者按
2025年世界肝炎日宣传大会暨第七届慢乙肝临床治愈学术大会于7月19日在北京隆重召开,会议主题为“聚中国智慧 飞跃慢乙肝临床治愈新高峰”。
免疫重建是乙肝临床治愈的核心所在,如何有效实现?来自北京大学医学部的鲁凤民教授以“免疫重建治愈慢性乙肝的问题与挑战”为主题,阐述了慢性乙肝临床治愈的主要障碍并提出了对策建议。肝霖君与您分享精彩内容。

从全国血清HBsAg流行率的研究发现,围产期的感染慢性化率大于90%,婴幼儿期的慢性化率大于20%。EASL 2025指南建议成功阻断母婴垂直传播的婴幼儿,儿童时期可能还需要加强免疫。目前我国慢乙肝患者数量仍然庞大,由HBV所致的肝硬化、肝癌的比例分别约为77%和84%。
一 慢性乙肝自愈/治愈的主要障碍
长期持续炎症下肝细胞的死亡与再生——肝脏免疫病理改变
免疫耐受打破后,宿主的抗HBV免疫通过清除感染肝细胞逐渐降低感染肝细胞的数量,cccDNA池显著下降,残存cccDNA因表观遗传修饰转向转录沉默。慢乙肝患者持续的高水平抗原暴露导致HBV特异性免疫细胞耗竭、免疫应答受损,因此HBsAg自发清除率低,持续的肝损伤累积可能导致肝硬化、肝癌的发生。
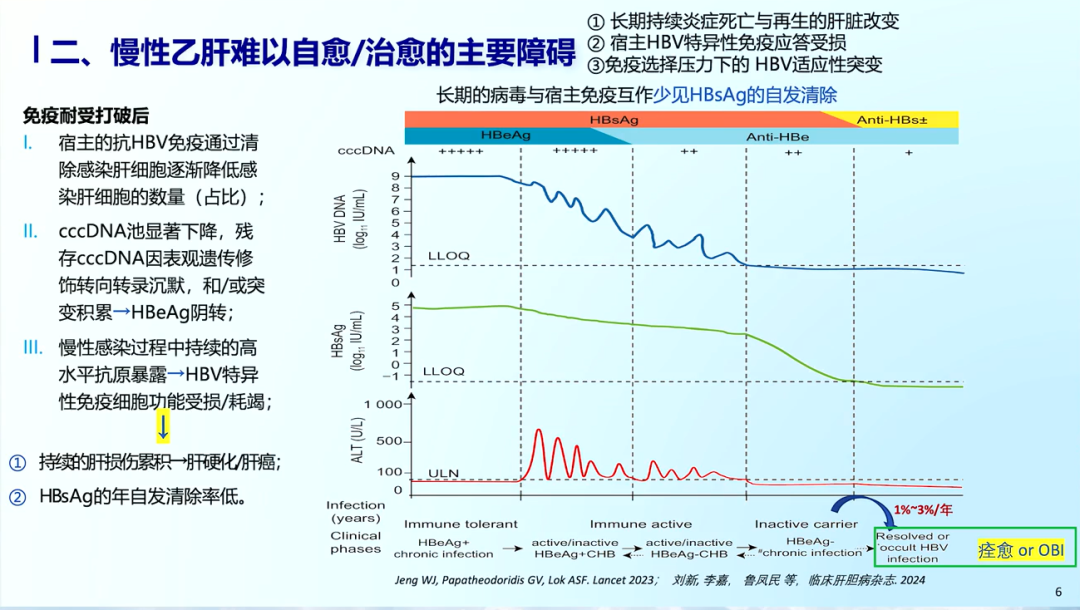
长期高水平病毒抗原暴露诱发宿主HBV特异性免疫应答受损
宿主抗HBV特异性细胞免疫活性随年龄变化。在总的HBV特异性细胞毒性T细胞(CTL)中,3 - 24岁慢乙肝患者的HBs-CTL比例> 30% - 40%,经长时间、持续高水平暴露下的功能耗竭后,下降到35岁以上患者的HBs-CTL比例< 5%。慢性HBV感染者无法形成有效的抗HBV特异性免疫应答的原因可能在于HBe/core由Kupffer细胞提呈,将CD8+ T细胞致敏并激活为效应性T细胞;HBeAg阴转后,HBe/core由肝细胞提呈,CD8+ T细胞虽能被局部激活并增殖,但不会进一步分化为效应细胞。
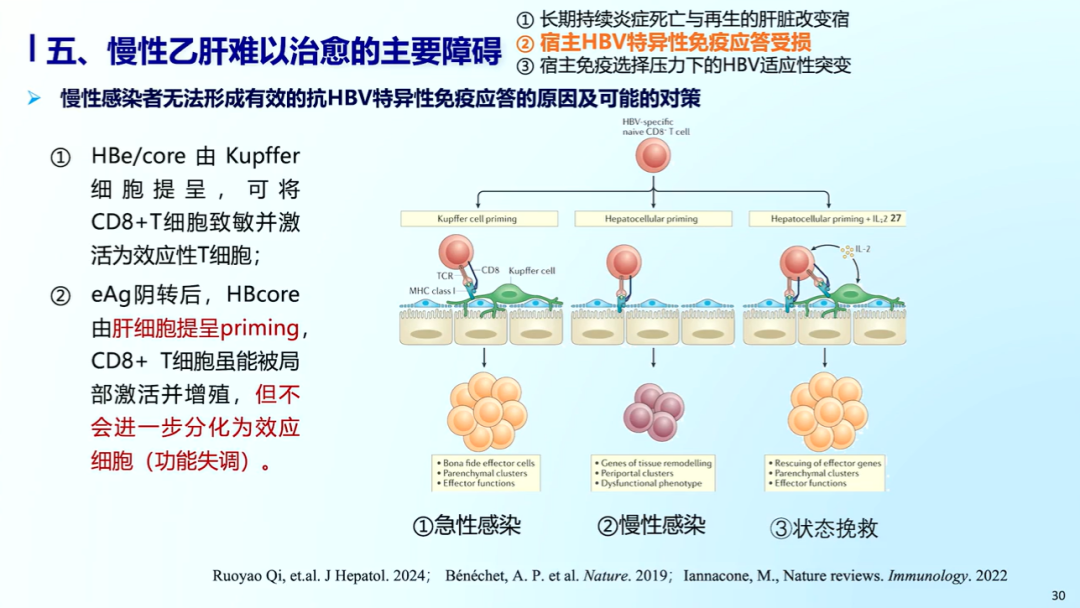
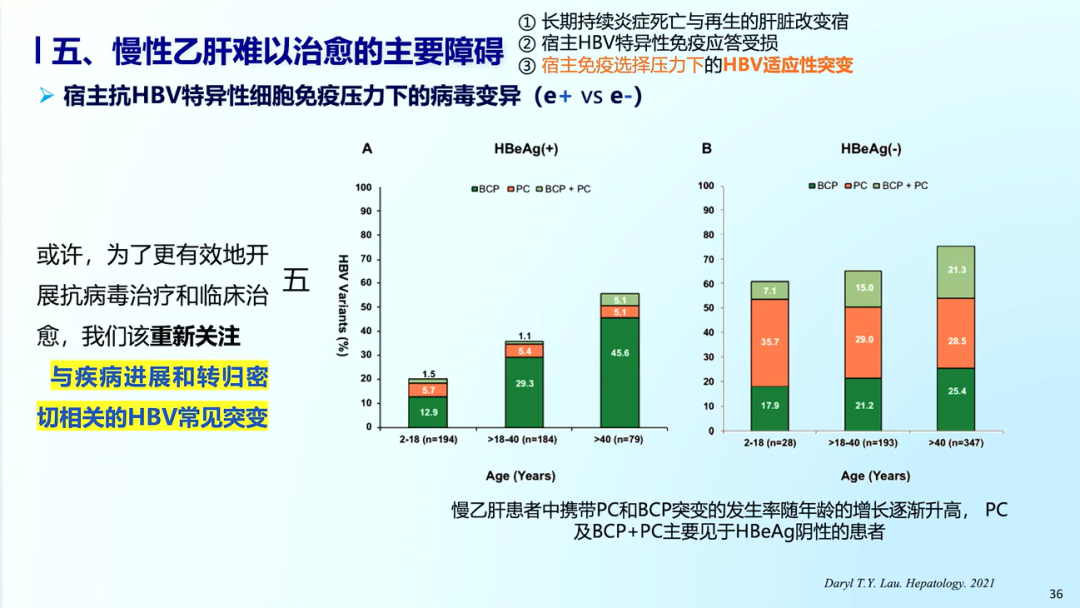
宿主免疫选择压力下的HBV适应性突变
研究发现CP/BCP突变使HBeAg表达减少或消失,以逃逸宿主免疫;另外促进HBV复制和稳定cccDNA池,导致慢性感染维持。另外,HBV可通过抗原表位突变、逃避CD8+ T细胞的识别,HBV-core的突变频率(71.9%)高于其他抗原,这表明HBV-core是宿主HLA-I免疫压力的主要靶点。HBV的适应性进化能力、与低病毒载量和低HBsAg水平显著负相关,这提示有效的免疫压力可通过限制病毒复制降低其进化潜能。
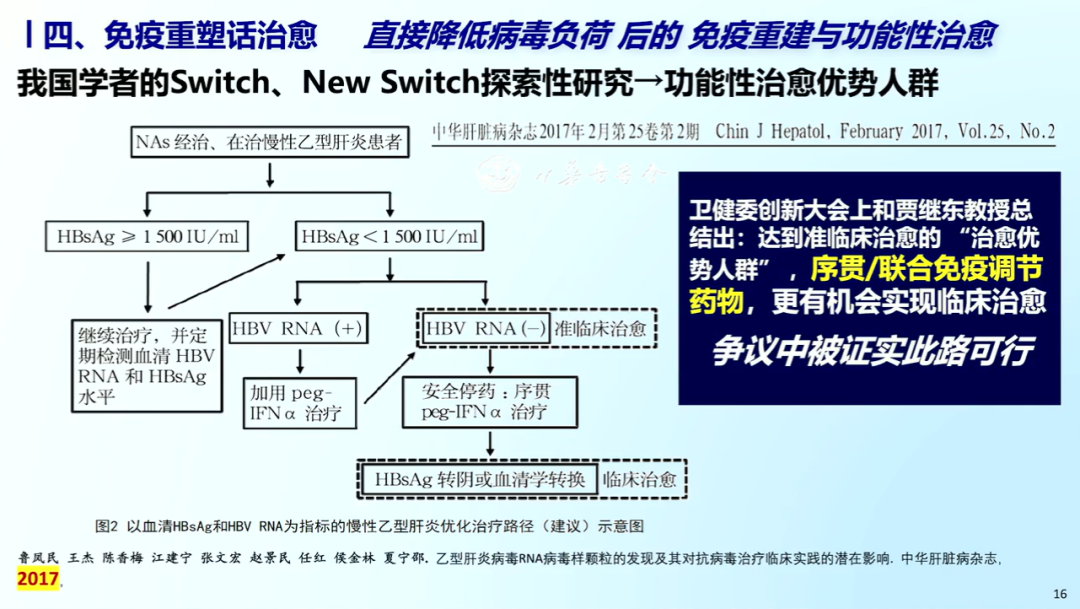
二 免疫重建与慢乙肝临床治愈
NAs类药物可阻断HBV DNA复制、逆转录,但对病毒蛋白抗原的表达几乎没有影响,对整合源头的HBsAg无直接作用,研究发现长时间的NAs治疗极少带来慢乙肝患者的临床治愈。SWITCH、NEW SWITCH研究表明NAs经治慢乙肝患者通过序贯或联合使用PEG IFNα治疗,更有可能实现临床治愈。2022版《慢性乙型肝炎防治指南》推荐> 30岁慢乙肝患者接受抗病毒治疗,对于优势人群可加用PEG IFNα以追求临床治愈。
“珠峰”项目数据表明慢乙肝患者接受PEG IFNα治疗可获得较高的HBsAg清除率,基线HBsAg水平越低,患者的HBsAg清除率越高,HBsAg ≤ 100 IU/mL的患者48周HBsAg清除率达56.1%,其中部分患者没有治愈,可能与宿主对干扰素的负反馈机制有关。
相比未获得临床治愈的慢乙肝患者,临床治愈患者免疫重建的标志之一是Pol、HBs特异性CTL显著增加。免疫重塑有助于实现慢乙肝临床治愈,可通过激活宿主抗HBV特异性细胞免疫应答进行免疫重塑,如HBV特异性CD8+ T细胞的复现或新现等。
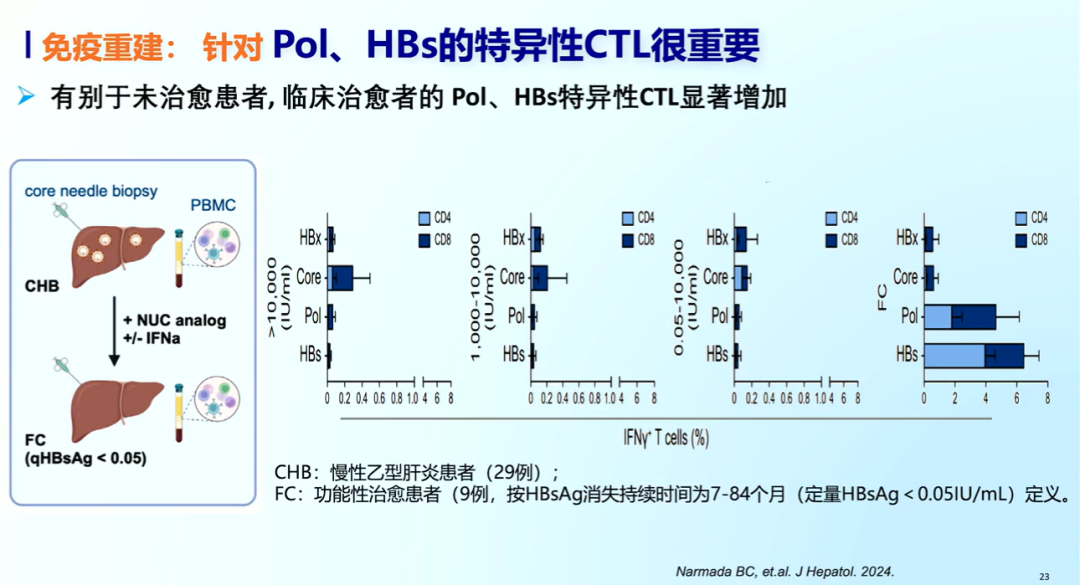
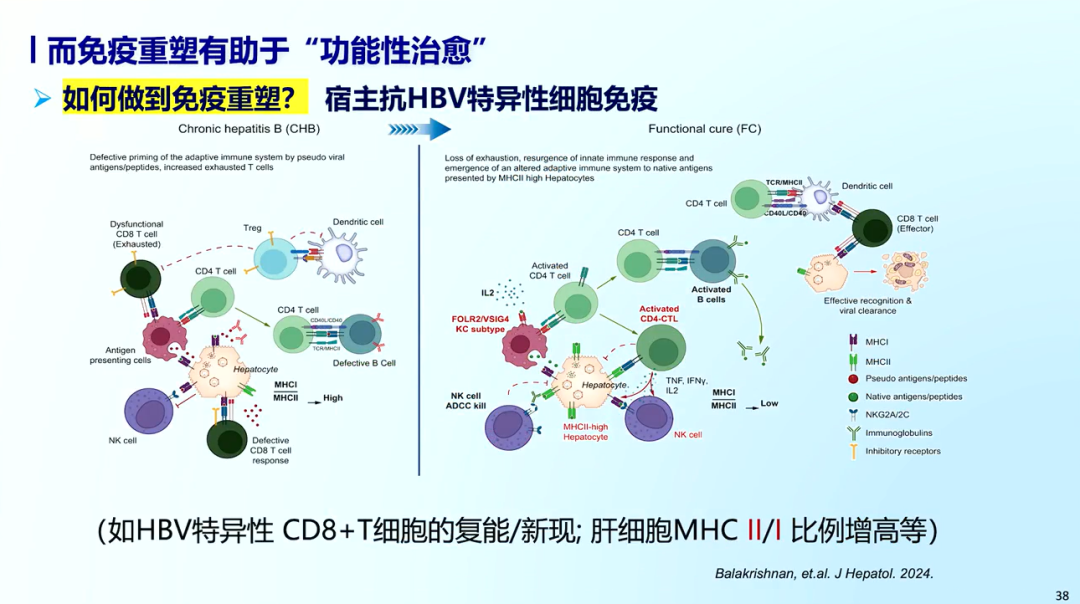
三 联合PEG IFNα等免疫调节药物,以追求临床治愈
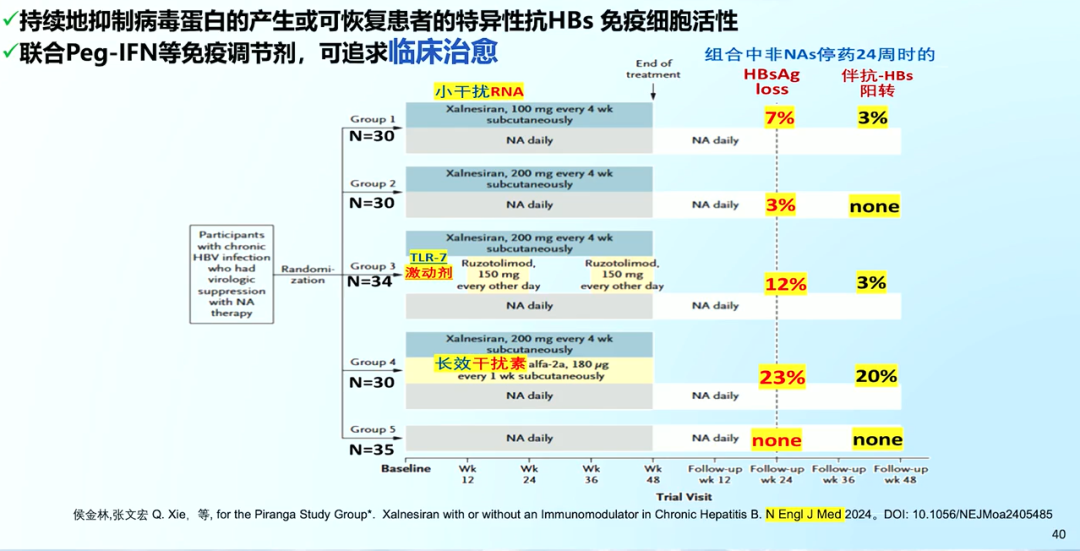
单用直接抗病毒药物(DAAs)难以带来治愈,需要改变依赖单一抗病毒药物的传统思维,联合PEG IFNα等免疫调节药物,以有效地激活或修复受损的免疫应答,使其能够协同作用,共同奔向慢乙肝临床治愈。

- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)