首页 > 医疗资讯/ 正文
双硫死亡是一种新型的受控细胞死亡方式,它涉及由于过量二硫键形成而导致的细胞骨架崩塌,将代谢和活性氧与潜在的癌症治疗靶点联系起来。近期的多组学研究强调了双硫死亡相关基因 (DRG) 特征在泛癌症中的预后价值;然而,其生物学功能和治疗相关性背后的分子机制仍不甚明了。
2025年7月25日,复旦大学附属中山医院Xu Xiao、广州医科大学附属中医医院刘丹、同济大学附属东方医院翟博、复旦大学附属中山医院Huang Jianfeng、同济大学附属东方医院宋振宇共同通讯在Advanced Science 在线发表题为“Glucose Deprivation-Induced Disulfidptosis via the SLC7A11-INF2 Axis: Pan-Cancer Prognostic Exploration and Therapeutic Validation”的研究论文。该研究利用 LASSO Cox 回归构建了涵盖 33 种癌症类型的 DRG 评分模型,并开发了包含 DRG 评分的列线图用于预后预测。
此外,还分析了肿瘤微环境、突变谱和免疫治疗反应。DRG 评分是跨癌症的独立预后因素,与不良预后和恶性特征相关。葡萄糖缺乏会诱导 SLC7A11high 细胞(SLC7A11 高表达)发生双硫死亡,尤其是在 DRG 评分高的癌症中,例如卵巢癌。沉默INF2可阻止双硫死亡并降低对伊罗夫文的敏感性,而这种敏感性可通过GLUT抑制剂逆转。SLC7A11敲低可降低双硫死亡,恢复ATP/NADPH水平,并在葡萄糖缺乏的情况下保护细胞骨架,而INF2敲低则会损害细胞迁移。此外,背根节评分可预测预后和治疗反应。SLC7A11-INF2轴调节双硫死亡、迁移和药物敏感性,突显了其作为卵巢癌代谢易感性标志物的潜在价值。

癌症仍然是全球死亡的主要原因,2024年美国新增病例超过200万,死亡人数超过60万。尽管治疗手段的进步提高了某些癌症患者的生存率,但包括卵巢癌(OV) 在内的许多恶性肿瘤的长期预后仍然不佳。作为典型的难治性妇科肿瘤,OV仍然是临床关注的焦点。它在美国女性癌症相关死亡率中排名第六,全球排名第八,晚期患者的5年生存率仅为约30%。标准的OV治疗包括肿瘤细胞减灭手术和随后的铂类化疗,并使用PARP抑制剂(如尼拉帕尼)进行维持治疗,无论同源重组状态如何,都能提供无进展生存获益。然而,大多数患者最终都会复发,治疗耐药性仍然是一个主要障碍。这些局限性凸显了对更持久、肿瘤特异性更强的OV治疗策略的迫切需求。治疗耐药性越来越多地与肿瘤细胞以外的因素相关,包括肿瘤微环境 (TME)。展望未来,未来的癌症治疗将越来越依赖于整合分子分析和代谢靶向,以解决特定情况下的脆弱性。
在这种治疗背景下,“双硫死亡”——一种新型的受调控细胞死亡形式——于2023 年首次被描述,其涉及葡萄糖缺乏条件下二硫化物应激诱导的细胞骨架崩塌。双硫死亡受一系列分子通路调控,易受遗传和药物调控。在高表达溶质载体家族 7 成员 11 (SLC7A11)(一种胱氨酸转运蛋白)的肿瘤细胞中,葡萄糖缺乏可引发双硫死亡。当细胞缺乏葡萄糖时,SLC7A11 活性升高可能会降低烟酰胺腺嘌呤二核苷酸磷酸 (NADPH) 水平并引发二硫化物应激。这种应激会促进某些蛋白质胱氨酸残基巯基之间形成二硫键,从而损害其正常活性和功能,最终导致细胞死亡。双硫死亡除了导致代谢易损性外,还可能导致免疫逃逸和化学耐药性。当CD8+ T细胞发生双硫死亡时,其耗竭会削弱抗肿瘤免疫力。此外,肌动蛋白细胞骨架完整性的破坏会损害免疫突触的形成,并降低T细胞活化和肿瘤清除率。同时,由SLC7A11过表达驱动的抗氧化缓冲作用可能抑制活性氧(ROS)介导的细胞毒性,从而降低许多化疗药物的疗效。此外,这一认识为代谢癌症治疗的新干预措施开辟了潜在途径。
在营养充足的条件下,SLC7A11 可增强谷胱甘肽合成并降低氧化应激。SLC7A11 基因可抑制铁死亡,并在多种癌症中上调。2017 年有报道称,SLC7A11 在缺乏葡萄糖的情况下显著致敏细胞死亡。考虑到 WAVE 调控复合物仅轻微阻碍双硫死亡,二硫键的紊乱可能会影响多种蛋白质,例如构成肌动蛋白细胞骨架的蛋白质。此外,Yan 等人强调与中度过表达(例如通过双硫死亡)相比,SLC7A11 的高水平过表达可使癌细胞对过氧化氢诱导的细胞死亡更敏感。SLC7A11 对细胞命运的影响受其表达水平和代谢环境的影响。例如,葡萄糖转运蛋白 (GLUT) 抑制剂可有效抑制细胞对葡萄糖的吸收,导致与肌动蛋白细胞骨架相关的蛋白质二硫键交联增强、骨骼肌收缩,并在 SLC7A11 表达升高的癌细胞中诱导双硫死亡。双硫死亡主要发生在这些细胞中,因为将胱氨酸转化为胱氨酸所需的 NADPH 生成不足,从而引发二硫化物应激。越来越多的证据表明,引发双硫死亡可作为治疗各种癌症的有效策略。因此,探索双硫死亡在癌症发展中的作用及其对不同治疗干预的反应至关重要。
近期研究表明,双硫死亡相关基因 (DRG) 在多种癌症中发挥作用,例如肝细胞癌 (LIHC)、膀胱尿路上皮癌 (BLCA)、乳腺浸润性癌 (BRCA) 和肺腺癌(LUAD)。然而,这些过程背后的具体分子机制及其治疗意义仍不清楚。为了填补这一空白,该研究利用原发性肿瘤的转录组数据对 DRG 进行了全面的泛癌种分析。通过应用最小绝对收缩和选择算子 (LASSO) Cox 回归模型,构建了一个稳健的双硫死亡相关基因标签 (DRGS),该标签广泛适用于多种恶性肿瘤。该研究还开发了一个包含 DRG 评分作为定量工具的列线图,用于预测患者预后。在各种类型的癌症中,DRG 评分升高与不良临床预后之间存在密切联系。具有高DRG 评分的 OV 细胞主要由 SLC7A11high 细胞组成。 SKOV3卵巢癌细胞株体外研究表明,SLC7A11高表达的细胞在缺糖条件下会发生双硫死亡。DRG评分分析显示,倒置formin 2 (INF2) 基因在多种女性性腺肿瘤中显著上调,尤其是在卵巢细胞株中。INF2编码福明家族蛋白的一个成员,通过其抑制结构域在调控肌动蛋白丝动力学中起着至关重要的作用。INF2表达增加与子宫内膜癌、前列腺癌和甲状腺癌中的线粒体裂变有关。该研究的功能实验进一步表明,INF2参与了双硫死亡并调节卵巢细胞对治疗的反应性。该研究增强了对 DRGS在多种癌症中的作用的理解,并强调了 SLC7A11-INF2 轴作为生物标志物和治疗靶点的潜力,特别是在 OV 等代谢脆弱的肿瘤中。
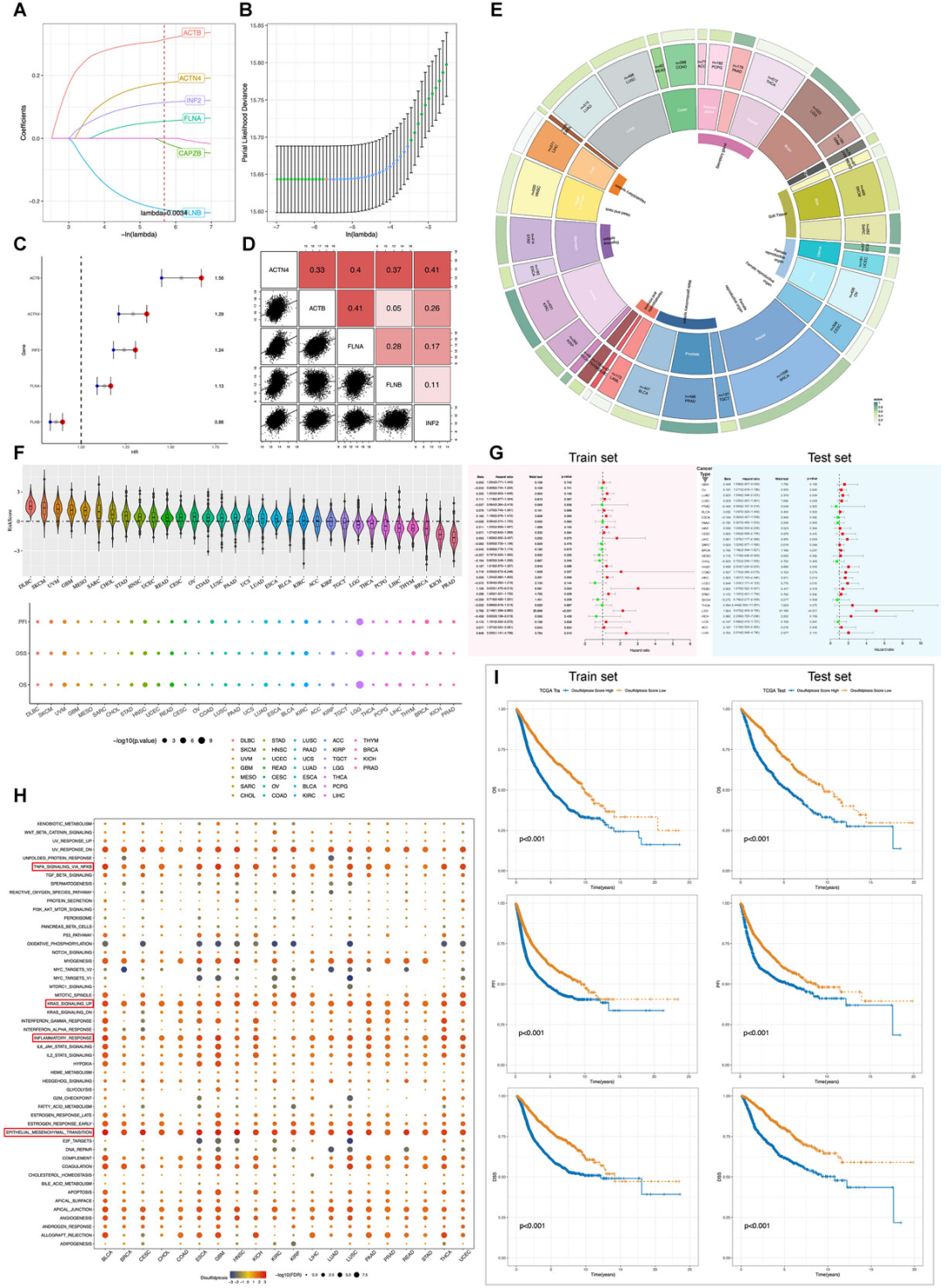
图1 双硫死亡调控基因标签(DRGS)的构建及预后性能评估(图源自Advanced Science)
参考消息:
https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202408556
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)