首页 > 医疗资讯/ 正文
摘要
背景:超快通道心脏麻醉(Ultra-fast-track cardiac anesthesia,UFTCA)是心脏手术后增强恢复(Enhanced recovery after cardiac surgery,ERACS)的关键组成部分。然而,对UFTCA实施影响因素的研究仍然有限。
目的:本研究旨在确定右胸腔镜微创心脏手术(Minimally invasive cardiac surgery,MICS)中UFTCA的预测因素,并开发一种预测UFTCA实施的列线图方法。
方法:这项回顾性研究招募了947名患者,他们在2021年1月至2023年7月期间接受了右胸腔镜MICS检查。患者被随机分为推导组(70%)和验证组(30%)。采用单变量logistic回归分析进行变量选择,然后采用多变量logistic回归模型确定显著预测因子,并构建预测UFTCA实施的列线图。使用验证队列对模型的鉴别、校准和临床有效性进行评估。
结果:多因素分析确定了UFTCA实施的六个独立预测因素:手术类型、胸壁筋膜平面阻滞(Fascial plane chest wall blocks,FPCWB)、术中舒芬太尼和地塞米松剂量、晚于晚上8点的手术和体外循环(CPB)持续时间。列线图表现出良好的判别能力,推导组和验证组的受试者工作特征(ROC)曲线下面积分别为0.869和0.862。校正图与理想对角线接近,决策曲线分析(Decision curve analysis, DCA)证实了模型的临床实用意义。
结论:本研究开发并验证了一个列线图,可以预测MICS患者实施UFTCA。列线图显示,复杂手术,特别是多瓣膜手术,大剂量舒芬太尼,CPB持续时间长,手术时间晚于晚上8点对UFTCA实施不利,而地塞米松和FPCWB对UFTCA实施有利。
关键词:加速术后恢复;超快通道心脏麻醉;微创心脏手术;预测建模;围手术期管理

引言
目前增强术后恢复(ERAS)的概念和原则在世界范围内已被普遍接受。ERAS已显示出其巨大的优势,但较高的死亡率和并发症发生率使心脏手术患者的ERAS方案难以制定。早期,增强心脏手术后恢复(ERACS)是在快速麻醉的基础上发展起来的。快通道心脏麻醉(FTCA)被定义为术后6-8小时内拔管,取得了显著的临床效益。在此基础上,超快通道心脏麻醉(UFTCA)的概念被开发出来,定义为在心脏手术后1小时内拔管。
由于需要心脏手术的患者数量不断增加,加速患者术后恢复、减轻医疗负担、促进有限医疗资源的充分利用变得更加紧迫。几项研究表明,UFTCA显著缩短了住院和重症监护病房(ICU)停留时间,与传统心脏麻醉相比,甚至降低了患者的成本。然而,UFTCA仍然存在很大的争议和问题,特别是它针对特定的患者和手术类型的实践。此外,这对麻醉医生以及科室的合作也是一个巨大的挑战。
本中心于2021年开始对接受右胸腔镜微创心脏手术(MICS)的患者实施UFTCA。大量研究表明,MICS是ERACS的组成部分,与传统的胸骨切开术相比,MICS可以减少创伤、失血和术后并发症。目前,将MICS与UFTCA相结合的研究相对较少,甚至没有文献研究MICS下UFTCA的预测因素。通过深入分析大量的医疗病史,我们的研究试图揭示潜在的决定因素,并开发一个列线图,可以预测UFTCA在右胸腔镜MICS背景下的采用。
材料与方法
本研究经浙江省人民医院机构审查委员会(IRB)批准(批准号:QT2024007)。我们确认所有实验均按照相关指南和规定进行。由于本研究为回顾性设计,浙江省人民医院IRB放弃了书面知情同意的要求。
参与者
在2021年1月1日至2023年7月30日期间,共有967名患者在一家学术机构接受了右胸腔镜MICS筛查。研究数据完全来自我们机构的电子病历系统,该系统捕获了患者的术前特征和术中细节。
排除符合以下标准的患者:心源性休克、感染性休克、体外膜氧合(ECMO)支持、左心室辅助装置(LVAD)植入、数据明显不完整。最终,947例患者入组(图1)。
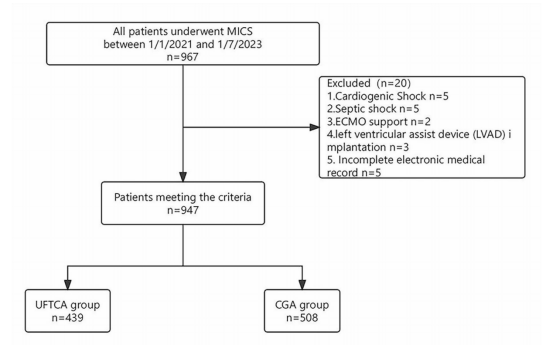
图1.研究人群特征的流程图
CGA,常规全身麻醉;ECMO,体外膜肺氧合;MICS,微创心脏手术;UFTCA,超快通道心脏麻醉
麻醉和拔管
所有患者术前均由同一名麻醉医师进行评估。采用标准化麻醉方案。患者在进入手术室前接受术前教育。入手术室后进行常规监测、有创动脉血压、中心静脉置管。麻醉诱导使用依托咪酯、异丙酚、舒芬太尼和顺式阿曲库铵。麻醉诱导后,将0.375%罗哌卡因溶液与1µg/kg右美托咪定混合(共40-60 ml)用于胸壁筋膜平面阻滞(FPCWB),即深锯肌前平面阻滞或深锯肌前平面联合胸神经I (PECS I)和胸神经II (PECS II)阻滞。
持续输注异丙酚和瑞芬太尼维持麻醉。UFTCA患者,术后1小时内达到拔管标准并拔除气管导管,随后转ICU。常规全麻组(CGA)持续给予麻醉维持药物,直至患者转至ICU。
在我中心所有微创心脏手术均采用单腔气管导管。我们的手术从股动静脉插管开始建立CPB。达到全流量CPB后,暂停机械通气,通过右腋窝小切口进行手术。在此过程中,萎陷的右肺提供了最佳的手术暴露。使用专门的手术器械通过这种方法进行心脏手术。这项技术消除了对双腔管的需求,同时仍能获得足够的手术视野。
经过综合评估,对考虑实施UFTCA的患者调整麻醉维持用药。认为患者符合拔管的指征:(1)稳定的血流动力学,血管加压药物支持最小[去甲肾上腺素≤0.05μg/(kg·min),多巴酚丁胺≤5.0μg/(kg·min)]甚至无血管加压药物支持,且无难治性心律失常。(2)出血量最小(引流量< 50 mL/h),血红蛋白≥80 g/L, ACT恢复到术前基线。(3)动脉血气分析显示自主呼吸时氧合充足(SPO2≥95%,FiO2 100%,PaO2≥60 mmHg, PaCO235-45 mmHg, pH 7.35-7.45),无电解质失衡。(4)通过适当逆转神经肌肉阻滞保持完全警觉,并能够遵循伸舌、睁眼、握拳和抬头等指令。(5)保持体温正常(体温≥36℃),患者拔管后转ICU。若术后30分钟内无法拔管,则将患者转至麻醉恢复室,接受全面监护、呼吸机支持和专业管理。如果60分钟内无法拔管,则放弃UFTCA,并将患者转至ICU。
统计分析
本研究采用R 4.3.3版本进行统计分析。P值小于0.05 (P < 0.05)认为有统计学意义。使用中位数和极差对连续数据进行汇总,以反映数据集的固有特征。对于分类数据,我们使用频率和百分比来传达每个类别的分布。为了比较患者组,我们将Mann-Whitney U检验应用于连续变量,而卡方检验用于分析分类变量。传统的机器学习程序建议,对于相对较小的数据量(约10,000个),使用7:3分割比率。因此,对于模型推导,选择663例患者作为推导组,其余284例患者分配给验证组。
我们使用单变量回归分析。p < 0.05的变量纳入多元logistic分析。在对以上两步进行综合评估后,我们最终寻找具有统计学意义的指标。然后,我们构建了一个列线图。将各变量结果对应的得分相加,得到总分,即UFTCA成功实施的得分。通过内部验证对模型进行验证。我们分别使用判别和校准来评估推导组和验证组。使用受试者工作特征 (ROC) 曲线以及曲线下面积 (AUC) 作为指标来评估区分能力(指模型区分成功实施 UFTCA 的人的能力)。使用Hosmer-Lemeshow拟合优度检验评估模型校准,该检验将观察到的概率与模型预测的概率进行比较。P>0.05的值表示校准满意。此外,我们使用决策曲线分析(DCA)来帮助我们了解建模在临床决策中的价值。
结果
患者基线临床特征
本研究共筛查了2021年1月至2023年7月期间在我院接受右侧胸腔镜MICS的967例患者,排除20例,包括心源性休克5例、感染性休克5例、需要ECMO支持2例、接受LVAD植入3例以及临床资料不完整5例(图1)。最终纳入研究的947例患者中,663例作为推导组,284例患者作为验证组。患者的人口统计学和临床特征总结在补充表S1中。共有439例患者(46.36%)成功实施了UFTCA。
模型开发
在推导组中,单变量分析确定了28个与UFTCA实施显著相关的变量(补充表S2)。多变量分析结果显示,手术类型(比值比[OR]=4.88,95%置信区间[CI]:1.52~15.63,p=0.008)、术中舒芬太尼用量(OR=1.04,95% CI:1.03~1.05,p<0.001)、体外循环(CPB)持续时间(OR=1.02,95% CI:1.01~1.03,p=0.001)以及手术结束时间晚于晚上8点(OR=2.29,95% CI:1.34~3.93,p=0.003)是UFTCA实施的不利因素;而胸壁筋膜平面阻滞(FPCWB,OR=0.15,95% CI:0.08~0.30,p<0.001)和地塞米松用量(OR=0.92,95% CI:0.87~0.98,p=0.012)则有利于UFTCA的实施(表1)。这些结果表明,手术复杂度较高(尤其是多瓣膜手术)、舒芬太尼用量增加、CPB时间延长以及手术结束时间过晚会降低UFTCA实施的成功率,而使用地塞米松和胸壁筋膜平面阻滞则有助于实现术后即刻拔管。使用这六个候选预测因素开发了一个列线图,用于预测成功实施UFTCA的概率(图2)。
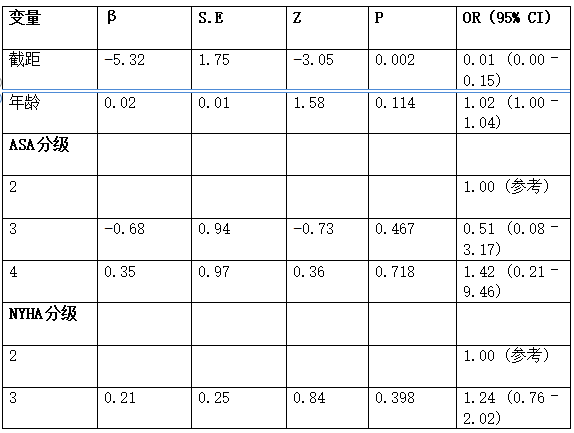
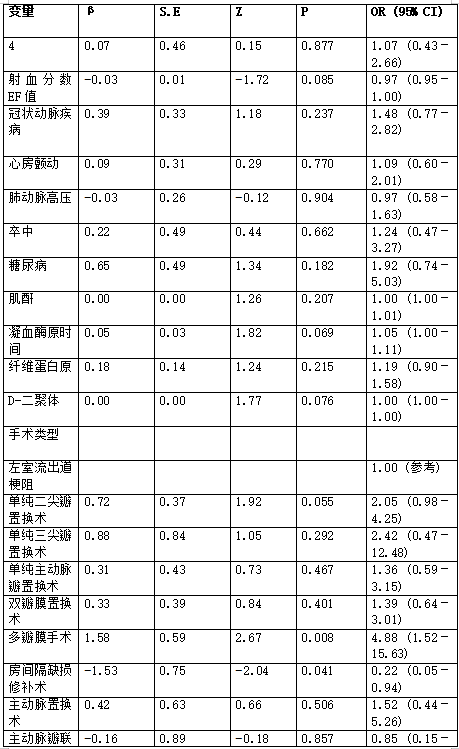
表 1. UFTCA实施的多变量逻辑回归模型。
ASA:美国麻醉医师协会; AVR:主动脉瓣置换术; CI:置信区间; CPB:体外循环; DVR:双瓣膜置换术; EF: 射血分数; LVOT: 左心室流出道; MVR: 二尖瓣置换术; NYHA: 纽约心脏病协会; OR: 比值比; TVR: 三尖瓣置换术。
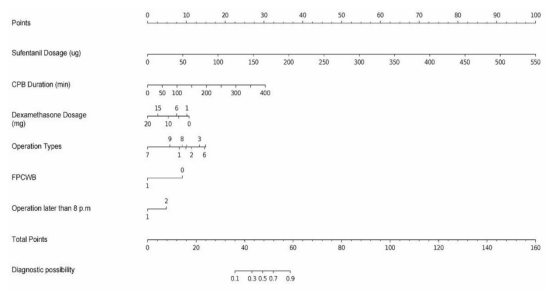
图2. 预测UFTCA实施的列线图
手术类型中引用的数字:1. 左室流出道梗阻;2. 单纯二尖瓣置换术;3. 单纯三尖瓣置换术;4. 单纯主动脉瓣置换术;5. 双瓣膜置换术;6. 多瓣膜手术;7. 房间隔缺损修补术;8. 主动脉置换术;9. 主动脉瓣联合升主动脉置换术;10. 其他。AVR, 主动脉瓣置换术; CPB, 体外循环; DVR, 双瓣膜置换术; FPCWB, 筋膜平面胸壁阻滞; LVOT, 左心室流出道; MVR, 二尖瓣置换术; TVR, 三尖瓣置换术; UFTCA, 超快通道心脏麻醉。
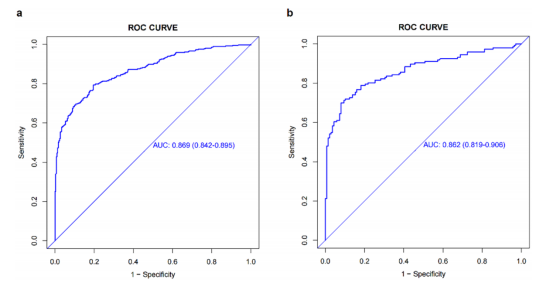
图3. 推导组 (a) 和验证组 (b) 的受试者工作特征 (ROC) 曲线分析
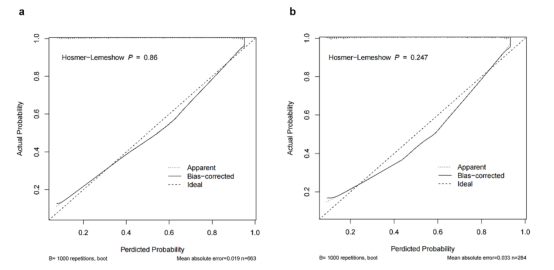
图4. 推导组 (a) 和验证组 (b) 的校准曲线
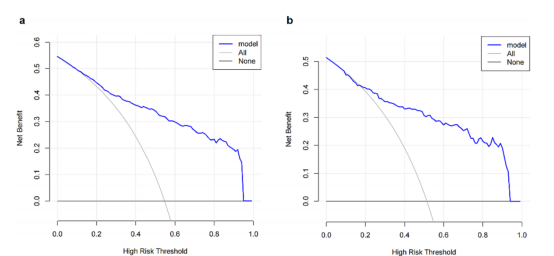
图5. 推导组(a)与验证组(b)的决策曲线分析(DCA)。
模型性能与内部验证
该列线图的曲线下面积(AUC)在推导组为0.869(95% CI: 0.842–0.895),在验证组为0.862(95% CI: 0.842–0.895)(图3a, b)。两个队列的校准曲线均显示预测值与观察值之间紧密匹配,验证了所开发预测模型的出色校准(图4a, b)。Hosmer–Lemeshow检验在推导组和验证组产生的P值分别为0.86和0.247,均不显著。这些结果表明预测的UFTCA实施与观察到的实施之间具有很强的一致性。采用DCA评估模型的临床实用性(图5a, b)。分析显示,在广泛的决策阈值范围(概率从10%到95%)内,使用该列线图的风险估计可为患者带来更高的净收益。这也意味着为本研究构建的列线图具有很强的区分性能、良好的校准预测、有意义的临床适用性,并且能够应用于不同的患者群体。
讨论
UFTCA和MICS都是ERACS的重要组成部分。随着微创技术的出现,心脏手术经历了显著的发展。与胸骨正中切开术相比,MICS在亚洲人群中的应用已被证明是安全、有效且可重复的。然而,UFTCA在MICS中的实施目前尚未广泛开展。自2021年以来,我们中心一直负责管理MICS下的UFTCA,并取得了令人满意的结果。该研究提供了一个经过验证的用于预测成功实施UFTCA的列线图,以帮助临床决策。本研究确定了六个独立的预测因素,并用于构建一个估算UFTCA实施可能性的新型列线图。该列线图在内部验证期间表现出良好的AUC和校准性能。此外,DCA也证实了该列线图的临床实用性。这表明当阈值风险在10%到95%范围内时,使用该预测模型做出干预决策是有利的。
心脏手术后立即拔管的研究主要集中在新生儿和儿童。关于成人实施UFTCA预测因素的研究相对较少。一些研究确定了术后立即拔管的潜在预测因素,包括年龄、体重指数(BMI)、糖尿病、手术类型、芬太尼剂量、椎旁阻滞和术中输血。我们还检索了心脏手术下实施FTCA的相关预测因素,如近期急性冠脉综合征、术前肾功能和体外循环时间。相比之下,我们的研究表明,术中舒芬太尼和地塞米松剂量、CPB持续时间、胸肌筋膜平面阻滞的使用、手术类型以及手术结束时间晚于晚上8点是实施UFTCA的独立因素。在这些预测因素中,术中地塞米松剂量和手术结束时间晚于晚上8点在以往文献中很少被提及。
在我们中心进行微创MICS期间,右肺需要萎陷,这可能导致复张性肺损伤。先前的研究表明糖皮质激素对肺泡-毛细血管膜通透性以及炎症介质和组织修复介质具有显著益处。基于此证据,我们中心接受MICS的患者常规使用地塞米松或甲泼尼龙,尽管其临床效果尚不明确。我们的临床观察显示,与接受CGA的患者相比,接受UFTCA的患者术后恶心呕吐(PONV)的发生率更高。而地塞米松在预防PONV方面被充分证明有效,因此我们的心脏手术麻醉医生在实施UFTCA时倾向于使用地塞米松。本研究的另一个重要发现是手术结束时间对UFTCA实施的影响。有证据表明,夜间手术可能比日间手术有更高的术后并发症和不良事件发生率。此外,如果外科医生从白天连续工作到晚上,术后并发症的发生率会大大增加。这表明适当的工作量可以确保外科医生的工作状态,并增加患者住院期间的安全性。另外,在夜间,一些麻醉医生主观上更倾向于减少他们的工作量,因此他们更愿意选择传统的全身麻醉,这样可以在术后无需复苏而直接将患者送入ICU。
FTCA和UFTCA的基础是给予相对小剂量的短效阿片类药物,并辅以丙泊酚或其他麻醉药物。因此,显著减少舒芬太尼剂量是实施UFTCA的独立预测因素。然而,减少术中阿片类药物的使用存在争议,因为它可能导致术后镇痛需求增加。我们中心在UFTCA中实施FPCWB以缓解术后疼痛。我们之前的观察性研究显示,使用FPCWB的患者ICU补救镇痛的发生率低于未使用者。Toscano等人的研究表明,持续的深前锯肌平面阻滞可改善术后疼痛并减少术后阿片类药物需求。在本研究中,CPB持续时间是实施UFTCA的独立预测因素。CPB是心脏手术期间使用的非生理性循环,可导致肺内皮损伤和肺血管阻力增加。许多研究表明,CPB持续时间是心脏手术后并发症(如肾损伤和脑微栓塞)的独立危险因素。CPB持续时间可能与手术的复杂性相关。结果显示,多瓣膜手术是实施UFTCA的独立危险因素。接受单一手术的患者比接受复杂手术的患者更有可能成功拔管。
本研究有几个局限性。首先,该模型是关于MICS中实施UFTCA的,不能适用于所有类型的心脏手术。其次,尽管我们中心有既定的UFTCA方案,但外科医生或麻醉医生在决定是否实施UFTCA时仍存在一些主观因素影响,例如手术复杂性和结束时间过晚。第三,研究的回顾性性质限制了在确定的预测因素与UFTCA实施之间建立因果关系以及推广性的能力。
为了确认模型的有效性,有必要进行进一步的多中心前瞻性研究。在机器学习进展的推动下,已经开发出更广泛的变量筛选方法。扩大考虑的变量数量并应用不同的筛选策略可以构建增强的预测模型。
结论
在本研究中,结合单变量和多变量逻辑分析筛选出6个预测因子,并构建了一个预测UFTCA实施的列线图。结果表明,手术更复杂(尤其是多瓣膜手术)、舒芬太尼剂量更高、CPB持续时间更长以及手术结束时间晚于晚上8点不利于UFTCA的实施,而使用地塞米松和FPCWB则有利于UFTCA。该列线图在区分能力、校准和实际临床应用中表现良好。研究结果表明其有潜力帮助决策在MICS患者中实施UFTCA。
醉仁心胸 评述
本研究聚焦于超快通道心脏麻醉,超快通道心脏麻醉作为心脏手术术后增强恢复的核心环节,其实施效果与患者术后康复进程紧密相关。然而针对UFTCA实施影响因素及精准预测工具的研究较为匮乏,限制了ERACS理念在临床实践中的深度落地。研究发现揭示了UFTCA实施的关键促进与阻碍因素:有利因素:胸壁筋膜平面胸壁阻滞的应用、术中给予地塞米松。不利因素:手术复杂程度高(尤其是多瓣膜手术)、术中舒芬太尼剂量大、体外循环(CPB)持续时间长、手术开始时间晚于晚上8点。使用这六个候选预测因素开发了一个列线图,用于预测成功实施UFTCA的概率。列线图验证环节,指导组与验证组受试者工作特征(ROC)曲线下面积分别达0.869、0.862,校正图贴合理想对角线,决策曲线分析(DCA)亦佐证临床实用价值,构建出兼具区分度、校准度与临床效能的预测模型。
从临床意义看,该列线图实现多维度突破:一方面,清晰界定复杂手术(尤其多瓣膜手术)、大剂量舒芬太尼、长时CPB、晚时段手术对UFTCA实施的阻碍,以及地塞米松、FPCWB的促进作用,为麻醉方案个性化优化提供量化依据 ;另一方面,填补MICS中UFTCA预测工具空白,推动ERACS从理念向精准实践转化,助力麻醉科医师提前识别高风险场景、调整干预策略,加速心脏手术围术期加速康复进程。
本研究不仅填补了MICS中UFTCA预测因素的研究空白,更重要的是,它提供了一个经过严格验证、性能优良的预测模型(列线图)。该模型直观揭示了影响UFTCA实施的临床关键点,为优化围术期管理、推动ERACS理念在微创心脏手术中的落地提供了有力的数据支持和实用的决策工具。
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)