首页 > 医疗资讯/ 正文
痤疮是一种损容性的毛囊皮脂腺单位的慢性炎症性疾病,全球发病率为9.38%,以青少年最常见,15~20岁发病率最高。目前认为痤疮主要与皮脂分泌增加、毛囊内角质细胞的异常增殖和分化、细菌定植以及随后的宿主炎症反应相关,其中炎症反应贯穿痤疮的始终。自体活性物质、激素、微生物等均通过作用于相关受体进而引起一系列炎症因子分泌、皮脂分泌增多、角质形成细胞分化改变等方式参与痤疮的发生发展。
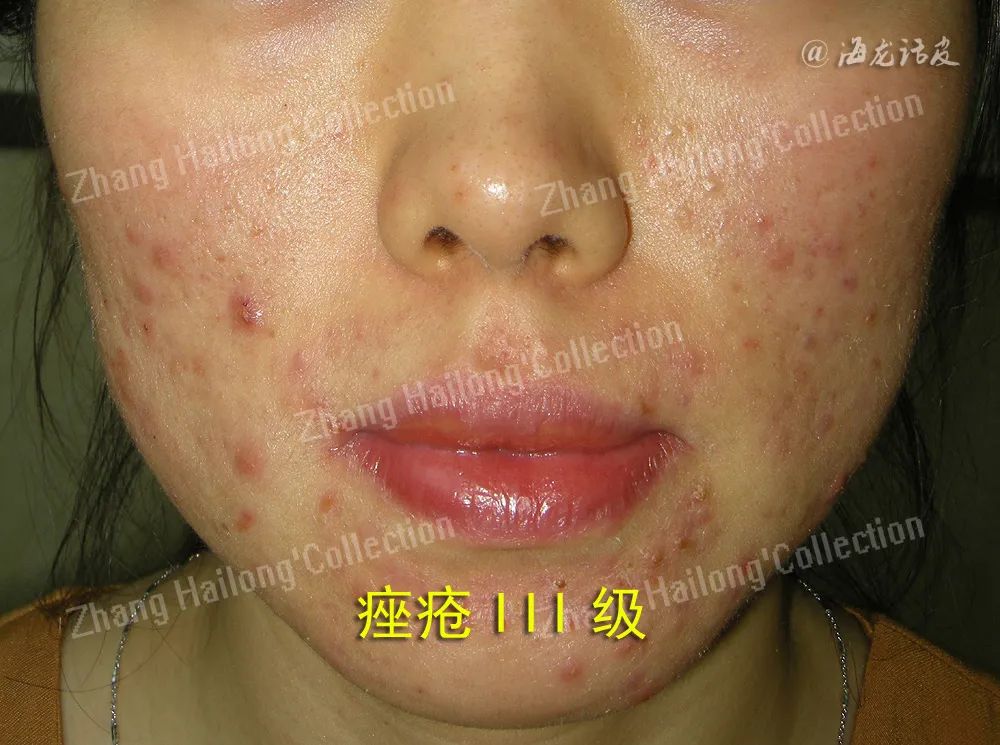
目前组胺受体(histamine receptor,HR)、雄激素受体(androgen receptor,AR)、Toll样受体(toll-like receptors,TLRs)在痤疮发病机制中备受关注,成纤维细胞生长因子受体(fibro blast growth factor receptor,FGFR)、肝脏X受体(liver X receptor,LXR)、黑皮质素受体(melanocortin receptor,MCR)与痤疮发病研究尚少,本文对这些受体在痤疮中的作用进行阐述,为痤疮的临床治疗提供新思路。
1.介导炎症反应的相关受体
1.1HR
组胺是一种血管活性化学物质,广泛分布于人体各种组织,由L-组氨酸通过组氨酸脱羧酶催化合成,作为介质或神经递质与特定亚型受体结合,参与瘙痒、炎症、细胞增殖与分化、免疫反应等生理和病理过程。HR分为4个亚型:H1R~pR,其中H1R 广泛表达于神经细胞、平滑肌细胞、免疫细胞等,H1R信号传导使得炎症部位嗜酸性粒细胞和中性粒细胞的趋化性增加、抗原呈递细胞的功能容量增加,同时促进前列环素、一氧化氮、花生四烯酸及其代谢物和血栓素的合成、气道和血管平滑肌细胞收缩。
此外,H1R信号转导与MAPK信号转导和cAMP积累有关,导致促炎基因表达增加。肥大细胞分布于皮肤和粘膜中,组胺与同一受体的结合促进了细胞内钙的释放和肥大细胞向组织中的募集,肥大细胞通过产生大量介质对外界刺激做出反应参与多种炎症性疾病。此外,痤疮丙酸杆菌会改变痤疮毛囊微环境的pH值,这是产生组胺或组胺样物质的最佳环境,导致痤疮患者瘙痒。
Eliasse等研究发现肥大细胞的活化标志物CD69在粉刺阶段达到峰值,CD4T细胞促进了肥大细胞产生IL-17。在一项纳入17例超过6个月痤疮瘢痕患者研究中,患者萎缩性瘢痕和增生性瘢痕中均存在肥大细胞浸润。痤疮的炎症反应由组胺的释放介导,因此,引入抗组胺药可以有效防止新的痤疮病变的形成。有研究表明,异维A酸联合左西替利嗪治疗痤疮效果较单服用异维A酸更佳。异维A酸联合地氯雷他定治疗痤疮后,患者血清白介素(interleukin,IL)-1、IL-6、IL-8、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)表达水平降低。在一项针对60例志愿者的随机、双盲对照临床试验中,治疗组痤疮患者外用H1R拮抗剂2%Meclozine药物凝胶治疗12周后痤疮严重程度指数评分降低了20.1%(P<0.001),未报告不良事件。
1.2AR
AR属于类固醇/核受体超家族,具有配体结合域、DNA结合域和N端调节域3个结构域。AR的配体是活性雄激素:双氢睾酮(dihydrotest osterone,DHT)和睾酮。角质形成细胞、成纤维细胞、汗腺细胞、毛囊外毛根鞘的基底细胞、皮脂腺细胞等均有AR的表达。活性雄激素与AR的结合可以刺激巨噬细胞及皮脂腺细胞分泌促炎因子IL-1、IL-6和TNF-α,这与在痤疮病变部位观察到的炎症反应一致。
促炎因子分泌导致的局部炎症反应又进一步加剧雄激素水平异常,形成恶性循环,促成痤疮的发生和进展。Clascoteron作为一种雄激素受体抑制剂,与雄激素二氢睾酮竞争与皮脂腺和毛囊中的AR结合,以剂量依赖性方式抑制双氢睾酮造成的痤疮下游效应如脂质合成和炎性细胞因子的产生,以减弱痤疮发病机制所需的信号传导。
1.3TLRs
TLRs表达于许多细胞的跨膜蛋白,是最早发现的模式识别受体。TLRs的名称源于其结构和功能与果蝇中发现的一种跨膜受体Toll相似,Toll是在果蝇中发现的一个受体蛋白,参与其胚胎发育时背腹极性的建立,后又有研究证实Toll参与果蝇的抗真菌免疫。进一步研究发现,哺乳动物存在Toll的同源分子,能诱导炎症应答基因的表达,构成TLRs家族。人类TLRs家族包括TLR1~TLR10及TLR14。
1.3.1TLR2:当受到刺激时,TLR2与TLR1或TLR6形成异源二聚体,负责识别多种微生物相关分子模式,如肽聚糖(peptidoglycans,PGNs)、脂蛋白、脂磷壁酸(lipoteichoic acid,LTA)和脂多糖(lipopolysaccharides,LPS),其中PGNs是痤疮丙酸杆菌细胞壁主要成分。角质形成细胞可被痤疮杆菌激活,通过TLR2诱导的细胞内钙内流产生促炎细胞因子(如IL-6和单核细胞趋化蛋白-1),钙通过TLR2激活的持续流入导致角化。痤疮的严重程度与TLR2水平呈正相关。王慧等还发现TLR2水平的升高与痤疮瘢痕形成相关。
1.3.2TLR4:TLR4形成一个由TLR4同源二聚体和两个髓样分化蛋白-2(myeloid differentiation protein-2,MD-2)组成的受体复合物。可溶性的脂多糖结合蛋白(LPS-binding protein,LBP)可以通过从细菌膜或细菌来源的外膜囊泡中提取,并将其递送到TLR4受体复合物中,从而进一步发挥分子伴侣的作用。此外,TLR4也通过Toll/IL1R结构域的衔接蛋白介导的信号通路,从而产生抗炎细胞因子,如IL-10和干扰素(interferon,IFN)-β。光动力疗法治疗痤疮患者后发现皮脂腺上TLR2与TLR4受体显著减少。壬二酸、水杨酸均能通过与TLR4蛋白受体有效地结合从而抑制痤疮丙酸杆菌引起的角质形成细胞表面TLR4蛋白的表达。维A酸类药物及抗微生态药物均可通过下调TLR2/TLR4抑制痤疮的炎症反应。
1.4FGFR
FGFR属于受体酪氨酸激酶超家族,包括4种亚型:FGFR1~4。研究发现FGFR2突变体与痤疮发病相关,进一步研究发现,在患有痤疮的皮肤组织中,AR信号触发两种FGFR2配体FGF-7和FGF-10的转录,从而导致FGFR2信号的激活。
1.5LXR
LXR是在脂质代谢和运输中起关键作用的核受体,表达在表皮角质形成细胞和成纤维细胞中,可以刺激表皮屏障形成所需的脂质合成,并诱导皮脂分泌增加。此外,已证明LXR激活可上调IFN-γ等炎性因子的表达,并促进M1巨噬细胞极化,引发促炎反应并分泌各种促炎因子。
2.与皮脂分泌相关的受体
2.1HR
皮脂腺是负责产生皮脂的主要细胞,皮脂过度分泌参与痤疮的发生发展,皮脂腺细胞中存在H1R,苯海拉明作为H1R拮抗剂可使皮脂生物标志物角鲨烯水平显著降低,调节皮脂腺功能。此外,H1R还可以通过G-蛋白偶联途径直接与腺苷酸环化酶结合,补充cAMP水平。由于胰岛素通过降低脂肪细胞cAMP的速率来减少脂肪代谢,因此,如果cAMP的产生是由H1R拮抗剂介导的,这有助于减少脂肪细胞中的皮脂腺细胞。H1R拮抗剂可能是痤疮、皮脂溢出等与皮脂生成过多相关疾病的一种新的治疗选择。
2.2AR
雄激素在皮肤的作用主要取决于结合AR的水平,而并非完全取决于雄激素水平的高低。AR功能的缺失及AR转录水平的下降均可抑制雄激素对皮肤附属器官的作用。当AR被雄激素配体激活后,AR则与热休克蛋白解离,发生构象改变,进而暴露核移位信号,诱导相关脂质调节基因的转录,促进皮脂细胞的增殖和分化,并诱导脂质合成,这个过程中过氧化物酶体增殖物激活受体(peroxisome proliferators activated receptors PPARs)可作为配体起协同作用。
此外,雄激素可通过AR/胆固醇调节元件结合蛋白1(sterol regulator yelement binding protein1,SREBP-1)/乙酰辅酶A羟化酶1(acetyl coenzyme A carboxylase1,ACC1)蛋白信号通路的过度激活使皮脂分泌增多。AR还可通过提高FGFR2的活性,刺激皮脂腺过度分泌。螺内酯可以阻断双氢睾酮与皮脂腺细胞内AR的结合从而抑制雄激素诱导的皮脂腺细胞增殖并减少皮脂的分泌。
2.3胰岛素样生长因子-1受体
胰岛素样生长因子-1(insulin like growth factor1,IGF-1)水平在青春期增加,通过诱导5α-还原酶活性和AR激活来刺激皮脂腺的脂肪生成并增强雄激素信号传导。目前已证实,痤疮与胰岛素抵及高胰岛素血症之间存在密切关联,高胰岛素血症刺激IGF-1受体,导致IGF-1表达增加,增强肾上腺对促肾上腺皮质激素的敏感性,促进肾上腺雄激素的产生,增强AR活性。
此外,IGF-1可通过激活皮脂腺PI3K/Akt/Fox01途径,减少SZ95细胞增殖,诱导脂质积累,刺激脂肪形成。有研究发现活动性痤疮和痤疮后疤痕患者的IGF-1的血清水平都显著高于对照组,IGF-1水平升高通过激活PI3/Akt通路和MAPK/ERK信号转导和诱导固醇调节元件结合蛋白1c来增加脂肪生成。
2.4MCR(黑皮质素受体)
MCR有5个亚型:MC1R~MC5R。在人皮脂腺中,MC1R和MC5R均有表达。既往MC5R水平仅在小鼠皮脂腺细胞和人皮脂腺细胞培养模型中进行了研究,有研究发现,与对照组相比,痤疮组MC5R水平并不高。
3.与角化过程相关的受体
雄激素是来源于性腺和肾上腺的一种类固醇激素,包括雄激素前体(脱氢表雄酮、硫酸脱氢表雄酮和雄烯二酮)和具有活性的雄激素(睾酮和二氢睾酮)。雄激素与AR结合在滤泡漏斗处代谢更强,皮脂成分的改变和IL-1通过过度刺激细胞增殖和损害分化程序导致角质形成细胞的角化及脱屑。Kumtornrut等体外分析表明,真皮成纤维细胞表达高水平的AR,这些细胞在激素刺激后释放的生长因子可以抑制角质形成细胞分化,从而证明雄激素与AR结合可能对角质形成细胞产生间接影响。
4.结语
对痤疮的不断深入研究发现,HR、AR、TLRs在不同环节参与了痤疮的发生与发展,以这些受体作为靶点的治疗逐渐受到关注。通过抗组胺药可减少炎症介质的释放、缓解痤疮的瘙痒、减少皮脂细胞中的角鲨烯以及抑制肥大细胞诱导的纤维化和瘢痕;雄激素受体拮抗剂或抑制雄激素受体活性可抑制下游炎症因子的产生、减少皮脂生成;下调TLRs(TLR2及TLR4)可抑制痤疮引起机体的炎症及免疫反应。
目前对于FGFR、LXR、MCR研究尚少,关于抗组胺药及雄激素受体抑制剂的局部使用在痤疮中的应用仍缺乏多中心、大数据临床研究,其潜在疗效仍需要进一步阐明。针对性阻断TLR2及TLR4的药物目前处于研究空白,在治疗痤疮中有很大前景。综上,未来可以考虑使用与痤疮发病相关受体的抑制剂来开发新的痤疮治疗方法。
参考文献:
1.林雨秋,聂文佳,李光,李世洋.痤疮发病相关受体的研究进展[J].皮肤性病诊疗学杂志,2025,32(6):449-454.
2.单雨婷,路永红,杜秀君.雄激素及雄激素受体在痤疮发病中的作用[J]皮肤病与性病,2016,38(2):108-112.
3.王慧,官杰,罗晓庆等.Toll样受体2与白介素-10在痤疮瘢痕形成过程中的作用及相关性[J].临床皮肤科杂志,2014,43(12):713-715.
4.贾仁川,林景荣.雄激素在痤疮发病机制中的作用及治疗应用[J].中国皮肤性病学杂志,2023,37(5):503-508.
5.冯睿,蒋娟.痤疮的抗雄激素治疗进展[J].中国麻风皮肤病杂志,2022,38(7):483-487.
6.其他参考文献(略).
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)