首页 > 医疗资讯/ 正文
婴儿猝死综合征(SIDS)是指1岁以下婴儿在无明显外伤或明显病因情况下,突然、意外死亡,尽管经过详尽尸检和病史调查,仍难以解释其死因。当前学界普遍认为SIDS的发病机制呈多因子叠加效应,即“致病易感期的胎儿/婴儿生物学脆弱+关键发育期+环境因素”。过去十余年研究发现,一些自身免疫介导的自身抗体可作用于心脏离子通道,引发致命性心律失常,导致猝死风险增加,但自身免疫与SIDS之间的直接联系并未被充分探明。
7月8日,发表于Circulation期刊上的一项前沿研究揭示了自体免疫在SIDS发病中的潜在作用。该研究由瑞士伯尔尼大学及法国南特大学等多中心团队合作完成,通过系统筛查婴儿血清中的自身抗体,对TRPV2离子通道的自身抗体与SIDS的关联进行了深入探索,并构建动物模型证实了其致死性作用,首次提出抗TRPV2自身抗体可能是婴儿猝死的一个关键生物标志物和潜在治疗靶点。

本研究使用来自多中心的婴儿血清样本,共计47例,包含SIDS死亡婴儿、意外窒息致死婴儿及健康对照组。通过创新的肽微阵列技术,对针对心脏离子通道表面外部肽段的自身抗体进行高通量筛查,重点分析IgG自身抗体的分布及其差异。此外,研究团队设计动物实验,将小鼠免疫接种以人类及鼠源TRPV2通道的靶向肽序列诱导自身免疫反应,随后监测新生小鼠的存活情况,并通过电生理学检测TRPV2通道功能变化和心肌细胞功能学指标,揭示抗体对心脏功能的影响。
研究结果
自身抗体谱发现
结果显示,在所有筛查的自身抗体中,唯一与SIDS显著相关的自身抗体靶向TRPV2(瞬时受体电位范尼尔2型通道)的一段独特肽段(PTGPNATESVQPMEGQEDEG),该肽段对应TRPV2的外部“孔崁环”结构域,该结构域对维持通道开放构象至关重要。SIDS组中84.6%的婴儿血清检测出抗TRPV2抗体,对比意外窒息组50%及健康对照组25%,差异显著(P=0.028),准确率达71%。
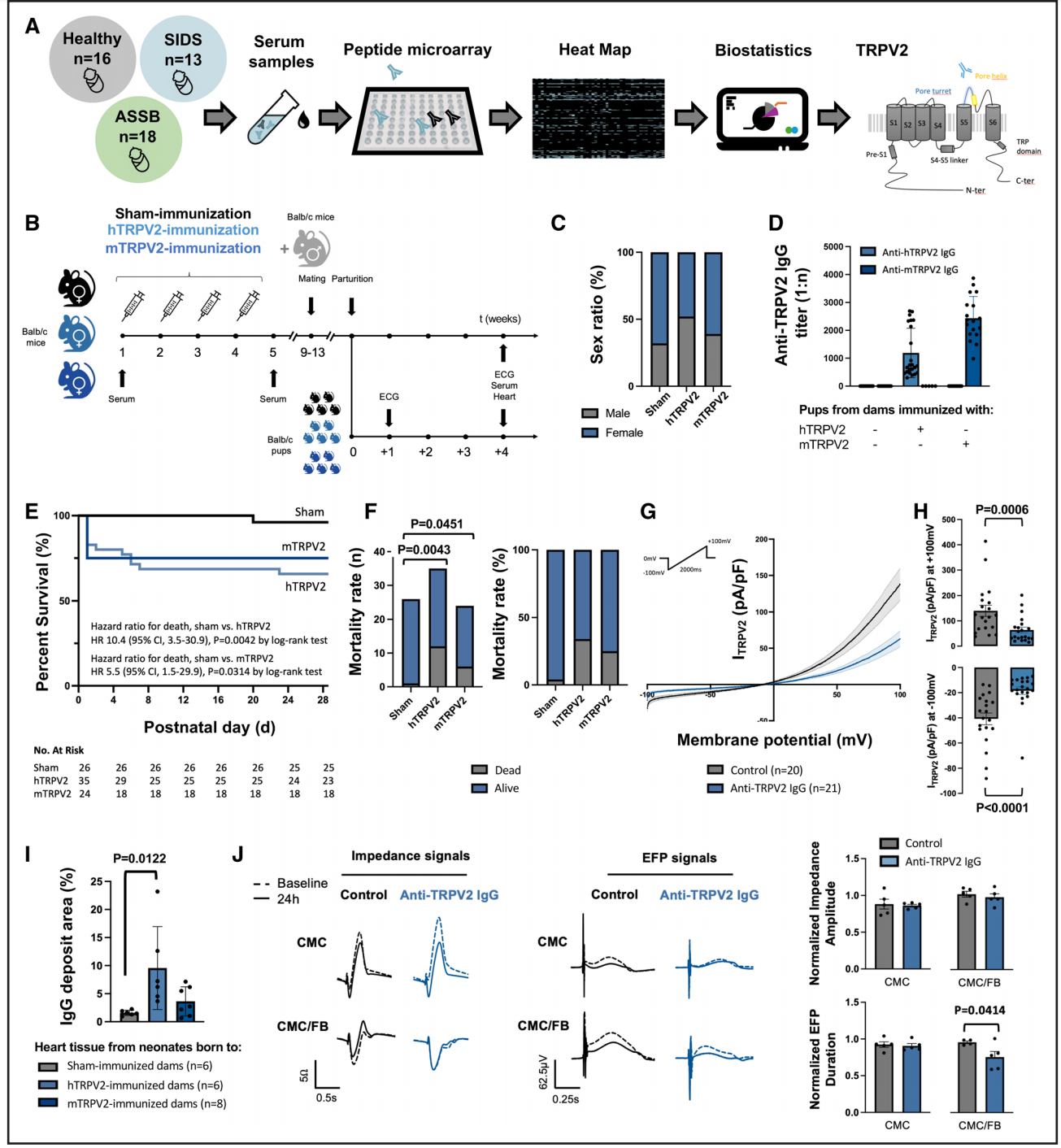
图:SIDS免疫特征
动物模型验证
通过免疫接种,平衡小鼠产生了针对人或鼠TRPV2靶点肽段的自身抗体,免疫母鼠产下的后代中,检测到母体抗TRPV2 IgG通过胎盘传递。新生小鼠中,12/35(人TRPV2抗体组)与6/24(鼠TRPV2抗体组)在出生后一个月内死亡,远高于对照组仅1例死亡(P=0.0174)。死亡多发生在出生后6天内。生存分析显示,人TRPV2自身抗体组新生儿死风险增10倍,鼠组则增5倍
电生理功能改变
HEK293细胞表达的人TRPV2通道,在机械刺激下表现出典型的电流-电压特征。加入抗TRPV2自身抗体后,通道电流幅度减少约50%,提示抗体抑制通道活性。进一步在人心肌细胞与心脏成纤维细胞的共培养系统中,抗体导致细胞场外电位持续时间缩短,反映心电图QT间期缩短,推测可能引发心律失常风险增高。免疫组化显示抗TRPV2抗体沉积于新生鼠心肌内,主要位于纤维细胞分布区域。
研究意义与潜在影响
本研究首次从免疫学角度揭示了抗TRPV2自身抗体与婴儿猝死综合征的密切联系,从分子靶点、功能障碍到动物模型的致死现象,为SIDS的病因分析提供新视角。TRPV2离子通道在心肌细胞、心脏巨噬细胞及间质成纤维细胞中表达,主要参与调节细胞内钙离子浓度及心肌收缩力协调。抗TRPV2抗体通过特异性结合抑制通道开放,可能破坏心肌细胞间机械信号传导和电活动同步,诱发致命心律失常。该发现与“多因素三重风险模型”高度契合,说明自身免疫可成为婴儿本体脆弱性的重要组成部分。
鉴于SIDS诊断的复杂性和标志物的缺乏,抗TRPV2自身抗体有望成为首个可靠的血清生物标志物,辅助临床早期识别高危婴儿。此外,其作为治疗靶点潜力巨大,可通过免疫吸附或抗体中和策略减少新生儿猝死风险,开辟新型防治思路。未来还需大规模多中心前瞻队列研究验证抗体的预警价值并解剖其作用的分子机制。
原始出处
Maguy A, Tessier A, Mahendran Y, et al. Anti-TRPV2 Autoantibody Linked to Sudden Infant Death Syndrome. Circulation. 2025;152(1):81–84. doi:10.1161/CIRCULATIONAHA.125.073748
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)