首页 > 医疗资讯/ 正文
外周T细胞淋巴瘤(PTCL)是一类侵袭性强的恶性肿瘤,治疗选择有限,传统治疗进展缓慢。异基因造血干细胞移植(allo-HCT)是治疗对一线治疗无反应或复发的PTCL患者的主要手段。在一些罕见的T细胞淋巴瘤亚型中,allo-HCT也应考虑用于一线巩固。
尽管allo-HCT在PTCL治疗中已确立其地位,但缺乏针对allo-HCT的详细指南。因此欧洲血液和骨髓移植学会(EBMT)实践协调和指南委员会于2024年9月30日至10月1日在法国里尔召开国际专家会议,制定了关于PTCL患者接受allo-HCT的最佳实践建议,于近日发表于《The Lancet Haematology》。

针对主要PTCL亚型的allo-HCT建议
PET的使用
-
PET是PTCL分期和疗效评估的首选成像方式。
-
在完成常规治疗后,无论是初始治疗还是挽救治疗,都建议进行PET检查。
-
建议进行中期PET检查,并计算最大标准化摄取值的变化(ΔSUVmax)。
一线治疗中的HCT巩固(图1)
-
尽可能考虑参加临床试验。
-
对于适合移植且完全代谢缓解的患者,应考虑自体HCT巩固。
-
对于具有高危特征且完全代谢缓解的ALK阳性间变性大细胞淋巴瘤(ALCL)患者,自体HCT可作为选择;然而其作用受到维布妥昔单抗联合CHP(环磷酰胺、多柔比星和泼尼松)或CHEP(环磷酰胺、多柔比星、依托泊苷和泼尼松)方案的挑战。
-
目前不推荐对首次完全缓解的患者进行异基因HCT巩固性。
-
对于未达到完全缓解的患者,治疗应视为失败,应考虑异基因HCT。
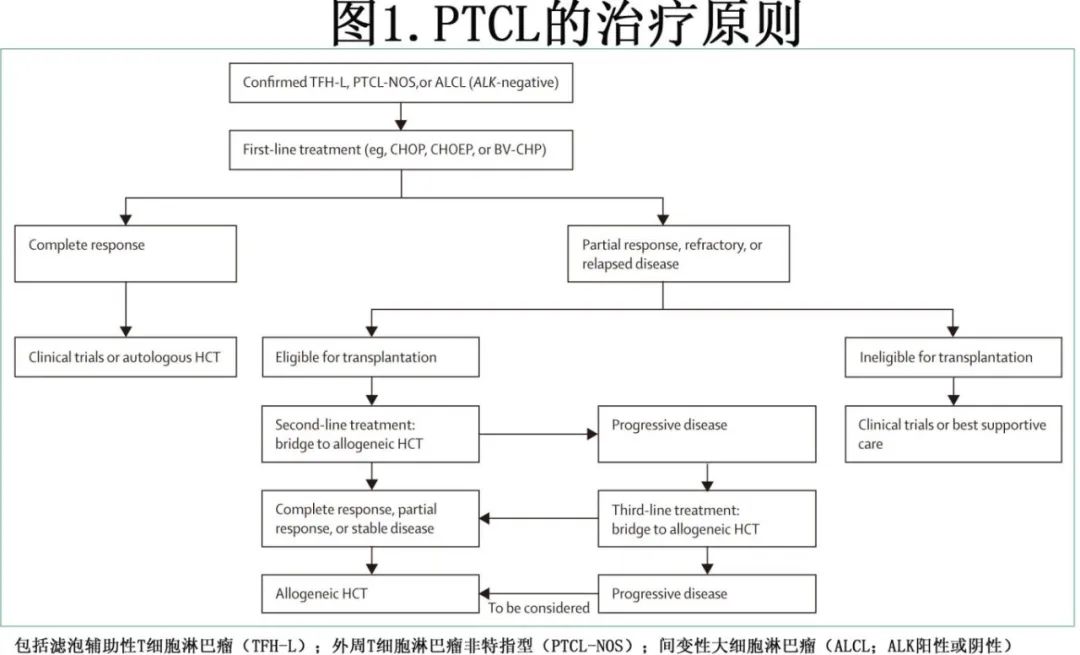
复发或难治性PTCL患者
-
异基因HCT是所有合格患者的首选治疗:
-
对一线治疗反应不足或难治的患者。
-
在首次完全缓解后复发的患者,无论之前的治疗如何(包括自体HCT)。
-
对于不适合异基因HCT的患者,如果患者在首次完全缓解后复发并达到第二次代谢完全缓解,可考虑自体HCT。
异基因HCT的时机(图1)
-
应尽早确定异基因HCT的资格。
-
一旦对一线治疗无反应变得明显,应立即开始寻找供者。
-
只要保持移植资格,无论挽救治疗的结果如何,都应进行异基因HCT。
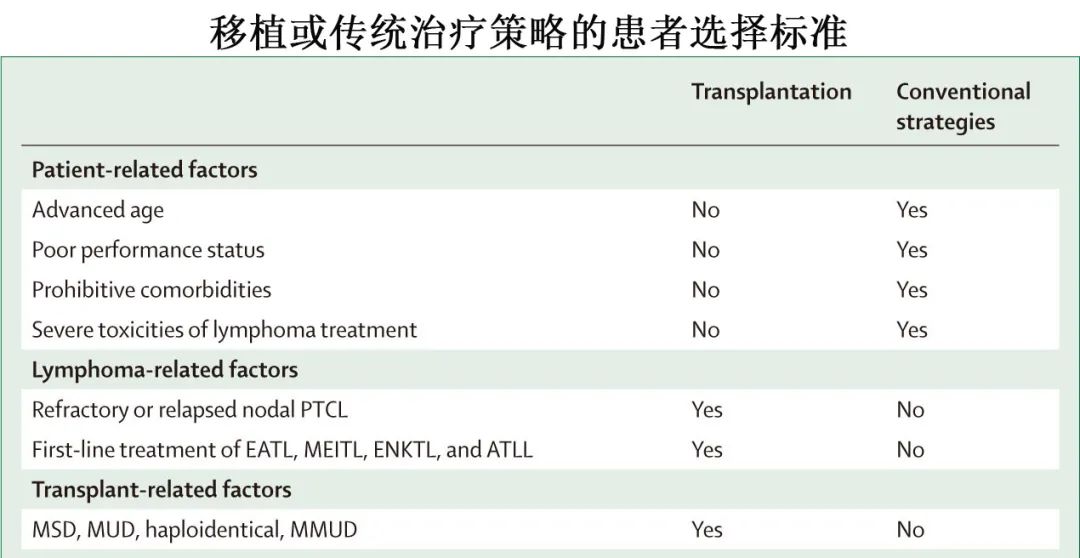
权衡年龄、体能状态和合并症对异基因HCT指征的影响
-
资格标准适用于所有PTCL亚型。
-
没有严格的年龄限制;年龄应结合其他风险因素进行评估。
-
HCT合并症指数(HCT-CI)评分≤2且表现状态良好的患者最适合异基因HCT;然而这些因素必须与年龄、合并症和疾病状态一起考虑,以确定异基因HCT的总体风险。
挽救治疗方案选择
-
鼓励参加临床试验。
-
首选基于铂类或吉西他滨的方案(例如DHAP [地塞米松、阿糖胞苷和顺铂或卡铂])。
-
对于CD30阳性非间变性大细胞淋巴瘤,维布妥昔单抗为基础方案联合化疗是另一种治疗选择。
-
对于间变性大细胞淋巴瘤,如果之前对维布妥昔单抗有反应,推荐维布妥昔单抗单药或联合治疗。
-
对于,ALK阳性间变性大细胞淋巴瘤,如果对于之前对BV无反应,可以考虑ALK抑制剂,如克唑替尼或brigatinib。
异基因HCT前的疾病状态(图1)
-
完全缓解的患者在异基因HCT后的结局最好,但部分缓解的患者也应直接进行异基因HCT。
-
稳定或进展性疾病的患者如果移植则可以预期长期生存,因此如果合格,应个体化考虑异基因HCT。
-
不鼓励通过反复挽救治疗来达到完全缓解;推荐进行不超过一到两线的挽救治疗。
-
尽管PET成像已成为标准方案,但其在PTCL和移植背景下的预后价值仍有待明确。
外周T细胞淋巴瘤亚型
-
组织学亚型不应成为决定是否进行异基因HCT的因素。
供者选择、干细胞来源和移植物抗宿主病(GVHD)预防
-
首选的供者顺序为:相合同胞供者、相合无关供者、半相合供者、不全相合无关供者。
-
外周血干细胞和骨髓都是可接受的移植物来源。
-
GVHD预防应根据受者和供者的HLA匹配程度、预处理类型和干细胞来源来指导。
预处理方案
-
没有明确证据表明清髓性预处理优于减低强度预处理(反之亦如此),因此推荐使用减低强度预处理,以扩大异基因HCT的可及性,并可能降低非复发死亡率。
-
由于没有数据支持特定的减低强度预处理方案,各中心应继续使用当地已建立的减低强度预处理方案。
移植后干预
-
没有数据支持对PTCL进行常规移植后干预。
-
不推荐常规监测残留疾病,因为缺乏标准化方法和证据支持其在指导干预中的有效性。
-
没有数据支持在PTCL中使用预防性或抢先性供者淋巴细胞输注(DLI)。
-
移植后免疫抑制减量的时机必须考虑个体复发和GVHD风险。
移植后复发的管理
-
免疫疗法方法:
-
如果可能,减少或停用免疫抑制剂。
-
单独使用DLI或与化疗或靶向治疗联合使用(如果有)。
-
应考虑进行第二次异基因HCT。
-
强烈建议将患者纳入前瞻性临床试验。
关于罕见PTCL亚型中allo-HCT 指征的建议
肝脾T细胞淋巴瘤(HSTCL)(图2)
-
在所有适合allo-HCT的患者中,应在诊断时开始寻找供者。
-
对于完全缓解或部分缓解的患者,强烈推荐在一线治疗后进行allo-HCT。
-
对于稳定或进展性疾病的患者,在allo-HCT前应考虑一次挽救治疗。
-
移植后维持治疗:由于复发风险非常高,应考虑预防性供者淋巴细胞输注(DLI)。
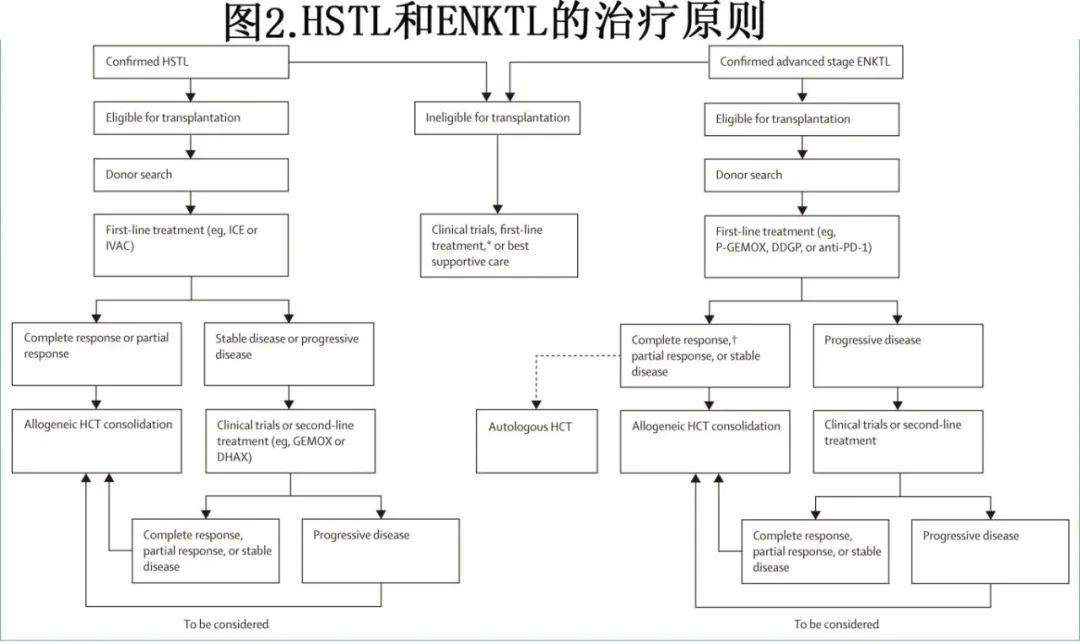
NK/T细胞淋巴瘤((图2)
-
局限期疾病的一线治疗:对于首次完全缓解的患者,通常不推荐allo-HCT。
-
晚期疾病的一线治疗:
-
应在诊断时开始寻找供者。
-
对于部分缓解或稳定疾病的患者,推荐allo-HCT,对于首次完全缓解的患者也可作为选择。
-
如果allo-HCT不可行,应考虑对完全缓解的患者进行自体HCT。
-
复发或难治性疾病:
-
对于所有符合条件的患者,allo-HCT是首选治疗。
-
如果使用了基于抗PD-1抗体的联合治疗,在allo-HCT前应有4-6周的洗脱期。
肠病相关T细胞淋巴瘤(EATL)(图3)
-
对于完全缓解的患者,推荐将自体HCT作为一线巩固。
-
对于所有符合条件的患者,如果对一线治疗反应不足或难治,或在首次完全缓解后复发(无论之前的治疗如何,包括自体HCT),allo-HCT是首选治疗。
-
必须仔细评估患者资格,考虑与相关胃肠道疾病相关的脆弱性。
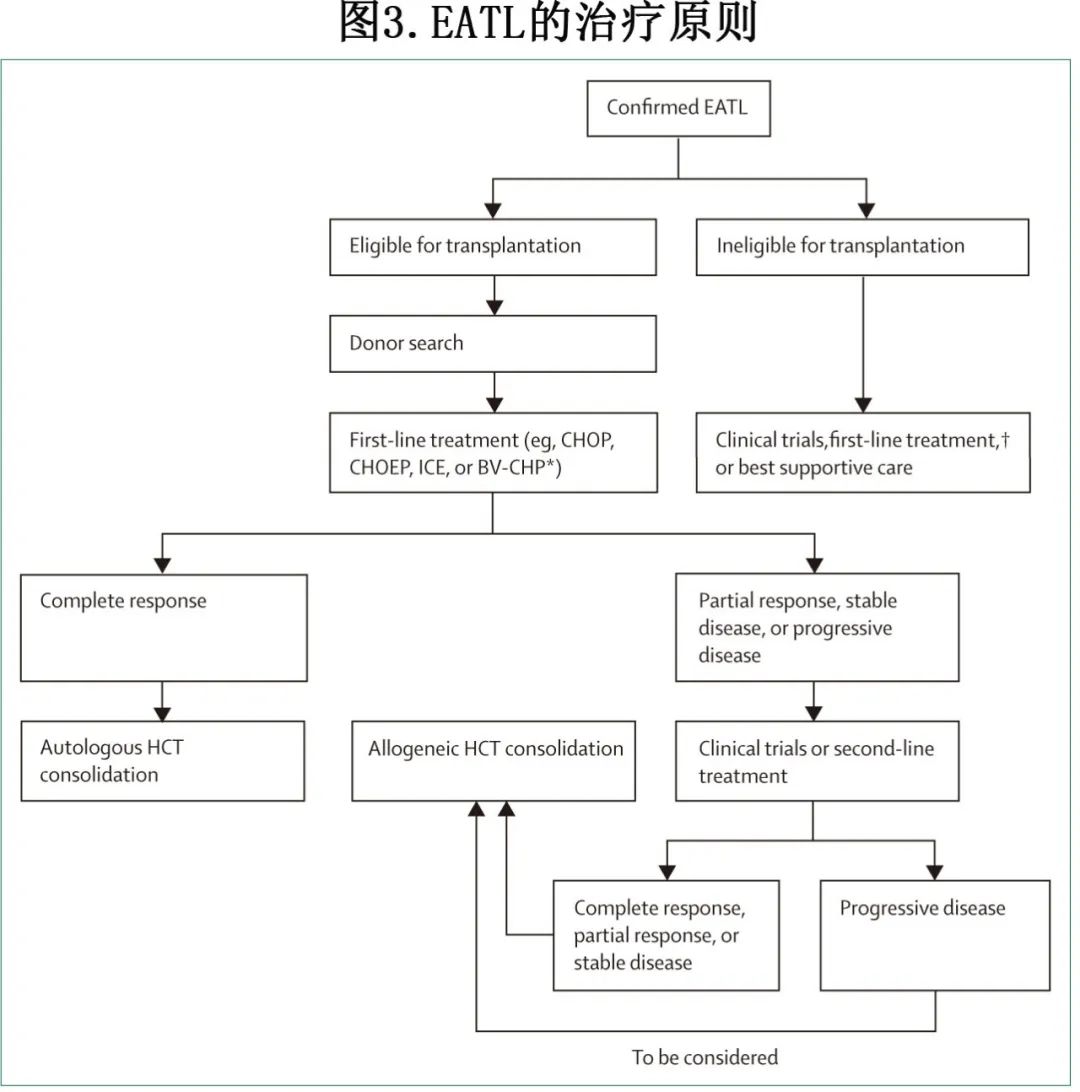
单形性上皮性肠T细胞淋巴瘤(MEITL)(图4)
-
对于符合条件的患者,在诊断时开始寻找供者。
-
可考虑将allo-HCT作为一线治疗的巩固,用于完全缓解、部分缓解或稳定疾病的患者。
-
如果allo-HCT不可行,应考虑对完全缓解的患者进行自体HCT。
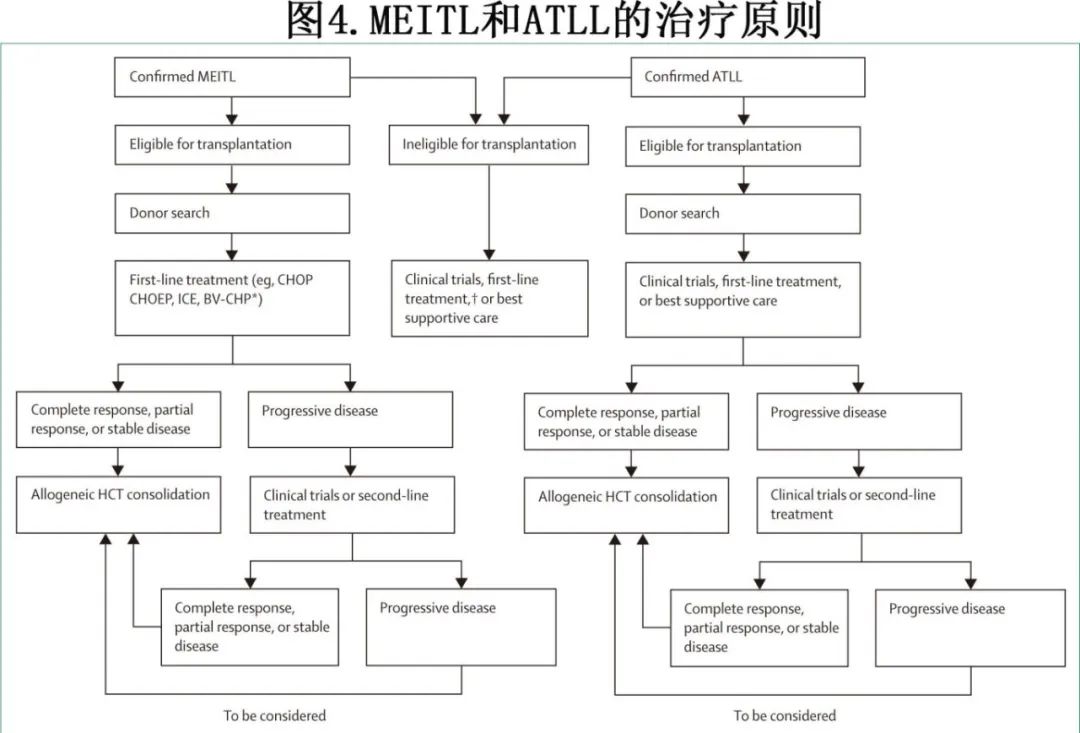
成人T细胞白血病/淋巴瘤(ATLL)(图4)
-
对于慢性高危、急性或淋巴瘤亚型患者,应在诊断时评估allo-HCT的资格并考虑寻找供者。
-
一旦达到完全缓解、部分缓解或稳定疾病,应考虑将allo-HCT作为一线治疗选择。
-
如果一线治疗中未进行allo-HCT,在复发或难治情况下应考虑使用allo-HCT。
参考文献
Lancet Haematol . 2025 Jul;12(7):e542-e554. doi: 10.1016/S2352-3026(25)00073-0.
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)