首页 > 医疗资讯/ 正文
亮点总结
-
研究首次证明,DNA甲基化标志物RIMS1在H. pylori根除后高风险人群中,能显著区分不同胃癌发生风险。
-
基于DNA甲基化水平设定的阈值,可精准识别“超级高危”亚群,提示其需更频繁的胃镜筛查。
-
该研究为胃癌精准风险分层提供了坚实的分子依据,未来有望优化筛查策略,减少漏诊和过度检查。
研究概要
在胃癌防控领域,如何精准识别高危人群并实施个性化筛查方案,成为医学界关注的焦点。本文发表在2025年Gut杂志上,由日本多家顶尖研究机构共同完成一项大规模前瞻性队列研究,首次验证DNA甲基化标志物RIMS1在H. pylori根除后高危人群中的风险预测价值。研究共纳入1757名经过成功根除H. pylori感染且表现为开放性胃窦萎缩的健康受试者,通过内镜活检样本检测DNA甲基化水平,随访五年,筛查出27例胃癌病例。

研究重点在于:首先,比较甲基化水平最高四分位(Q4)与最低四分位(Q1)人群的胃癌发生风险,发现Q4组的风险显著升高(HR约5.7-7.7);其次,制定15.7%的甲基化阈值,将风险超高人群(超级高危)筛查频次由每两年一次提升至每年一次,极大提高筛查的精确性和针对性。此项成果为胃癌早期筛查的个性化与精准化提供了重要的分子依据,为类似肿瘤筛查策略的优化提供了理论基础。
研究背景
胃癌依然是全球范围内发病率和死亡率较高的消化系统恶性肿瘤之一。2022年数据显示,全球约有968,000例新发病例,死于胃癌的死亡人数达66万,占据世界癌症死亡前列。Helicobacter pylori(简称H. pylori)感染被公认为胃癌的重要致病因素。随着抗菌治疗的推广,H. pylori的根除已成为预防胃癌的核心策略,但根除后仍有0.5%-1.2%的感染者可能出现胃癌,现行指南建议对所有H. pylori根除后的人群每两年进行一次胃镜筛查。
然而,鉴于受检人群日益庞大,如何精确筛查、避免资源浪费成为挑战。传统的临床危险因素(如年龄、性别、活检后粘膜变性程度等)在风险分层中表现有限,因此迫切需要寻找可靠的生物标志物,以实现个性化、精准的风险评估。
近年来,基于基因组和表观遗传学的研究表明,DNA甲基化的异常积累——即“表观遗传突变负担”,在多个炎症相关癌种中与风险密切相关。⽤于胃癌的研究亦表明,胃黏膜中多基因甲基化水平的升高,与胃癌风险显著相关。这为通过海量分子信息精准筛查高危人群提供了技术基础。
研究方法
本研究为多中心前瞻性队列,采用标准操作从2015年至2019年间在日本68个机构招募符合条件的H. pylori根除且表现为开放性胃窦萎缩的健康志愿者。入组者均经过多项检测确认H. pylori感染状态,根除成功后在胃窦和胃体活检样本中检测DNA甲基化水平,主要标志物为RIMS1基因。
利用亚硫酸盐转化-焦磷酸测序技术(pyrosequencing)量化甲基化水平,并将最大值(胃窦或胃体样本)作为风险指标。随访期内每年一轮内镜筛查,记录胃癌发病情况。
研究的主要分析内容包括:比较甲基化水平四分位(Q1-Q4)组的胃癌发生率,采用Cox比例风险模型计算风险比(HR),并根据风险模型开发出临床可用的甲基化阈值,以优势病例控制避免漏诊。
研究结果
受试者基本情况
-
总共纳入1757名志愿者(男女比例各半),中位年龄64岁。
-
随访中,1624人至少进行一次内镜检查,平均随访时间约4年前后。
-
在随访期内,出现27例原发性胃癌,其中73%的病例为腺癌,部分为低分化型。
DNA甲基化分布特征
-
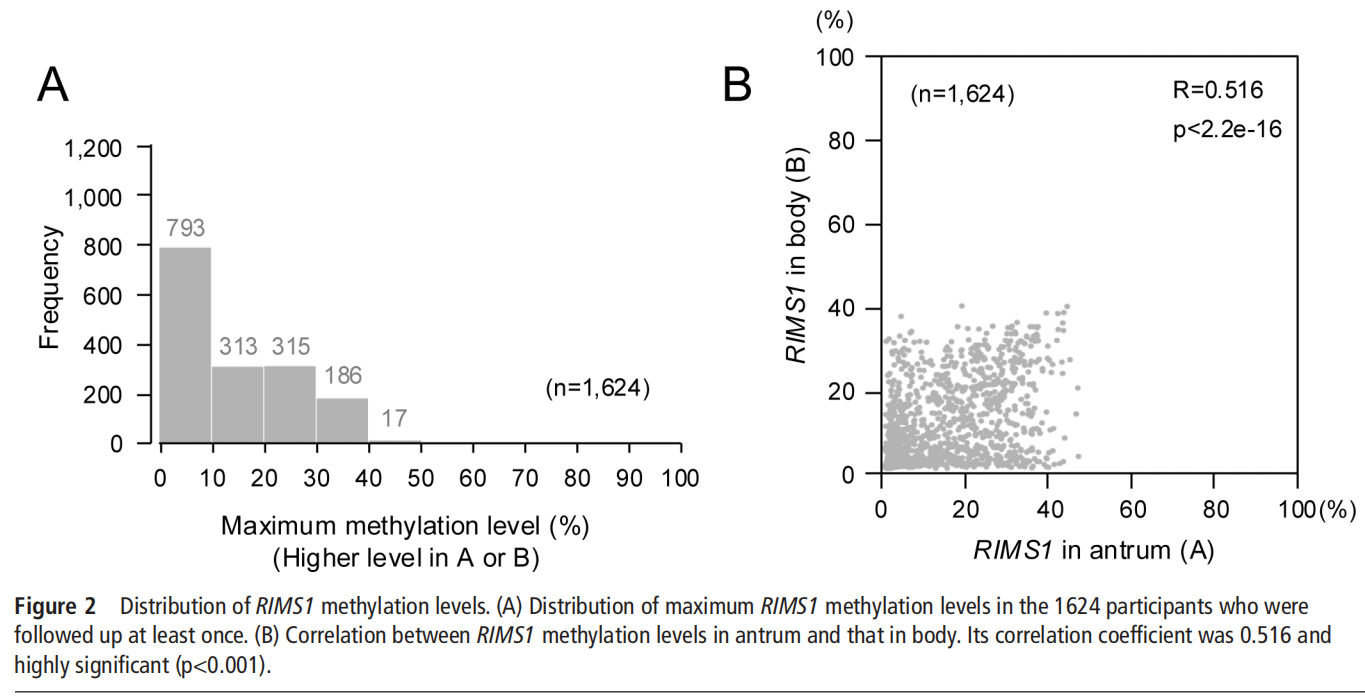
甲基化水平在随机人群中呈广泛分布,最大值最低的48.8%的受试者甲基化水平低于10%。
-
在线Supplementary图显示,胃窦和胃体的甲基化水平高度相关(相关系数R=0.516,P<0.001)。
-
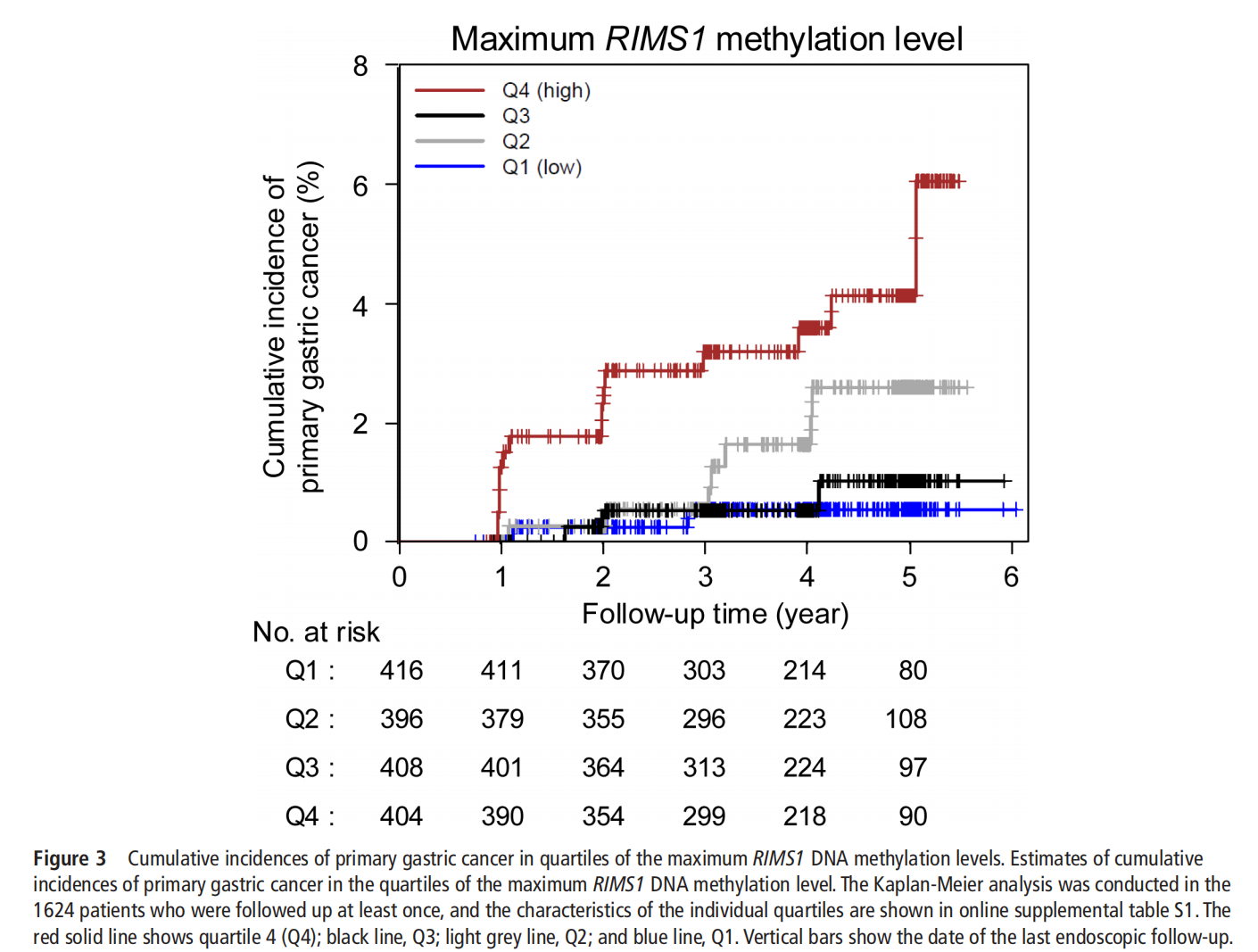
甲基化水平越高,胃癌风险越大,风险在四分位(Q4)显著升高。
风险分层效果
-
Q4人群的胃癌发生率为972.8/10万/年,而Q1人群仅127.1/10万/年。
-
Cox回归分析显示,Q4组相较Q1,风险增加约7.7倍(未经调整)和5.7倍(调整年龄、性别后),差异统计学显著(P<0.05)。
-
亚组分析亦证实这一趋势,年龄≥60岁、女性子群中风险增强明显。
临界值的建立与应用
-
通过模型拟合,确定了甲基化水平25.7%的阈值(对应风险概率)作为“超级高危”筛查阈。
-
按照日本2年一次筛查的建议,将该阈值调整为甲基化水平29.2%,在NNS(每筛查一个人,发现一例癌症所需人次)为1000基础上,评估出进一步划定的风险阈。
结论
高甲基化水平的受试者,尤其是在25.7%以上,即为“超级高危”,需要增加筛查频率。此风险标志物的应用潜力巨大,有望推动临床风险评估从经验判断转向分子指标导向的决策。
讨论
本研究创新性地在临床高危人群中验证了DNA甲基化标志物RIMS1作为预测胃癌风险的有效工具。此前多项研究已提示甲基化水平与胃癌风险相关,但缺乏前瞻性大样本验证。此次多中心研究以严谨的方法确认了甲基化水平的风险分层能力,尤其是在H. pylori根除后患者中,显著提升了筛查的精准度。
此外,利用临界值识别“超级高危”亚群,为临床提供了具体可行的筛查策略调整依据。制定年筛计划,结合分子风险指标,有望降低胃癌的早期诊断漏失率,改善预后。
未来,结合遗传信息、环境因素,可进一步完善风险模型。此外,扩展到无萎缩或轻度萎缩人群,探索更广泛的应用范围,也具备重要意义。该研究还为其他炎症相关癌种的筛查提供了表观遗传学新的思路和方法,为精准肿瘤预防奠定理论基础。
原始出处
Yamada H, et al. Precision risk stratification of primary gastric cancer after eradication of H. pylori by a DNA methylation marker: a multicentre prospective studyGut 2025;0:1–9. doi:10.1136/gutjnl-2025-335039
- 搜索
-
- 1000℃李寰:先心病肺动脉高压能根治吗?
- 1000℃除了吃药,骨质疏松还能如何治疗?
- 1000℃抱孩子谁不会呢?保护脊柱的抱孩子姿势了解一下
- 1000℃妇科检查有哪些项目?
- 1000℃妇科检查前应做哪些准备?
- 1000℃女性莫名烦躁—不好惹的黄体期
- 1000℃会影响患者智力的癫痫病
- 1000℃治女性盆腔炎的费用是多少?
- 标签列表
-
- 星座 (702)
- 孩子 (526)
- 恋爱 (505)
- 婴儿车 (390)
- 宝宝 (328)
- 狮子座 (313)
- 金牛座 (313)
- 摩羯座 (302)
- 白羊座 (301)
- 天蝎座 (294)
- 巨蟹座 (289)
- 双子座 (289)
- 处女座 (285)
- 天秤座 (276)
- 双鱼座 (268)
- 婴儿 (265)
- 水瓶座 (260)
- 射手座 (239)
- 不完美妈妈 (173)
- 跳槽那些事儿 (168)
- baby (140)
- 女婴 (132)
- 生肖 (129)
- 女儿 (129)
- 民警 (127)
- 狮子 (105)
- NBA (101)
- 家长 (97)
- 怀孕 (95)
- 儿童 (93)
- 交警 (89)
- 孕妇 (77)
- 儿子 (75)
- Angelababy (74)
- 父母 (74)
- 幼儿园 (73)
- 医院 (69)
- 童车 (66)
- 女子 (60)
- 郑州 (58)